






高中化学苏教版 (2019)必修 第二册专题6 化学反应与能量变化第二单元 化学反应中的热集体备课课件ppt
展开1 | 放热反应和吸热反应
第二单元 化学反应中的热
必备知识 清单破
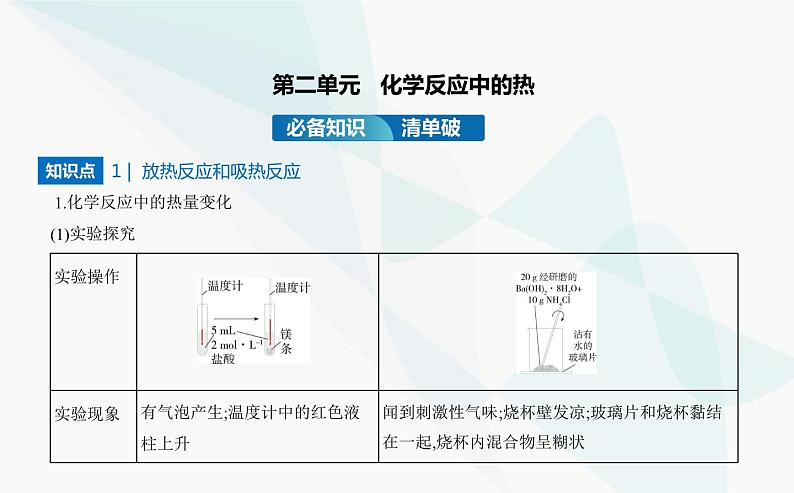
1.化学反应中的热量变化(1)实验探究
(2)结论:化学反应中有新物质生成的同时,必然伴随着能量变化,通常表现为热量的释放或吸 收。2.放热反应与吸热反应(1)概念①放热反应:放出热的反应。②吸热反应:吸收热的反应。易错分析 吸热反应、放热反应均是对化学反应而言。像核反应、物质的三态变化(气→ 液→固)、浓硫酸的稀释等过程都能放出热量,但它们不属于放热反应,因为它们不属于化学 变化。(2)常见的放热反应和吸热反应
特别提醒 并非所有的分解反应都为吸热反应,如2H2O2 2H2O+O2↑为放热反应。并非所有的化合反应都为放热反应,如CO2+C 2CO为吸热反应。
1.概念:定量地表示一个特定的反应放出或吸收的热量的化学方程式。2.意义:不仅表明了化学反应中的物质变化,也表明了化学反应中的能量变化。3.书写方法
2 | 热化学方程式
特别提醒 (1)热化学方程式中要标明所有物质在反应条件下的状态(气态、液态、固态分 别用g、l、s表示)。(2)注意ΔH的正、负号,负值表示在该条件下反应放热,正值表示在该条件下反应吸热。(3)热化学方程式中各物质前的化学计量数不表示分子个数,只表示物质的量,因此,它可以是 整数,还可以是分数。化学计量数与ΔH的数值成正比。
1.热值:指一定条件下单位质量的可燃物完全燃烧所放出的热,常用单位是kJ·g-1。2.提高燃料的使用效率(1)当今世界上使用最多的能源是化石燃料——煤、石油、天然气。(2)化石燃料使用中存在的问题①通常燃料燃烧放出的热量不可能全部转化为有用功,总有部分热量转化为废热排出或损耗 掉。②煤等化石燃料的燃烧常常伴随着大量烟尘、CO、SO2、氮氧化物(NOx)等有毒有害物质的 排放。③有些煤中灰分含量大,水分多,热值较低。
3 | 燃料燃烧释放的能量 氢燃料的应用前景
(3)解决燃料燃烧存在的问题和研究方向①节约现有能源。②提高燃料的使用效率,减少对环境的污染,如把石油、煤等化石燃料转化为清洁燃料。③开发氢能、水能、太阳能、风能等更清洁、更高效的能源。知识拓展 太阳能的利用
3.氢燃料的应用前景(1)氢能的优点 氢气的热值在普通燃料中是最高的,且氢气燃烧的产物只有水,不会产生对环境有害的 污染物,是一种清洁燃料。(2)氢能利用存在的问题①廉价的制氢技术是首要难点。原因:制氢需要消耗大量的能量且效率低。②安全可靠的贮存氢气的方法是关键。原因:H2密度小、熔点低、难液化。(3)氢燃料的应用前景①发射人造卫星和载人飞船的运载火箭常用液氢作燃料。②氢燃料混合动力有轨电车。③氢燃料电池。
知识辨析1.氢氧化钠固体溶于水,溶液的温度升高,该变化为放热反应。这种说法对吗?2.吸热反应需要加热才能发生,放热反应都不需要加热就可以发生。这种说法对吗?3.只要有化学键的断裂,发生的一定是化学反应。这种说法对吗?4.热值即反应放出或吸收的热量,可用ΔH表示。这种说法对吗?
一语破的1.不对。氢氧化钠固体溶于水属于物理变化,是放热过程,但不是放热反应。2.不对。需要加热才能发生的反应不一定是吸热反应,如硫与铁的反应需要加热才能发生,但 是放热反应;吸热反应不一定需要加热才能发生,如Ba(OH)2·8H2O晶体和NH4Cl晶体的反应是 吸热反应,但不需要加热就能发生。3.不对。化学反应必须有旧键断裂和新键形成。4.不对。热值是指在一定条件下单位质量的可燃物完全燃烧所放出的热量,常用单位是kJ·g-1。ΔH的常用单位是kJ·ml-1。
1 | 对化学反应中能量变化的理解
关键能力 定点破
1.化学反应中能量变化的原因(1)化学反应中能量变化与化学键的关系——微观角度 特别提醒 化学反应的实质是旧化学键的断裂和新化学键的形成。
(2)化学反应的能量变化与物质内部能量的关系——宏观角度
2.化学反应中能量的转化形式 主要是化学能与热能之间的相互转化,也有其他形式的能量转化,如化学能可以转化成 光能、电能等。
典例 反应A(g)+B(g) C(g)的能量变化如图所示,下列有关说法正确的是( ) A.1 ml A(g)的能量高于1 ml C(g)的能量B.该反应放出的能量为(E3-E1)kJC.X(g)是该反应的催化剂D.该反应分为两个阶段,第一个阶段吸热,第二个阶段放热
思路点拨 由题图得出的相关信息有:反应A(g)+B(g) C(g)为放热反应,且放出的热量为(E2-E1)kJ;A(g)+B(g) X(g)为吸热反应,且吸收的热量为(E3-E2)kJ;X(g) C(g)为放热反应,且放出的热量为(E3-E1)kJ。
解析 1 ml A(g)+1 ml B(g)的总能量高于1 ml C(g)的能量,不能判断1 ml A(g)的能量与1 ml C(g)的能量的高低,A错误;该反应放出的能量为(E2-E1)kJ,B错误;X(g)是该反应的中间产 物,不是催化剂,C错误;该反应分为两个阶段,第一阶段反应物的总能量小于生成物的总能量, 为吸热反应,第二阶段反应物的总能量大于生成物的总能量,为放热反应,D正确。
1.判断热化学方程式正误的方法——“四看法”(1)看各物质在反应条件下的聚集状态是否正确。(2)看ΔH的“+”“-”是否正确。“+”一般省略。(3)看ΔH的单位是否正确。(4)看ΔH数值与化学计量数是否相对应。如果化学计量数改变,则ΔH也要按比例改变。当反 应逆向进行时,其ΔH'与反应正向进行时的ΔH的数值相等,正、负号相反。2.化学反应中能量变化的计算方法(1)根据反应物和生成物的总能量计算ΔHΔH=生成物总能量-反应物总能量,例如,化学反应 N2(g)+ H2(g) NH3(g)的能量变化如图所示:
2 | 判断热化学方程式正误的方法及化学反应中ΔH的计算
由上图可知,该反应是放热反应,生成1 ml NH3(g)放出的热量为(b-a) kJ。(2)根据键能计算ΔHΔH=反应物的键能总和-生成物的键能总和知识拓展 断开气态物质中1 ml某种共价键生成气态原子需要吸收的能量,就是该共价键
的键能。共价键的键能越大,该共价键越牢固。
典例 H2和I2在一定条件下能发生反应H2(g)+I2(g) 2HI(g),能量变化如图所示。
断开1 ml H—I键需要吸收的能量是 ( )A. kJ B. kJC. kJ D. kJ
化学苏教版 (2019)第二单元 化学反应中的热优质课件ppt: 这是一份化学苏教版 (2019)<a href="/hx/tb_c4002515_t3/?tag_id=26" target="_blank">第二单元 化学反应中的热优质课件ppt</a>,文件包含62化学反应中的热分层练习-高一化学同步精品课堂苏教版必修第二册原卷版docx、62化学反应中的热分层练习-高一化学同步精品课堂苏教版必修第二册解析版docx等2份课件配套教学资源,其中PPT共0页, 欢迎下载使用。
高中化学苏教版 (2019)必修 第二册第二单元 化学反应中的热课文配套课件ppt: 这是一份高中化学苏教版 (2019)必修 第二册<a href="/hx/tb_c4002515_t3/?tag_id=26" target="_blank">第二单元 化学反应中的热课文配套课件ppt</a>,共42页。PPT课件主要包含了放热反应与吸热反应,观察思考,化学能,1放热反应,2吸热反应,热化学方程式,交流讨论,拓展视野,燃料燃烧释放的能量,几种燃料的热值等内容,欢迎下载使用。
必修 第二册第二单元 化学反应中的热课文配套课件ppt: 这是一份必修 第二册第二单元 化学反应中的热课文配套课件ppt,共53页。PPT课件主要包含了自主预习·新知导学,合作探究·释疑解惑,课堂小结,探究任务1,探究任务2,答案B等内容,欢迎下载使用。













