



还剩24页未读,
继续阅读
所属成套资源:2023-2024学年九年级上册化学(课件+练习)沪教版
成套系列资料,整套一键下载
初中化学沪教版九年级上册第1节 构成物质的基本微粒教课课件ppt
展开
这是一份初中化学沪教版九年级上册第1节 构成物质的基本微粒教课课件ppt,共32页。PPT课件主要包含了原子的探索,新课引入,原子核,原子的微观结构,ArH,新课讲解,随堂练习,答案C,作业布置等内容,欢迎下载使用。
我国第一颗原子弹爆炸(附高清视频)
人类对于原子的探索(附高清视频)
原子的质量和体积都很小(附高清视频)
原子质量与相对原子质量的区别
相对原子质量的计算(附高清视频)
人类探索的脚步从未停止过
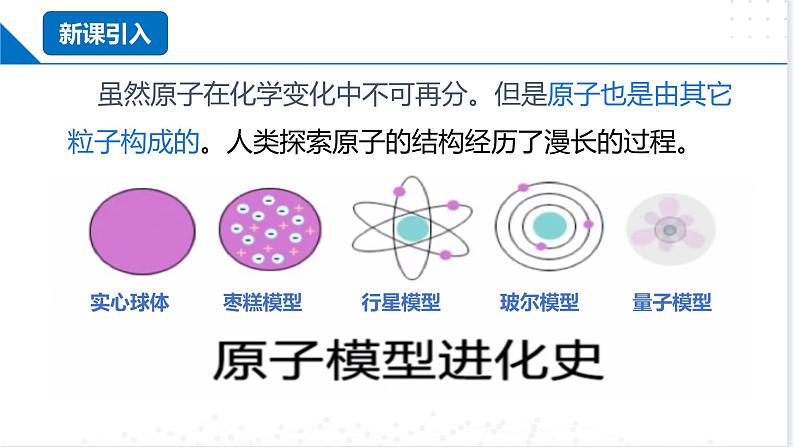
虽然原子在化学变化中不可再分。但是原子也是由其它粒子构成的。人类探索原子的结构经历了漫长的过程。
实心球体 枣糕模型 行星模型 玻尔模型 量子模型
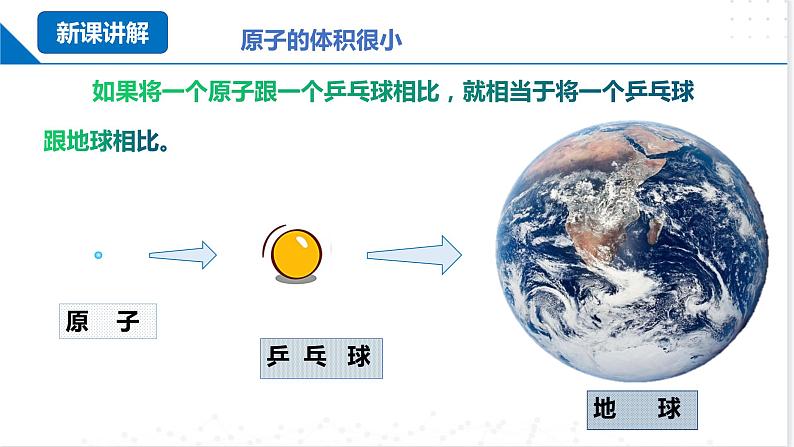
如果将一个原子跟一个乒乓球相比,就相当于将一个乒乓球跟地球相比。
核电荷数:原子核所带的电荷数
核电荷数 质子数
1. 原子是由__________与__________构成的。2. 原子核是由__________和__________构成的。3. 每个质子带1个单位的__________,每个电子带1个单位的__________,中子__________。4. 由于原子核内质子所带电荷与核外电子的电荷__________,但__________,因此,原子__________。5. 原子核所带的正电荷数(核电荷数)就等于核内的__________,也等于__________的数目。
三、核电荷数、质子数、中子数、电子数的关系
原子的种类不同,质子数______(相同/不同)【原子分类的依据】。相同原子的质子数=核电荷数=___________数。所有的原子都有中子吗?质子数和中子数 (一定/不一定)相等。由于原子核和核外电子所带电荷,电量 ,电性 所以整个原子不带电(电中性)。分子带电吗?
在分子、原子、质子、中子、电子这些粒子中,选择合适的答案。 (1)能直接构成物质的粒子有: (2)在化学变化中最小的粒子有: (3)不显电性的粒子有: (4)带正电的粒子有: (5)带负电的粒子有: (6)构成原子的微粒有: (7)构成原子核的微粒有:
原子一般由质子、中子和电子构成,它们(1个粒子)的质量如下表所示:
一个碳原子的质量是:1.993×10-26千克;一个氧原子的质量是:2.657×10-26千克;一个铁原子的质量是:9.288×10-26千克
由于原子质量的数值太小,书写和使用都很不方便,怎么办?
相对原子质量就是以一种碳原子质量的1/12(1.66×10-27Kg)为标准,其他原子的质量跟它相比较所得到的比。
某原子的相对原子质量(Ar)=
例: 一个氢原子的质量为1.67×10-27Kg,一个碳12原子的质量为 1.993×10-26Kg,求氢原子的相对原子质量。(写出计算过程,结果保留整数)
1.67×10-27 kg
1.993×10-26kg
m某原子
(2)相对原子质量的单位是: 。(3)原子实际质量的单位是: 。
比较原子质量与相对原子质量
(1) 相对原子质量________ (“等于”或“不等于”)原子的实际质量,是个比值。
1.相对原子质量的单位:相对原子质量是一个比值,单位为“1”,一般不读出也不写出。2.由于电子质量很小,甚至可以忽略不计,所以相对原子质量在数值上约等于质子数与中子数之和,即相对原子质量≈质子数+中子数。
相对原子质量是一个比值,它不是一个原子的实际质量,但能反映出一个原子实际质量的相对大小。原子的质量越大,其相对原子质量也越大。不同种原子的实际质量之比等于它们的相对原子质量之比。如氢的相对原子质量为1,碳的相对原子质量为12,则一个碳原子的实际质量也是一个氢原子实际质量的12倍。
相对分子质量的定义与计算
Mr= 16×2 = 32
Mr = 12+ 16×2 = 44
Mr= 1×2 + 32 + 16×4 = 98
化学式中各原子的相对原子质量的总和,就是相对分子质量(符号为Mr)
Mr= 1×2 + 16 = 18
1、是化学式中各原子的相对原子质量的总和
如何理解相对分子质量?
单位:是“1”,通常省略不想
1.计算相对分子质量(写出过程)H:1 O:16 N:14 Cu:64 Cl:35.5 Ca:40 S:32
(1)CO2 _______________________________(2)Ca(OH)2 ___________________________(3)CaCO3 ____________________________(4)CuSO4 _____________________________(5)NH4NO3 ___________________________(6)2HCl ______________________________
=12+16×2=44
=40+(16+1)×2=74
=40+12+16×3=100
=64+32+16×4=160
=14×2+4×1+16×3=80
=2×(1+35.5)=73
例1.(2023四川乐山二模)下列关于原子的叙述正确的是( )A.原子只能构成分子,不能构成物质B.原子中不存在带电粒子,故原子不显电性C.原子是化学变化中的最小粒子D.任何原子的原子核都是由质子和中子构成的
例2.(2023新疆中考真题)下列说法正确的是( )A.SO2中含有氧分子B.2H表示两个氢分子C.O2中氧元素的化合价为-2价D.CO表示一个一氧化碳分子是由一个碳原子和一个氧原子构成
例3.(2023福建莆田二模)下列叙述中不正确的是( )①原子是化学变化中的最小粒子; ②原子是不能再分的粒子 ;③一切物质都是由原子直接构成的;④一切原子核都是由质子和中子构成的 ;⑤原子不显电性 ;⑥原子之间有间隔A.①和②B.②③和④C.③和⑤D.③和⑥
例4.(2023·四川成都·统考中考真题)化学家张青莲主持测定了铟、铱、锌等元素相对原子质量的新值。碳12原子的质量为1.993x10-26Kg,一种锌原子的质量为1.096x10-25Kg,,该锌原子的相对原子质量是( )
A.12B.64C.66D.
1.(2021·山东菏泽·统考中考真题)下列说法中,错误的是( )A.作为相对原子质量标准的碳原子是由6个中子和6个质子构成的B.相对原子质量是以碳原子质量的1/12作为标准C.相对原子质量和原子的实际质量是一个概念 D.一种原子的相对原子质量近似等于原子核内质子数和中子 数之和
2.(2023·河南·统考二模)化学变化中的最小粒子是( ) A.分子 B.原子 C.质子 D.电子3.(2023·河北·统考一模)原子的质量主要集中在( )A.质子 B.中子 C.电子 D.原子核
4.据报道,上海某医院正在研究用放射性碘治疗肿瘤。 这种碘原子的核电荷数为53,相对原子质量为125。下列关于这种原子的说法中,错误的是( )A.中子数为72 B.质子数为72 C.电子数为53 D.质子数和中子数之和为1255.用其质量的1/12作为相对原子质量的标准的碳原子 相对原子的质量是( ) A.12g B.12 C.1/12g D.1/12
7.有一种放射性碘(I)原子,常用作核反应堆的燃料棒,其质子数为53,中子数为78。该碘原子的相对原子质量为( ) A.53 B.78C.127D.131
6、北斗三号使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,钛原子的核外电子数为( ) A.22 B.48 C.70 D.26
8、已知在某原子中共有的粒子数为 40,其中不带电的粒子数为 14,则该原子的相对原子质量为( ) A.54 B.13 C.27 D.26
通过本节课的学习,同学们谈谈有哪些收获?
1.完成配套练习册;2.预习 核外电子的排布及离子;3.书面作业:课后习题10、11。
我国第一颗原子弹爆炸(附高清视频)
人类对于原子的探索(附高清视频)
原子的质量和体积都很小(附高清视频)
原子质量与相对原子质量的区别
相对原子质量的计算(附高清视频)
人类探索的脚步从未停止过
虽然原子在化学变化中不可再分。但是原子也是由其它粒子构成的。人类探索原子的结构经历了漫长的过程。
实心球体 枣糕模型 行星模型 玻尔模型 量子模型
如果将一个原子跟一个乒乓球相比,就相当于将一个乒乓球跟地球相比。
核电荷数:原子核所带的电荷数
核电荷数 质子数
1. 原子是由__________与__________构成的。2. 原子核是由__________和__________构成的。3. 每个质子带1个单位的__________,每个电子带1个单位的__________,中子__________。4. 由于原子核内质子所带电荷与核外电子的电荷__________,但__________,因此,原子__________。5. 原子核所带的正电荷数(核电荷数)就等于核内的__________,也等于__________的数目。
三、核电荷数、质子数、中子数、电子数的关系
原子的种类不同,质子数______(相同/不同)【原子分类的依据】。相同原子的质子数=核电荷数=___________数。所有的原子都有中子吗?质子数和中子数 (一定/不一定)相等。由于原子核和核外电子所带电荷,电量 ,电性 所以整个原子不带电(电中性)。分子带电吗?
在分子、原子、质子、中子、电子这些粒子中,选择合适的答案。 (1)能直接构成物质的粒子有: (2)在化学变化中最小的粒子有: (3)不显电性的粒子有: (4)带正电的粒子有: (5)带负电的粒子有: (6)构成原子的微粒有: (7)构成原子核的微粒有:
原子一般由质子、中子和电子构成,它们(1个粒子)的质量如下表所示:
一个碳原子的质量是:1.993×10-26千克;一个氧原子的质量是:2.657×10-26千克;一个铁原子的质量是:9.288×10-26千克
由于原子质量的数值太小,书写和使用都很不方便,怎么办?
相对原子质量就是以一种碳原子质量的1/12(1.66×10-27Kg)为标准,其他原子的质量跟它相比较所得到的比。
某原子的相对原子质量(Ar)=
例: 一个氢原子的质量为1.67×10-27Kg,一个碳12原子的质量为 1.993×10-26Kg,求氢原子的相对原子质量。(写出计算过程,结果保留整数)
1.67×10-27 kg
1.993×10-26kg
m某原子
(2)相对原子质量的单位是: 。(3)原子实际质量的单位是: 。
比较原子质量与相对原子质量
(1) 相对原子质量________ (“等于”或“不等于”)原子的实际质量,是个比值。
1.相对原子质量的单位:相对原子质量是一个比值,单位为“1”,一般不读出也不写出。2.由于电子质量很小,甚至可以忽略不计,所以相对原子质量在数值上约等于质子数与中子数之和,即相对原子质量≈质子数+中子数。
相对原子质量是一个比值,它不是一个原子的实际质量,但能反映出一个原子实际质量的相对大小。原子的质量越大,其相对原子质量也越大。不同种原子的实际质量之比等于它们的相对原子质量之比。如氢的相对原子质量为1,碳的相对原子质量为12,则一个碳原子的实际质量也是一个氢原子实际质量的12倍。
相对分子质量的定义与计算
Mr= 16×2 = 32
Mr = 12+ 16×2 = 44
Mr= 1×2 + 32 + 16×4 = 98
化学式中各原子的相对原子质量的总和,就是相对分子质量(符号为Mr)
Mr= 1×2 + 16 = 18
1、是化学式中各原子的相对原子质量的总和
如何理解相对分子质量?
单位:是“1”,通常省略不想
1.计算相对分子质量(写出过程)H:1 O:16 N:14 Cu:64 Cl:35.5 Ca:40 S:32
(1)CO2 _______________________________(2)Ca(OH)2 ___________________________(3)CaCO3 ____________________________(4)CuSO4 _____________________________(5)NH4NO3 ___________________________(6)2HCl ______________________________
=12+16×2=44
=40+(16+1)×2=74
=40+12+16×3=100
=64+32+16×4=160
=14×2+4×1+16×3=80
=2×(1+35.5)=73
例1.(2023四川乐山二模)下列关于原子的叙述正确的是( )A.原子只能构成分子,不能构成物质B.原子中不存在带电粒子,故原子不显电性C.原子是化学变化中的最小粒子D.任何原子的原子核都是由质子和中子构成的
例2.(2023新疆中考真题)下列说法正确的是( )A.SO2中含有氧分子B.2H表示两个氢分子C.O2中氧元素的化合价为-2价D.CO表示一个一氧化碳分子是由一个碳原子和一个氧原子构成
例3.(2023福建莆田二模)下列叙述中不正确的是( )①原子是化学变化中的最小粒子; ②原子是不能再分的粒子 ;③一切物质都是由原子直接构成的;④一切原子核都是由质子和中子构成的 ;⑤原子不显电性 ;⑥原子之间有间隔A.①和②B.②③和④C.③和⑤D.③和⑥
例4.(2023·四川成都·统考中考真题)化学家张青莲主持测定了铟、铱、锌等元素相对原子质量的新值。碳12原子的质量为1.993x10-26Kg,一种锌原子的质量为1.096x10-25Kg,,该锌原子的相对原子质量是( )
A.12B.64C.66D.
1.(2021·山东菏泽·统考中考真题)下列说法中,错误的是( )A.作为相对原子质量标准的碳原子是由6个中子和6个质子构成的B.相对原子质量是以碳原子质量的1/12作为标准C.相对原子质量和原子的实际质量是一个概念 D.一种原子的相对原子质量近似等于原子核内质子数和中子 数之和
2.(2023·河南·统考二模)化学变化中的最小粒子是( ) A.分子 B.原子 C.质子 D.电子3.(2023·河北·统考一模)原子的质量主要集中在( )A.质子 B.中子 C.电子 D.原子核
4.据报道,上海某医院正在研究用放射性碘治疗肿瘤。 这种碘原子的核电荷数为53,相对原子质量为125。下列关于这种原子的说法中,错误的是( )A.中子数为72 B.质子数为72 C.电子数为53 D.质子数和中子数之和为1255.用其质量的1/12作为相对原子质量的标准的碳原子 相对原子的质量是( ) A.12g B.12 C.1/12g D.1/12
7.有一种放射性碘(I)原子,常用作核反应堆的燃料棒,其质子数为53,中子数为78。该碘原子的相对原子质量为( ) A.53 B.78C.127D.131
6、北斗三号使用了钛合金材料,钛原子的质子数为22,相对原子质量为48,钛原子的核外电子数为( ) A.22 B.48 C.70 D.26
8、已知在某原子中共有的粒子数为 40,其中不带电的粒子数为 14,则该原子的相对原子质量为( ) A.54 B.13 C.27 D.26
通过本节课的学习,同学们谈谈有哪些收获?
1.完成配套练习册;2.预习 核外电子的排布及离子;3.书面作业:课后习题10、11。














