






还剩31页未读,
继续阅读
所属成套资源:2023-2024学年九年级上册化学(课件+练习)沪教版
成套系列资料,整套一键下载
第3章 物质构成的奥秘(复习课件)-2023-2024学年九年级化学上册(沪教版)
展开
这是一份第3章 物质构成的奥秘(复习课件)-2023-2024学年九年级化学上册(沪教版),共39页。
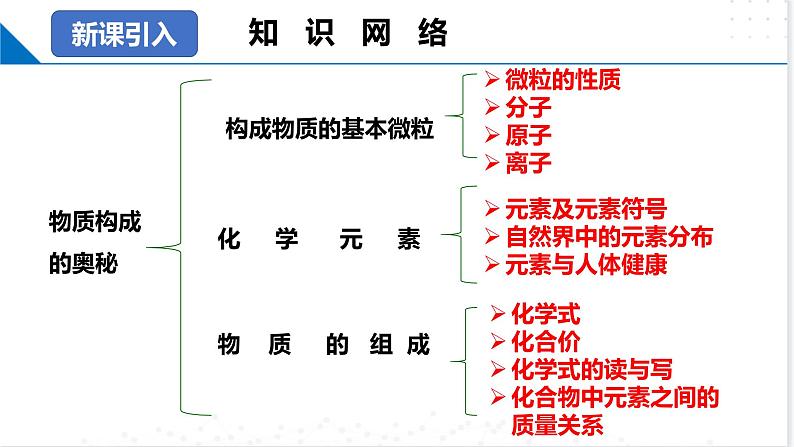
(复习课件) 第3章 物质构成的奥秘 目录CONTENTS 一 二 构成物质的基本微粒组成物质的化学元素 三 五 物质的组成物质构成的奥秘构成物质的基本微粒微粒的性质分子原子离子元素及元素符号自然界中的元素分布元素与人体健康化 学 元 素化学式化合价化学式的读与写化合物中元素之间的质量关系物 质 的 组 成新课引入知 识 网 络性质“小”——微粒的体积和_______都很小“动”——微粒总是在___________“间”——微粒之间都有一定的________“同”——同种物质分子的化学性质_______,不同种物质分子的化学性质不同应用区别物理变化和化学变化:从微观角度来分析,对于由分子构成的物质,当发生______(填“物理”或“化学”,下同)变化时,物质的分子本身没有发生变化,当发生_____变化时,原物质的分子发生了变化,生成了新物质的分子质量不断地运动空隙相同物理化学新课讲解构成物质的基本微粒解释常见现象:根据分子在 中,可解释物质的扩散(如气体的扩散、液体的蒸发、固体的溶解等);根据分子之间有______可解释热胀冷缩,气体易被压缩等现象不断地运动空隙新课讲解构成物质的基本微粒分子:保持物质(由分子构成)_________的最小微粒。由分子构成的物质有H2O、CO2等原子原子是________中的最小微粒。由原子构成的物质有Fe、Cu等金属和氦、氖等稀有气体原子结构构成原子核_______(带正电)________(不带正电)核外电子(带负电,分层排布)等量关系:核电荷数=质子数=核外电子数原子结构示意图(以钠原子为例)意义:表示核外电子数排布化学性质化学变化质子中子电子层电子数原子核质子数 相对原子质量新课讲解构成物质的基本微粒构成原子的各粒子间的关系①构成原子的粒子有三种:_________________。但并不是所有的原子都是由这三种粒子构成的,如氢原子中只有一个质子和一个电子,没有中子。②原子核内质子所带电荷与核外电子的电荷数____,电性________,所以原子___________。③原子核所带电荷数叫做核电荷数。核电荷数=_________=______________质子、中子、电子相等相反不显电性质子数核外电子数新课讲解构成物质的基本微粒相对原子质量定义:以一种碳原子的质量的 作为基准,其他原子的质量与这一基准的比表达式:某原子的相对原子质量=近似计算式:相对原子质量≈____________+中子数单位:相对原子质量单位为“1”,通常省略不写注意:相对分子质量(Mr)等于构成分子的各原子的相对原子质量(Ar)的总和质子数 新课讲解构成物质的基本微粒 阳离子:原子在______电子带_________的离子,如Na+、K+等 阴离子:原子在______电子带_________的离子,如Cl-、SO42-等 注意:阳离子不一定都是金属离子,如H+、NH4+等离子分类表示方法:失去失去正电荷得到负电荷意义:每个镁离子带两个单位的正电荷2个镁离子定义:在化学变化在,电中性的原子因得到或_______电子而成为带电荷的微粒新课讲解构成物质的基本微粒元素与物质、微观粒子的关系原子元素质子数相同的一类原子金刚石、汞等分 子氧气、氢气等离 子氯化钠等结合结合分解聚集得失电子结合新课讲解构成物质的基本微粒分子、原子、离子之间的联系新课讲解构成物质的基本微粒 金属元素:“ ”(汞除外),最外层电子数<4(H、He、B除外), 易____电子 非金属元素:“ ”、“ ”、“气”字旁,最外层电子数>4,易______电子, 稀有气体元素最外层有8个电子(He)有两个,相对稳定元素与元素符号分类元素元素符号书写原则:元素符号用1个或2个拉丁字母表示,第一个字母_____,第二个字 母____宏观:表示一种元素(如H:宏观表示_______),若物质的化学式与元 素符号相同时,则还表示这种物质微观:表示这种元素的一个原子(如H:微观表示__________),元素符 号前面加上化学计量数,该符号只具有微观意义 (如2H:表示__________)意义核电荷数失去得到大写小写氢元素 1个氢原子2个氢原子定义:具有相同的________(即质子数)的同一类原子总称新课讲解组成物质的化学元素元素周期表最早由俄国科学家门捷列夫编制的横行(周期):每一个横行叫周期,共有七个周期纵行(族):每一个纵行叫一个族,共有18个纵行16个族,其中8、9、10 三个纵行共同组成一个族元素周期表中元素信息: (以氮元素为例)元素周期表原子序数元素符号元素与元素符号新课讲解组成物质的化学元素自然界中元素的存在地壳:含量居于前四位的依次是_________________,其中含量最多的金属元 素是_____,含量最多的非金属元素是_______氧、硅、铝、铁铝氧氧氧太阳:含量最多的是氢,其次是氦,还含有碳、氮、氧和多种金属元素人体:含量最多的是_______,其次是碳、氢、氮海水:含量最多的是_______,其次是氢新课讲解组成物质的化学元素元素分类常量元素:碳(C)、氢(H)、氮(N)、钙(Ga)等微量元素:铁(Fe)、铜(Cu)、锰(Mn)、锌(Zn)、钴(Co)、碘(I)、硒(Se)等一些元素对人体健康的影响钙:主要存在于骨骼、牙齿中,缺钙有可能导致________、畸形,易得佝偻 病,主要食物来源:高钙奶、钙片、虾皮等铁:血红蛋白的主要成分,能帮助运输氧气,缺铁易得________ 主要食物来源:动物肝脏、瘦肉、蛋、鱼等锌:影响人体发育,缺锌会使儿童发育停滞,智力低下,严重时会得_______ 主要食物来源:动物肝脏、瘦肉、蛋、鱼等碘:甲状腺激素的重要成分,缺碘或碘过量均会导致___________ 主要食物来源:海产品、加碘盐等硒:微量的硒可以防晒,过量的硒则是致癌的因素之一 主要食物来源:富硒大米、富硒茶叶等氟:预防______ 主要食物来源:茶叶、海虾等骨质疏松贫血症侏儒症甲状腺疾病龋齿元素与人体健康新课讲解组成物质的化学元素混合物:由两种或两种以上物质混合而成的物质,如石油、食醋等纯净物定义:由__________组成的纯净物单质金属单质:如铜、铁等非金属单质(包括稀有气体单质),如氮气、氧气、氩气等按性质分化合物定义:由____________________组成的纯净物无机化合物氧化物:由______种元素组成,其中有一种元素是 氧的化合物,如H2O、Fe3O4等酸:解离时产生的阳离子全为H+的化合物,如硫酸、 盐酸等碱:解离时产生的阴离子全部为OH—的化合物,如 氢氧化钠、氢氧化钙等盐:解离时生成金属离子(或铵根离子)和酸根离子 的化合物,如氯化钠、硫酸钠等同种元素两种或两种以上元素两(或2)混合分离有机化合物:含碳元素的化合物(CO、CO2、碳酸、碳酸 盐等少数含碳化合物除外),如甲烷、乙醇等分类 ————新课讲解组成物质的化学元素定义:用___________和数字组合表示纯净物组成的式子意义宏观表示一种物质,如CH4表示_________________表示这种物质的元素组成,如CH4表示甲烷由_________________组成表示该物质的一个分子,如CH4表示_______________________表示物质的分子构成,如CH4表示____________________________________________ ________稀有气体、金属和固态非金属:用组成元素的元素符号表示(碘除外),如氖写为 Ne、铁写为Fe气态非金属:用元素符号和数字的组合表示,如氧气写为O2单质化合物:通常为正左负右,标价交叉,化简复查,如书写元素符号甲烷这种物质碳元素和氢元素一个甲烷分子一个甲烷分子由一个碳原子和四个氢原子构成(合理即可) 微观新课讲解物质的组成注意事项表示方法:在元素符号或原子团的正上方用符号和数字表示,如 等a.符号在前,数字在后b.表示某物质中某元素化合价时,需将整个化学式写出再标该元素的化合价常见元素及原子团的化合价常见元素的化合价记忆口诀:一价钾钠氯氢银,二价氧钙钡镁锌,三氯四硅五价磷, 二三铁,二四碳,二四六硫都齐全,铜汞二价最常见, 单质为零永不变(带点显负价)..常见原子团的化合价原子团化合价的数值等于所带电荷数-1-2新课讲解物质的组成一般规律a.在单质种,任何元素的化合价均为_________b.在金属化合物种,金属元素一般呈____价,非金属元素一般呈_____价,在非金属氧化物种,该非金属元素一般呈______价c.在化合物中各元素正负化合价代数和为_______d.在不同的物质中同种元素化合价可能不同计算计算原则:化合物中各元素正负化合价的代数和为______计算步骤(以Na2FeO4为例)零正负正零零新课讲解物质的组成化学式的相关计算新课讲解物质的组成典例精讲例1(2023年山东省威海市中考化学真题)下列关于分子、原子、离子的认识不正确的是( )A.在化学变化中,分子可以被创造也可以被消灭B.原子得失电子变成离子后,质量几乎不变,化学性质差别很大C.同种原子通过不同方式结合成的分子化学性质不同D.同种分子排列方式不同则化学性质不同【答案】D典例精讲例2.(2022年云南省中考)幼儿及青少年缺钙会患佝偻病。因此,每日必须摄入足够量的钙。这里的“钙”指的是( )A.原子 B.分子 C.元素 D.单质答案:C典例精讲例3(2023年黑龙江省牡丹江市中考化学真题)下列物质由原子直接构成的是( )A.氯化钠 B.过氧化氢 C.汞 D.C60【答案】C典例精讲例4(2023年湖南省长沙市中考化学真题)2022 年诺贝尔化学奖授予三位科学家,他们研究功能分子,搭建出复杂的分子结构。下列关于分子的说法正确的是( )A.物质一定是由分子构成的 B.通常分子的质量和体积都很小C.水变成冰以后分子停止了运动 D.构成H2O和H2O2的分子相同【答案】B典例精讲例5.(2023年湖南省益阳市中考化学真题 )小明的湿衣服在阳光下晒干了。下列用分子的观点解释这一变化错误的是( )A.水分子的质量变小了 B.水分子的间隔变大了C.水分子在不断运动 D.温度越高,水分子运动越快【答案】A典例精讲例6.(2023年北京市中考化学真题 )我国近代化学先驱徐寿创造了部分元素的汉语名称。下列元素名称与符号不一致的是( )A.钠(Na) B.钙(Ca) C.镁(Zn) D.锰(Mn)【答案】C-典例精讲例7.(2023年湖北恩施州中考化学真题)嫦娥五号带回的月壤中含有大量安全无污染的核聚变原料He-3如图所示。下列关于He-3的说法正确的是( )A.He-3是一种新元素B.He-3原子中含有1个质子,2个电子C.He-3原子中含有3个质子,没有中子D.H-3原子中含有2个质子,1个中子,2个电子【答案】D典例精讲例8.(2023年黑龙江省牡丹江市中考化学真题)如图是氟元素在元素周期表中的信息及原子结构示意图,下列表述错误的是( )A.氟属于非金属元素 B.氟原子核内有9个质子C.化学反应中氟原子易得电子 D.氟的相对原子质量为19.00g【答案】D典例精讲例9.(2023年湖北省鄂州市中考化学真题)铷是一种重要的化学元素,可应用于原子钟、卫星导航、计算机通信等。铷原子的结构示意图及其在元素周期表中的信息如图所示。下列说法正确的是( )A.铷原子在化学反应中易得到电子B.铷原子的中子数是37C.铷的相对原子质量是85.47gD.铷位于元素周期表第5周期【答案】D典例精讲例10.(2023年山东省烟台市中考化学真题)某种花青素(化学式C15H11O6)是天然的阳光遮盖物,能够阻挡紫外线。下列关于该花青素的说法正确的是( )A.花青素属于氧化物B.花青素由碳、氢、氧三种元素组成C.花青素由32个原子构成D.花青素中氧元素的质量分数最小【答案】B典例精讲例11.(2023年四川省凉山州中考化学真题)陈年老酒中的乙醇(C2H5OH)与乙酸(CH3COOH)反应生成具有果香味的乙酸乙酯(CH3COOC2H5),所以陈年老酒具有特殊的香味。下列说法错误的是( )A.闻到香味是分子在不断运动B.乙酸、乙醇、乙酸乙酯均属于有机物C.大量使用乙醇作燃料不利于推行碳达峰、碳中和D.乙酸乙酯由4个碳原子、8个氢原子和2个氧原子构成【答案】D典例精讲例12(2023年辽宁省抚顺市、本溪市、辽阳市中考化学真题)“赠人玫瑰,手留余香”。玫瑰花中含有的香茅醇(化学式为C10H20O)具有芳香的气味。请计算。(1)香茅醇的相对分子质量是 。(2)香茅醇中碳、氢、氧三种元素的质量比为 (填最简整数比)。【答案】(1)156;(2)30:5:41.(2023四川省成都市青白江中学校二模)下列关于分子的叙述中,正确的是( )A.一切物质都是由分子构成的B.分子是化学变化中的最小粒子C.分子是不能再分的一种粒子D.分子是保持物质化学性质的最小粒子答案:D达标检测2.(2023成都市通锦中学校二模)用分子的知识解释下列现象,正确的是( )A.缉毒犬能根据气味发现毒品,是由于分子不断运动B.铁丝在空气中不燃烧而在氧气中燃烧,说明空气中和氧气中的氧分子化学性质不同C.变瘪的乒乓球放入热水中能鼓起来,是由于分子受热体积变大D.降温能使水结成冰,是因为在低温下水分子静止不动答案:A达标检测3.(2023崇州市崇庆中学实验学校二模 ) 下列对分子、原子、离子的认识正确的是( )A.同种分子排列方式不同,化学性质不同B.在干冰中,分子因相互作用而静止不动C.同种原子按不同方式结合,可以构成不同的物质D.原子得失电子形成离子后,原子核发生了变化答案:C达标检测4.(2023河南周口二模)在下列示意图表示的粒子中,属于原子的有 (填序号,下同),属于阳离子的有 ,属于阴离子的有 ,属于同种元素的为 。②⑤⑥①④③④⑤达标检测5.(2023山东聊城二模)下列关于微观粒子说法不正确的是( )A.分子的质量一定比原子的质量大 B.同种原子可以构成不同种分子 C.所有原子都由原子核和核外电子构成 D.原子得到或失去电子变成离子答案:A达标检测1.完成配套练习册;2.完成导学案 。作业布置
(复习课件) 第3章 物质构成的奥秘 目录CONTENTS 一 二 构成物质的基本微粒组成物质的化学元素 三 五 物质的组成物质构成的奥秘构成物质的基本微粒微粒的性质分子原子离子元素及元素符号自然界中的元素分布元素与人体健康化 学 元 素化学式化合价化学式的读与写化合物中元素之间的质量关系物 质 的 组 成新课引入知 识 网 络性质“小”——微粒的体积和_______都很小“动”——微粒总是在___________“间”——微粒之间都有一定的________“同”——同种物质分子的化学性质_______,不同种物质分子的化学性质不同应用区别物理变化和化学变化:从微观角度来分析,对于由分子构成的物质,当发生______(填“物理”或“化学”,下同)变化时,物质的分子本身没有发生变化,当发生_____变化时,原物质的分子发生了变化,生成了新物质的分子质量不断地运动空隙相同物理化学新课讲解构成物质的基本微粒解释常见现象:根据分子在 中,可解释物质的扩散(如气体的扩散、液体的蒸发、固体的溶解等);根据分子之间有______可解释热胀冷缩,气体易被压缩等现象不断地运动空隙新课讲解构成物质的基本微粒分子:保持物质(由分子构成)_________的最小微粒。由分子构成的物质有H2O、CO2等原子原子是________中的最小微粒。由原子构成的物质有Fe、Cu等金属和氦、氖等稀有气体原子结构构成原子核_______(带正电)________(不带正电)核外电子(带负电,分层排布)等量关系:核电荷数=质子数=核外电子数原子结构示意图(以钠原子为例)意义:表示核外电子数排布化学性质化学变化质子中子电子层电子数原子核质子数 相对原子质量新课讲解构成物质的基本微粒构成原子的各粒子间的关系①构成原子的粒子有三种:_________________。但并不是所有的原子都是由这三种粒子构成的,如氢原子中只有一个质子和一个电子,没有中子。②原子核内质子所带电荷与核外电子的电荷数____,电性________,所以原子___________。③原子核所带电荷数叫做核电荷数。核电荷数=_________=______________质子、中子、电子相等相反不显电性质子数核外电子数新课讲解构成物质的基本微粒相对原子质量定义:以一种碳原子的质量的 作为基准,其他原子的质量与这一基准的比表达式:某原子的相对原子质量=近似计算式:相对原子质量≈____________+中子数单位:相对原子质量单位为“1”,通常省略不写注意:相对分子质量(Mr)等于构成分子的各原子的相对原子质量(Ar)的总和质子数 新课讲解构成物质的基本微粒 阳离子:原子在______电子带_________的离子,如Na+、K+等 阴离子:原子在______电子带_________的离子,如Cl-、SO42-等 注意:阳离子不一定都是金属离子,如H+、NH4+等离子分类表示方法:失去失去正电荷得到负电荷意义:每个镁离子带两个单位的正电荷2个镁离子定义:在化学变化在,电中性的原子因得到或_______电子而成为带电荷的微粒新课讲解构成物质的基本微粒元素与物质、微观粒子的关系原子元素质子数相同的一类原子金刚石、汞等分 子氧气、氢气等离 子氯化钠等结合结合分解聚集得失电子结合新课讲解构成物质的基本微粒分子、原子、离子之间的联系新课讲解构成物质的基本微粒 金属元素:“ ”(汞除外),最外层电子数<4(H、He、B除外), 易____电子 非金属元素:“ ”、“ ”、“气”字旁,最外层电子数>4,易______电子, 稀有气体元素最外层有8个电子(He)有两个,相对稳定元素与元素符号分类元素元素符号书写原则:元素符号用1个或2个拉丁字母表示,第一个字母_____,第二个字 母____宏观:表示一种元素(如H:宏观表示_______),若物质的化学式与元 素符号相同时,则还表示这种物质微观:表示这种元素的一个原子(如H:微观表示__________),元素符 号前面加上化学计量数,该符号只具有微观意义 (如2H:表示__________)意义核电荷数失去得到大写小写氢元素 1个氢原子2个氢原子定义:具有相同的________(即质子数)的同一类原子总称新课讲解组成物质的化学元素元素周期表最早由俄国科学家门捷列夫编制的横行(周期):每一个横行叫周期,共有七个周期纵行(族):每一个纵行叫一个族,共有18个纵行16个族,其中8、9、10 三个纵行共同组成一个族元素周期表中元素信息: (以氮元素为例)元素周期表原子序数元素符号元素与元素符号新课讲解组成物质的化学元素自然界中元素的存在地壳:含量居于前四位的依次是_________________,其中含量最多的金属元 素是_____,含量最多的非金属元素是_______氧、硅、铝、铁铝氧氧氧太阳:含量最多的是氢,其次是氦,还含有碳、氮、氧和多种金属元素人体:含量最多的是_______,其次是碳、氢、氮海水:含量最多的是_______,其次是氢新课讲解组成物质的化学元素元素分类常量元素:碳(C)、氢(H)、氮(N)、钙(Ga)等微量元素:铁(Fe)、铜(Cu)、锰(Mn)、锌(Zn)、钴(Co)、碘(I)、硒(Se)等一些元素对人体健康的影响钙:主要存在于骨骼、牙齿中,缺钙有可能导致________、畸形,易得佝偻 病,主要食物来源:高钙奶、钙片、虾皮等铁:血红蛋白的主要成分,能帮助运输氧气,缺铁易得________ 主要食物来源:动物肝脏、瘦肉、蛋、鱼等锌:影响人体发育,缺锌会使儿童发育停滞,智力低下,严重时会得_______ 主要食物来源:动物肝脏、瘦肉、蛋、鱼等碘:甲状腺激素的重要成分,缺碘或碘过量均会导致___________ 主要食物来源:海产品、加碘盐等硒:微量的硒可以防晒,过量的硒则是致癌的因素之一 主要食物来源:富硒大米、富硒茶叶等氟:预防______ 主要食物来源:茶叶、海虾等骨质疏松贫血症侏儒症甲状腺疾病龋齿元素与人体健康新课讲解组成物质的化学元素混合物:由两种或两种以上物质混合而成的物质,如石油、食醋等纯净物定义:由__________组成的纯净物单质金属单质:如铜、铁等非金属单质(包括稀有气体单质),如氮气、氧气、氩气等按性质分化合物定义:由____________________组成的纯净物无机化合物氧化物:由______种元素组成,其中有一种元素是 氧的化合物,如H2O、Fe3O4等酸:解离时产生的阳离子全为H+的化合物,如硫酸、 盐酸等碱:解离时产生的阴离子全部为OH—的化合物,如 氢氧化钠、氢氧化钙等盐:解离时生成金属离子(或铵根离子)和酸根离子 的化合物,如氯化钠、硫酸钠等同种元素两种或两种以上元素两(或2)混合分离有机化合物:含碳元素的化合物(CO、CO2、碳酸、碳酸 盐等少数含碳化合物除外),如甲烷、乙醇等分类 ————新课讲解组成物质的化学元素定义:用___________和数字组合表示纯净物组成的式子意义宏观表示一种物质,如CH4表示_________________表示这种物质的元素组成,如CH4表示甲烷由_________________组成表示该物质的一个分子,如CH4表示_______________________表示物质的分子构成,如CH4表示____________________________________________ ________稀有气体、金属和固态非金属:用组成元素的元素符号表示(碘除外),如氖写为 Ne、铁写为Fe气态非金属:用元素符号和数字的组合表示,如氧气写为O2单质化合物:通常为正左负右,标价交叉,化简复查,如书写元素符号甲烷这种物质碳元素和氢元素一个甲烷分子一个甲烷分子由一个碳原子和四个氢原子构成(合理即可) 微观新课讲解物质的组成注意事项表示方法:在元素符号或原子团的正上方用符号和数字表示,如 等a.符号在前,数字在后b.表示某物质中某元素化合价时,需将整个化学式写出再标该元素的化合价常见元素及原子团的化合价常见元素的化合价记忆口诀:一价钾钠氯氢银,二价氧钙钡镁锌,三氯四硅五价磷, 二三铁,二四碳,二四六硫都齐全,铜汞二价最常见, 单质为零永不变(带点显负价)..常见原子团的化合价原子团化合价的数值等于所带电荷数-1-2新课讲解物质的组成一般规律a.在单质种,任何元素的化合价均为_________b.在金属化合物种,金属元素一般呈____价,非金属元素一般呈_____价,在非金属氧化物种,该非金属元素一般呈______价c.在化合物中各元素正负化合价代数和为_______d.在不同的物质中同种元素化合价可能不同计算计算原则:化合物中各元素正负化合价的代数和为______计算步骤(以Na2FeO4为例)零正负正零零新课讲解物质的组成化学式的相关计算新课讲解物质的组成典例精讲例1(2023年山东省威海市中考化学真题)下列关于分子、原子、离子的认识不正确的是( )A.在化学变化中,分子可以被创造也可以被消灭B.原子得失电子变成离子后,质量几乎不变,化学性质差别很大C.同种原子通过不同方式结合成的分子化学性质不同D.同种分子排列方式不同则化学性质不同【答案】D典例精讲例2.(2022年云南省中考)幼儿及青少年缺钙会患佝偻病。因此,每日必须摄入足够量的钙。这里的“钙”指的是( )A.原子 B.分子 C.元素 D.单质答案:C典例精讲例3(2023年黑龙江省牡丹江市中考化学真题)下列物质由原子直接构成的是( )A.氯化钠 B.过氧化氢 C.汞 D.C60【答案】C典例精讲例4(2023年湖南省长沙市中考化学真题)2022 年诺贝尔化学奖授予三位科学家,他们研究功能分子,搭建出复杂的分子结构。下列关于分子的说法正确的是( )A.物质一定是由分子构成的 B.通常分子的质量和体积都很小C.水变成冰以后分子停止了运动 D.构成H2O和H2O2的分子相同【答案】B典例精讲例5.(2023年湖南省益阳市中考化学真题 )小明的湿衣服在阳光下晒干了。下列用分子的观点解释这一变化错误的是( )A.水分子的质量变小了 B.水分子的间隔变大了C.水分子在不断运动 D.温度越高,水分子运动越快【答案】A典例精讲例6.(2023年北京市中考化学真题 )我国近代化学先驱徐寿创造了部分元素的汉语名称。下列元素名称与符号不一致的是( )A.钠(Na) B.钙(Ca) C.镁(Zn) D.锰(Mn)【答案】C-典例精讲例7.(2023年湖北恩施州中考化学真题)嫦娥五号带回的月壤中含有大量安全无污染的核聚变原料He-3如图所示。下列关于He-3的说法正确的是( )A.He-3是一种新元素B.He-3原子中含有1个质子,2个电子C.He-3原子中含有3个质子,没有中子D.H-3原子中含有2个质子,1个中子,2个电子【答案】D典例精讲例8.(2023年黑龙江省牡丹江市中考化学真题)如图是氟元素在元素周期表中的信息及原子结构示意图,下列表述错误的是( )A.氟属于非金属元素 B.氟原子核内有9个质子C.化学反应中氟原子易得电子 D.氟的相对原子质量为19.00g【答案】D典例精讲例9.(2023年湖北省鄂州市中考化学真题)铷是一种重要的化学元素,可应用于原子钟、卫星导航、计算机通信等。铷原子的结构示意图及其在元素周期表中的信息如图所示。下列说法正确的是( )A.铷原子在化学反应中易得到电子B.铷原子的中子数是37C.铷的相对原子质量是85.47gD.铷位于元素周期表第5周期【答案】D典例精讲例10.(2023年山东省烟台市中考化学真题)某种花青素(化学式C15H11O6)是天然的阳光遮盖物,能够阻挡紫外线。下列关于该花青素的说法正确的是( )A.花青素属于氧化物B.花青素由碳、氢、氧三种元素组成C.花青素由32个原子构成D.花青素中氧元素的质量分数最小【答案】B典例精讲例11.(2023年四川省凉山州中考化学真题)陈年老酒中的乙醇(C2H5OH)与乙酸(CH3COOH)反应生成具有果香味的乙酸乙酯(CH3COOC2H5),所以陈年老酒具有特殊的香味。下列说法错误的是( )A.闻到香味是分子在不断运动B.乙酸、乙醇、乙酸乙酯均属于有机物C.大量使用乙醇作燃料不利于推行碳达峰、碳中和D.乙酸乙酯由4个碳原子、8个氢原子和2个氧原子构成【答案】D典例精讲例12(2023年辽宁省抚顺市、本溪市、辽阳市中考化学真题)“赠人玫瑰,手留余香”。玫瑰花中含有的香茅醇(化学式为C10H20O)具有芳香的气味。请计算。(1)香茅醇的相对分子质量是 。(2)香茅醇中碳、氢、氧三种元素的质量比为 (填最简整数比)。【答案】(1)156;(2)30:5:41.(2023四川省成都市青白江中学校二模)下列关于分子的叙述中,正确的是( )A.一切物质都是由分子构成的B.分子是化学变化中的最小粒子C.分子是不能再分的一种粒子D.分子是保持物质化学性质的最小粒子答案:D达标检测2.(2023成都市通锦中学校二模)用分子的知识解释下列现象,正确的是( )A.缉毒犬能根据气味发现毒品,是由于分子不断运动B.铁丝在空气中不燃烧而在氧气中燃烧,说明空气中和氧气中的氧分子化学性质不同C.变瘪的乒乓球放入热水中能鼓起来,是由于分子受热体积变大D.降温能使水结成冰,是因为在低温下水分子静止不动答案:A达标检测3.(2023崇州市崇庆中学实验学校二模 ) 下列对分子、原子、离子的认识正确的是( )A.同种分子排列方式不同,化学性质不同B.在干冰中,分子因相互作用而静止不动C.同种原子按不同方式结合,可以构成不同的物质D.原子得失电子形成离子后,原子核发生了变化答案:C达标检测4.(2023河南周口二模)在下列示意图表示的粒子中,属于原子的有 (填序号,下同),属于阳离子的有 ,属于阴离子的有 ,属于同种元素的为 。②⑤⑥①④③④⑤达标检测5.(2023山东聊城二模)下列关于微观粒子说法不正确的是( )A.分子的质量一定比原子的质量大 B.同种原子可以构成不同种分子 C.所有原子都由原子核和核外电子构成 D.原子得到或失去电子变成离子答案:A达标检测1.完成配套练习册;2.完成导学案 。作业布置
相关资料
更多









