

2024遂宁射洪中学高一下学期期末模拟化学试题含答案
展开(满分:100 分 时间:75分钟)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后, 再选涂其它答案标号。回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
3.考试结束后,请将答题卡交回。
可能用到的原子量:H-1 C-12 O-16 Mg-24 Al-27 S-32 Cl-35.5 Fe-56
第I卷 (选择题)
一、选择题(本大题共15个小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)
1.文房四宝是中华传统文化的瑰宝。下列有关叙述错误的是( )
A.羊毛可用于制毛笔,主要成分是蛋白质
B.松木可用于制墨,墨的主要成分是单质碳
C.竹子可用于造纸,纸的主要成分是纤维素
D.“北斗系统”组网成功,北斗芯片中的半导体材料为二氧化硅
2.下列表示正确的是( )
A.羟基的电子式为
B.正丁烷的球棍模型
C.阿司匹林的分子式:
D.乙烯的结构简式:CH2CH2
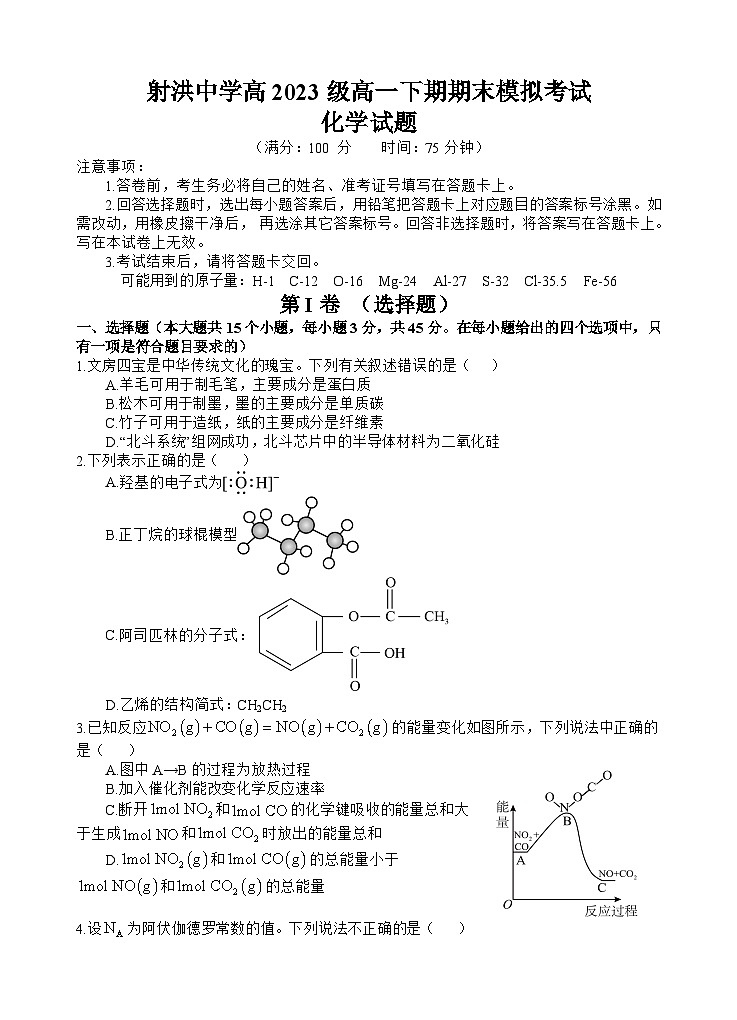
3.已知反应的能量变化如图所示,下列说法中正确的是( )
A.图中A→B的过程为放热过程
B.加入催化剂能改变化学反应速率
C.断开和的化学键吸收的能量总和大于生成和时放出的能量总和
D.和的总能量小于和的总能量
4.设为阿伏伽德罗常数的值。下列说法不正确的是( )
A.乙烯和丙烯的混合气体中含有原子的数目为
B.分子中含有的共价键数目为
C.标准状况下,中含有的碳原子数为0.1
D.由Cu、Zn和稀硫酸组成的原电池工作时,若生成,则电路通过电子
5.我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为。下列说法正确的是( )
A.该反应氧化产物为CO2B.该反应的还原剂为S
C.C被氧化,发生还原反应D.KNO3中的氮元素被氧化
6.下列关于乙醇的反应中,不涉及电子转移的是( )
A.乙醇与金属钠反应产生气体B.乙醇使酸性溶液变绿
C.乙醇使酸性溶液褪色D.乙醇与乙酸反应生成乙酸乙酯
7.用下列实验装置进行相应实验,能达到实验目的的是( )
A.用图1实现实验室制备B.用图2所示装置制取并收集乙酸乙酯
C.用图3进行氨气的尾气处理D.用图4所示装置进行石油的蒸馏实验
8.下列实验操作和现象以及对应的结论正确的是( )
9.对于下列过程中发生的化学反应,相应离子方程式正确的是( )
A.试管壁上的银镜用稀硝酸清洗:
B.向溶液中滴加氨水制备
C.海水提溴过程中将溴吹入吸收塔:
D.用三氯化铁溶液刻制覆铜电路板:
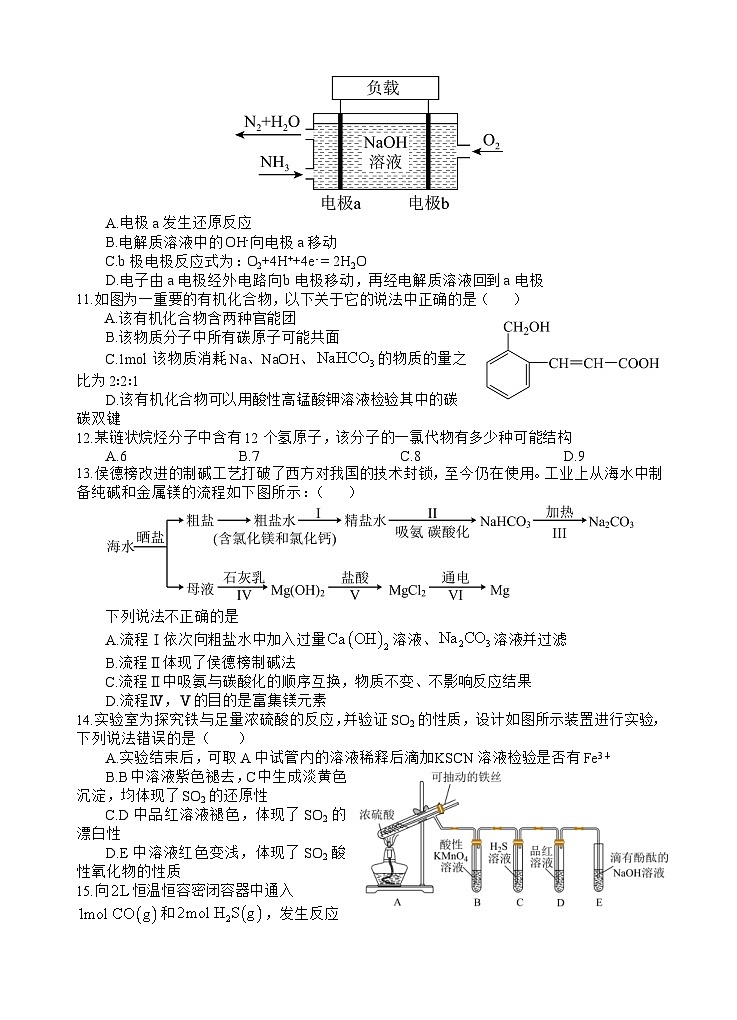
10.潜艇中使用的液氨一液氧燃料电池工作原理如图所示,下列说法正确的是( )
A.电极a发生还原反应
B.电解质溶液中的OH-向电极a移动
C.b极电极反应式为:O2+4H++4e- = 2H2O
D.电子由a电极经外电路向b电极移动,再经电解质溶液回到a电极
11.如图为一重要的有机化合物,以下关于它的说法中正确的是( )
A.该有机化合物含两种官能团
B.该物质分子中所有碳原子可能共面
C.1ml该物质消耗Na、NaOH、的物质的量之比为2∶2∶1
D.该有机化合物可以用酸性高锰酸钾溶液检验其中的碳碳双键
12.某链状烷烃分子中含有12个氢原子,该分子的一氯代物有多少种可能结构
A.6B.7C.8D.9
13.侯德榜改进的制碱工艺打破了西方对我国的技术封锁,至今仍在使用。工业上从海水中制备纯碱和金属镁的流程如下图所示:( )
下列说法不正确的是
A.流程Ⅰ依次向粗盐水中加入过量溶液、溶液并过滤
B.流程Ⅱ体现了侯德榜制碱法
C.流程Ⅱ中吸氨与碳酸化的顺序互换,物质不变、不影响反应结果
D.流程Ⅳ,Ⅴ的目的是富集镁元素
14.实验室为探究铁与足量浓硫酸的反应,并验证SO2的性质,设计如图所示装置进行实验,下列说法错误的是( )
A.实验结束后,可取A中试管内的溶液稀释后滴加KSCN溶液检验是否有Fe3+
B.B中溶液紫色褪去,C中生成淡黄色沉淀,均体现了SO2的还原性
C.D中品红溶液褪色,体现了SO2的漂白性
D.E中溶液红色变浅,体现了SO2酸性氧化物的性质
15.向恒温恒容密闭容器中通入和,发生反应,反应达到平衡状态,测得平衡时体积分数为20%。下列说法正确的是( )
A.CO和的平衡转化率均为60%
B.
C.混合气体的平均相对分子质量始终保持不变
D.若保持不变,可判断该反应已达到平衡状态
第II卷 非选择题
16.(12分)利用催化氧化反应将SO2转化为SO3是工业上生产硫酸的关键步骤,发生反应2SO2(g)+O2(g)2SO3(g)。回答下列问题:
(1)反应过程的能量变化如图所示,则该反应为 (填“放热”或“吸热”)反应。
(2)恒温恒容时,下列措施能使该反应速率增大的是 (填字母,下同)。
a.增加O2的浓度 b.选择高效催化剂
c.充入氦气 d.适当降低温度
(3)下列情况能说明该反应达到化学平衡状态的是 。
a.2v正(O2)=v逆(SO2) b.恒温恒容时,混合气体的密度不再随时间变化
c.SO3的物质的量不再变化 d.SO2、O2、SO3三者的浓度之比为2∶1∶2
(4)某次实验中,在容积为2 L的恒温密闭容器中通入10 ml SO2和a ml O2,反应过程中部分物质的物质的量随反应时间的变化如图所示。
①2 min时,v正(SO2) v逆(SO2)。(填“>”“<”或“=”)
②用SO3的浓度变化表示0~5 min内反应的平均速率是 ml·L-1·min-1。
③反应达到平衡时,O2的转化率为50%,则a=
17.(14分)如图为以淀粉为主要原料合成一种具有果香味的酯类物质的过程:
请回答下列问题:
(1)葡萄糖的分子式为 ,B分子中的官能团名称为 。
(2)反应⑦的化学方程式为 ,反应类型 。
(3)反应 = 5 \* GB3 \* MERGEFORMAT ⑤的化学方程式为 。
(4)为了检验反应①进行程度,需要的试剂有 。
a.新制的 b.碘水 c.NaOH溶液 d.溶液
(5)乙酸乙酯的某种同分异构体分子中含有2个甲基,且能与碳酸氢钠溶液反应,则该物质的结构简式为 。
18.(15分)为了探究Cl2、SO2同时通入H2O中发生的反应,某校化学兴趣小组同学设计了如图所示的实验装置。
(1)该化学兴趣小组的同学制取Cl2、SO2气体,现采用Na2SO3与70%的硫酸为原料制取SO2,采用MnO2和浓盐酸(12ml•L﹣1)为原料制取Cl2。在此试验中,F仪器的作用是___________;发生装置B应选择以下三种装置中的___________(选填序号)。
(2)B装置中主要反应的离子方程式为_________________________________。
(3)为验证通入D装置中的气体是Cl2过量还是SO2过量,兴趣小组的同学准备了以下试剂:
a.氯化铁溶液 b.氯化亚铁溶液 c.硫氰化钾溶液
d.氯化钡溶液 e.品红溶液 f.酸性高锰酸钾溶液
①若SO2过量,取适量D中溶液滴加至盛有___________(选填一个字母序号)试剂的试管内,发生的现象是___________________。
②若Cl2过量,取适量D中溶液滴加至盛有___________(选填一个字母)试剂的试管内,再加入___________(选填一个字母)试剂,发生的现象是溶液呈血红色,此现象的化学方程式为___________________。
19.(14分)工业上用铝土矿(含氧化铝、氧化铁)制取铝的过程如下:
回答下列问题:
(1)沉淀C的化学式为 ,该物质除了用于金属冶炼以外,还可用作颜料。
(2)电解熔融的氧化铝时,标准状况下若得到22.4 L O2,则同时生成 g铝。
(3)操作Ⅰ、操作Ⅱ和操作Ⅲ都是 (填操作名称),实验室要洗涤Al(OH)3沉淀的方法是
(4)生产过程中,除CaO和CO2可以循环利用外,还可以循环利用的物质有 (填化学式)
(5)写出Na2CO3溶液与CaO反应的离子方程式:
(6)CO2不能用稀硫酸或稀盐酸代替的原因是 操作和现象
结论
A
向汽油和地沟油中分别加入足量的NaOH溶液并加热,现象不同
可鉴别出地沟油
B
分别向鸡蛋清水溶液中加入饱和硫酸铵溶液和硫酸铜溶液,均产生沉淀
蛋白质遇盐变性
C
将混有乙烯的乙烷气体通入少量酸性溶液,溶液紫红色褪去
可提纯乙烷气体
D
向蔗糖溶液中加入稀硫酸,水浴加热一段时间,再加入新制悬浊液,用酒精灯加热,未见砖红色沉淀
蔗糖未水解
2024遂宁射洪中学高二下学期期末模拟化学试题含答案: 这是一份2024遂宁射洪中学高二下学期期末模拟化学试题含答案,文件包含化学试题docx、化学试题答案docx等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。
2024遂宁射洪中学高一下学期期中考试化学含答案: 这是一份2024遂宁射洪中学高一下学期期中考试化学含答案,文件包含化学试题doc、化学答案doc等2份试卷配套教学资源,其中试卷共11页, 欢迎下载使用。
2024遂宁射洪中学高一下学期4月月考试题化学含答案: 这是一份2024遂宁射洪中学高一下学期4月月考试题化学含答案,文件包含化学试题docx、化学答案doc等2份试卷配套教学资源,其中试卷共9页, 欢迎下载使用。












