





所属成套资源:(2024)新人教版化学九年级上册全册PPT课件+上课资料
人教版(2024)九年级上册课题2 化学方程式教课内容ppt课件
展开
这是一份人教版(2024)九年级上册课题2 化学方程式教课内容ppt课件,共35页。PPT课件主要包含了学习目标,课堂导入,化学反应中的定量关系,微粒个数比,物质质量比,20kg,实际质量,新知探究,实际质量比,找质量比等内容,欢迎下载使用。
1.知道根据化学方程式计算的依据,掌握化学方程式中的比例关系;2.能根据化学方程式进行简单的计算,并解决生产生活中的简单问题;3.学习利用质量关系、比例关系定量认识化学反应,认识定量研究对化学科学发展的重大作用。
若火箭燃料是液氢,助燃剂是液氧,写出火箭点火时会发生反应的化学方程式。
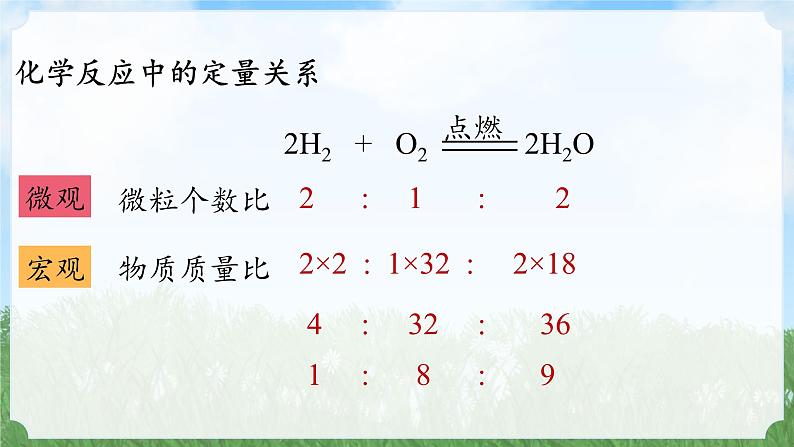
2 : 1 : 2
2×2 : 1×32 : 2×18
4 : 32 : 36
1 : 8 : 9
交流讨论:如果火箭推进器确定升空的火箭需要液氢20kg时,则火箭助燃剂仓中应填充多少千克的液氧使这些液氢完全燃烧?
在化学方程式中,各物质是质量比是一个定值
知识点1 根据化学方程式进行简单计算
利用化学方程式计算的依据:
(1)理论依据:质量守恒定律。(2)基本依据:化学方程式中各反应物、生成物之间的质量比。
=各物质的相对分子质量(或相对原子质量)与其化学式前化学计量数的乘积之比
化学方程式中的比例关系
碳在空气中燃烧的反应中,反应物与生成物之间的质量比可表示为:
C + O2 CO2
12 ︰ 16×2 ︰ 12+16×2
12 ︰ 32 ︰ 44
若: 12克 ︰ 32克 ︰ ( )克
若: 6克 ︰ ( )克 ︰ 22 克
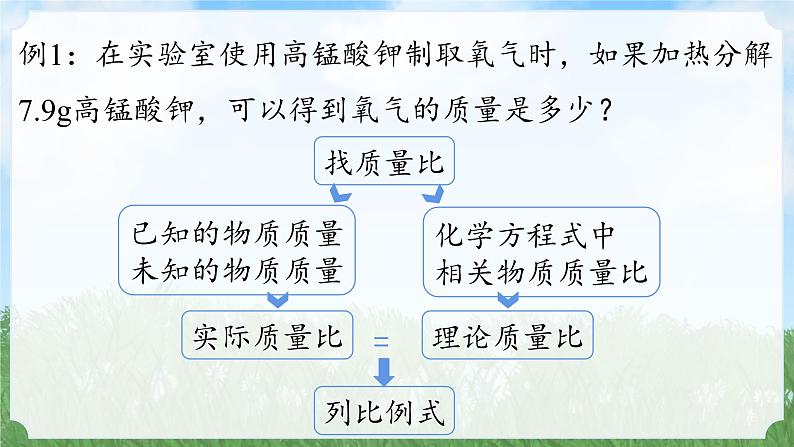
例1:在实验室使用高锰酸钾制取氧气时,如果加热分解7.9g高锰酸钾,可以得到氧气的质量是多少?
化学方程式中相关物质质量比
已知的物质质量未知的物质质量
2KMnO4 ══ K2MnO4 + MnO2 + O2
解:设可得氧气的质量为x。
2×158 1×32 7.9g x
答:可以得到0.8g氧气。
(1)设:根据题意设未知量;(2)写:正确书写化学方程式;(3)标:标出有关物质的量;(4)列:列出比例式,求解;(5)答:简明地写出答案。
利用化学方程式的简单计算
实验室做氧气的性质实验时需4kg氧气,若实验室以过氧化氢为原料制取氧气,需过氧化氢的质量是多少?
2H2O2 2H2O + O2
解:设生成4kg氧气需过氧化氢的质量为x。
答:需8.5kg的过氧化氢。
1.设未知量时一定要注意质量单位,已知量和未知量单位不一致的要先进行单位换算,单位必须一致才能计算。2.写方程式要注意配平,而且要注意化学方程式的完整,反应条件、气体和沉淀的符号要注意标明。
根据化学方程式计算需注意
3.相关物质的相对分子质量写在相应化学式的下面,一定要注意用相对分子质量乘以化学式前面的系数,已知量和未知量写在相应相对分子质量的下边。4.计算结果的小数位保留按题中要求进行,若题中没有要求,一般保留一位小数。
5.不纯物质质量需换算成纯物质的质量再代入计算 。6.计算时已知量若是气体体积,需换算成质量代入计算,气体的质量(g)=气体的体积(L)×气体的密度(g/L)。7.计算常用的关系式:
物质的纯度(质量分数)=
例2:工业上,煅烧石灰石(主要成分是CaCO3)产生的生石灰(CaO)和二氧化碳可分别用于生产建筑和化肥。制取5.6t氧化钙,需要碳酸钙的质量是多少?
答:需要碳酸钙的质量为10t。
x = =10t
CaCO3 CaO+ CO2↑
解:设需要碳酸钙的质量为x。
计算过程中常出现的错误:
1.未知量设的不对;2.化学方程式未配平;3.相对分子质量计算错误;4.比例关系不对;5.已知物质的质量和计算结果没写单位;6.计算结果不准确。
化学方程式计算的四种类型:
1.已知反应物的质量求生成物的质量;2.已知生成物的质量求反应物的质量;3.已知一种反应物的质量求另一种反应物的质量;4.已知一种生成物的质量求另一种生成物的质量。
例3:在反应2Mg+O2==2MgO中,镁、氧气、氧化镁的质量比为( )A.48:32:80 B.24:32:40C.24:32:64 D.24:32:80
1.常规型:已知反应物(或生成物)的质量,利用化学 方程式求生成物(或反应物)的质量。2.单位转换型:物质的体积、密度与质量间换算的有关 计算。3.利用质量守恒定律来寻找已知量型4.图表型
知识点2 利用化学方程式简单计算的类型
【例】实验室用加热KMnO4制取氧气,现加热15.8gKMnO4,充分反应后可以制得氧气多少克?
解:设加热15.8gKMnO4,充分反应后可制得氧气的质量为x。
答:加热15.8gKMnO4,充分反应后可以制得1.6g氧气。
解:11.2L氧气的质量为11.2L×1.43g/L≈16g
设生成氧化镁的质量为x。
答:生成氧化镁的质量为40g。
【例】足量的镁与标准状况下11.2L的氧气(氧气密度为1.43g/L)充分反应,生成氧化镁的质量为多少?
3.利用质量守恒定律来寻找已知量型
【例】久置的过氧化氢溶液,其中部分过氧化氢会分解生成氧气。某兴趣小组对实验室中一瓶久置的过氧化氢溶液(质量分数为30%)进行实验。测得相关数据如下:
过氧化氢溶液质量34.0g
(1)根据质量守恒定律,反应生成氧气的质量为 。(2)计算该过程中产生氧气需要过氧化氢的质量。
答:该过程中产生氧气需要过氧化氢的质量为1.7g。
解:设需要过氧化氢的质量为x。
【例1】实验室用加热KMnO4制取氧气,现用一定量KMnO4加热制取氧气,产生氧气的量与时间关系如图所示。(1)完全反应时,制得氧气的质量是多少?(2)有多少KMnO4发生了反应?
(2)解:设制得3.2g氧气,需加热KMnO4的质量为x。
答:有31.6g KMnO4发生了反应。
(1)由图可知,制得的氧气质量为3.2g。
【例2】实验室用加热KMnO4制取氧气,现将31.6g KMnO4放入大试管中进行加热,并在不同时刻测定试管内剩余固体的质量,质量变化如下表所示。
根据图表回答:(1)m的值是多少?(2)充分反应后得到氧气的质量为多少?(3)反应后得到MnO2的质量为多少?
(1)由表中数据可知,第5.0min时,剩余固体质量 不发生改变,则m的值为28.4。
(2)充分反应后得到氧气的质量为31.6g-28.4g=3.2g。
答:反应后得到 MnO2的质量为8.7g。
(3)解:设反应后得到 MnO2的质量为x。
1.设未知量2.写出反应的化学方程式3.找出相关量的质量关系4.列出比例式求解5.简明地写出答案
1.解题步骤必须规范完整2.化学方程式要配平3.带入量均指纯净物的质量4.计算过程单位要统一
1.在反应A+B C+2D中,已知2.9g的A与4.9g的B恰好完全反应生成6g的C,又知D的相对分子质量为18,则A的相对分子质量为( )
A.29 B.40 C.58 D.86
设A的相对分子质量为x。
解析:根据质量守恒定律可知,生成D的质量为2.9g+4.9g-6g=1.8g。
故A的相对分子质量为58。
2.氢气是理想的高能燃料,其燃烧产物对环境无污染。若充分燃烧8g氢气,在标准状况下,最少需要氧气的体积为多少?(标准状况下氧气的密度约为1.43g/L)
解:设需要氧气的质量为x。
氧气的体积为 ≈44.76L
答:最少需要氧气44.76L。
相关课件
这是一份初中化学人教版(2024)九年级上册课题2 化学方程式教学演示课件ppt,共17页。PPT课件主要包含了学习目标,课堂导入,新知探究,观察法,最小公倍数法,奇数配偶法,个O原子,设1法,分解反应,课堂小结等内容,欢迎下载使用。
这是一份人教版(2024)九年级上册课题2 化学方程式说课课件ppt,共25页。PPT课件主要包含了学习目标,课堂导入,质量守恒,文字表达式,微观示意图,符号表达式,信息少不便交流,书写不方便,信息不完整,新知探究等内容,欢迎下载使用。
这是一份初中化学人教版(2024)九年级上册第五单元 化学反应的定量关系课题2 化学方程式教课内容课件ppt,共24页。PPT课件主要包含了课题2第3课时,质量比,∶32,正比例,计算依据,设未知量,x08g,简明地写出答案,注意事项,计算结果要带单位等内容,欢迎下载使用。










