









所属成套资源:2025年高考化学一轮复习方案课件(含练习)
第一单元 第二讲 离子反应 离子方程式-2025年高考化学一轮复习方案课件
展开
这是一份第一单元 第二讲 离子反应 离子方程式-2025年高考化学一轮复习方案课件,文件包含第2讲ppt、第2讲doc等2份课件配套教学资源,其中PPT共60页, 欢迎下载使用。
第2讲 离子反应 离子方程式
1.了解电解质和非电解质、强电解质和弱电解质的概念。2.认识酸、碱、盐等电解质在水溶液中或熔融状态下能发生电离。3.通过实验事实认识离子反应及其发生的条件,能正确书写离子方程式并能进行相关计算。4.掌握常见离子的检验,能根据实验现象推断溶液中的某些离子。
考点一 电解质及其电离
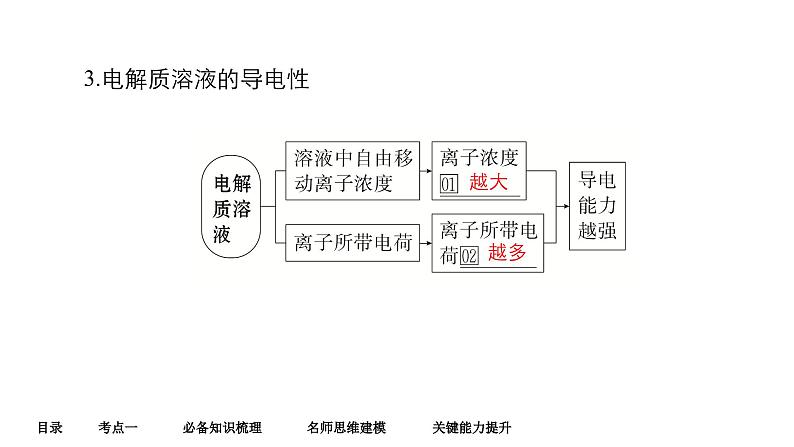
3.电解质溶液的导电性
NaOH===Na++OH-
NaCl溶于水,在水分子的作用下电离成Na+和Cl-。
Cl2为单质,既不属于电解质也不属于非电解质。
HCl是强电解质,但属于共价化合物。
CaCO3、AgCl溶于水的部分完全电离,属于强电解质。
导电性与离子浓度及离子所带电荷数有关。
1.关于电解质与电解质溶液导电性的几个注意点(1)电解质和非电解质都是化合物,单质和混合物既不是电解质也不是非电解质,如Cu、NaCl溶液等,所以能导电的物质不一定是电解质。(2)电解质不一定能导电,如固态NaCl、液态HCl等。(3)自身电离生成离子而导电的化合物才是电解质,而CO2、SO3、SO2、NH3的水溶液能导电,是因为它们与水反应生成的物质能电离出离子,故它们属于非电解质。
(4)电解质的强弱与其溶解性无关。如BaSO4难溶于水但却是强电解质,CH3COOH、NH3·H2O均易溶于水,但却是弱电解质。(5)溶液的导电性与电解质的强弱无关,只与溶液中自由移动离子的浓度大小及所带电荷的多少有关。强电解质溶液的导电能力不一定强,弱电解质溶液的导电能力不一定弱,如稀盐酸的导电能力弱于浓醋酸的导电能力。(6)能电离出H+的物质不一定是酸,如NaHSO4;能电离出OH-的物质不一定是碱,如Mg(OH)Cl;盐的构成不一定仅有金属阳离子和酸根阴离子,如铵盐。
NaCl===Na++Cl-
考点二 离子反应 离子方程式
2Fe3++Cu===2Fe2++Cu2+
Fe3++3SCN-===Fe(SCN)3
实际参加反应的离子符号来表示反应
CaCO3+2HCl==CaCl2+CO2↑+H2O
CaCO3+2H++2Cl-==Ca2++2Cl-+CO2↑+H2O
CaCO3+2H+==Ca2++CO2↑+H2O
H++OH-===H2O
Zn与浓硫酸反应产生SO2气体。
Al(OH)3溶于强碱而不溶于弱碱。
1.离子方程式中物质的“拆分”(1)一般规律①能拆分写成离子形式的物质是易溶的强电解质,包括强酸、强碱、大多数可溶性盐。②不能拆分的物质包括难溶电解质、弱电解质、气体、单质、氧化物,写成化学式。
(2)微溶物的处理①微溶物作为产物视为沉淀,不拆分。②作反应物时,澄清溶液拆分为离子,浑浊液不拆分。(3)产物NH3·H2O的处理
2Fe2++Cl2===2Fe3++2Cl-
2Fe2++2Br-+2Cl2===2Fe3++Br2+4Cl-
2Fe2++4Br-+3Cl2===2Fe3++2Br2+6Cl-
Fe2O3+6H++2I-===2Fe2++3H2O+I2
核心素养 证据推理与模型认知——突破与量有关的离子方程式的书写
[素养要求] 理解与辨析离子反应发生的条件,分析与推测离子方程式的书写,归纳与论证离子反应的特点,形成证据推理与模型认知的学科素养。
Al3++3OH-===Al(OH)3↓
Al3++3OH-===Al(OH)3↓
2I-+Cl2===I2+2Cl-
2Fe2++4I-+3Cl2===2Fe3++2I2+6Cl-
考点三 物质的组成与分类
若溶液中含有Mg2+,也会产生相同的实验现象。
饱和氯水会氧化KSCN,从而无法检验是否有Fe3+生成,进而不能检验Fe2+的存在,应向所得溶液中滴加少量氯水。
若溶液中含有Ag+时,加入BaCl2溶液则产生不溶于盐酸的AgCl沉淀。
加入稀盐酸,引入了Cl-。
2.无色溶液中离子检验的一般思路
3.离子推断的“四原则”
课时作业[建议用时:40分钟]
选择题(每小题只有1个选项符合题意)1.某化学兴趣小组在家中进行化学实验,按照图甲连接好线路后发现灯泡不亮,按照图乙连接好线路后发现灯泡亮,由此得出的结论正确的是( )A.NaCl是非电解质B.NaCl溶液是电解质C.NaCl是弱电解质D.NaCl在水溶液中电离出了可以自由移动的离子
Li3PO4+2HCl
===LiH2PO4+2LiCl
溶液中存在反应Ca2++H2PO ===CaHPO4+H+,反应后溶液酸性增强,需要不断加入适量NaOH溶液以维持溶液的pH基本不变,避免溶液酸性增强影响磷的沉淀
相关课件
这是一份大单元一 第一章 第二讲 离子反应 离子方程式-备战2025年高考化学大一轮复习课件(人教版),文件包含大单元一第一章第2讲离子反应离子方程式pptx、大单元一第一章第2讲离子反应离子方程式教师版docx、大单元一第一章第2讲离子反应离子方程式学生版docx等3份课件配套教学资源,其中PPT共60页, 欢迎下载使用。
这是一份2024届高考化学一轮复习离子反应、离子方程式课件,共1页。
这是一份2024届高三化学高考备考一轮复习专题离子反应 离子方程式课件,共60页。PPT课件主要包含了水溶液中或熔融状态下,化合物,水溶液中和熔融状态下,能全部电离,只能部分电离,自由移动的离子,溶于水,溶于水或受热熔化,全部是H+,全部是OH-等内容,欢迎下载使用。









