

江西省新余市2023-2024学年高一下学期期末质量检测化学试题(无答案)
展开总分:100分考试时间:75分钟
注意事项:
1.答题前,考生务必将自己的姓名、准考证号填写在答题卡上.
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑,如需改动,用橡皮擦干净后,再选涂其他答案标号.回答非选择题时,将答案写在答题卡上,写在本试卷上无效.
3.考试结束后,请将答题卡交回,试卷自行保存.
可能用到的相对原子质量:H-1 C-12 O-16 N-14 Na-23 Mn-55 Fe-56 Cu-64 Mg-24 K-39 Cl-35.5 S-32 Ti-48
一、单项选择题:本题共14小题,每小题3分,共42分.在每小题给出的四个选项中,只有一项是符合题目要求的.
1.非物质文化遗产中承载着大量的化学知识.下列说法错误的是( )
A.仙女下凡新余神话传说中毛衣女衣服上羽毛的主要成分是蛋白质
B.泸州油纸伞伞面涂刷桐油,桐油的主要成分是烃
C.斑铜制作技艺在铜中掺杂金、银等金属,斑铜的熔点比纯铜低
D.德青花瓷所用青料“苏麻离青”属低锰高铁类钴料,是天然无机材料
2.下列化学用语表述错误的是( )
A.羟基的电子式:
B.聚丙烯的结构简式:
C.正丁烷的球棍模型:
D.钙离子的结构示意图:
3.室温下进行下列实验,根据实验操作和现象所得到的结论正确的是( )
4.设为阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,46g有机物中的极性键数目一定为
的溶液中含有的数目为
C.常温下,1mlAl加入足量的浓硝酸中,反应转移的电子数为
D.0℃,101kPa时,22.4L氮气中的共用电子对数目为
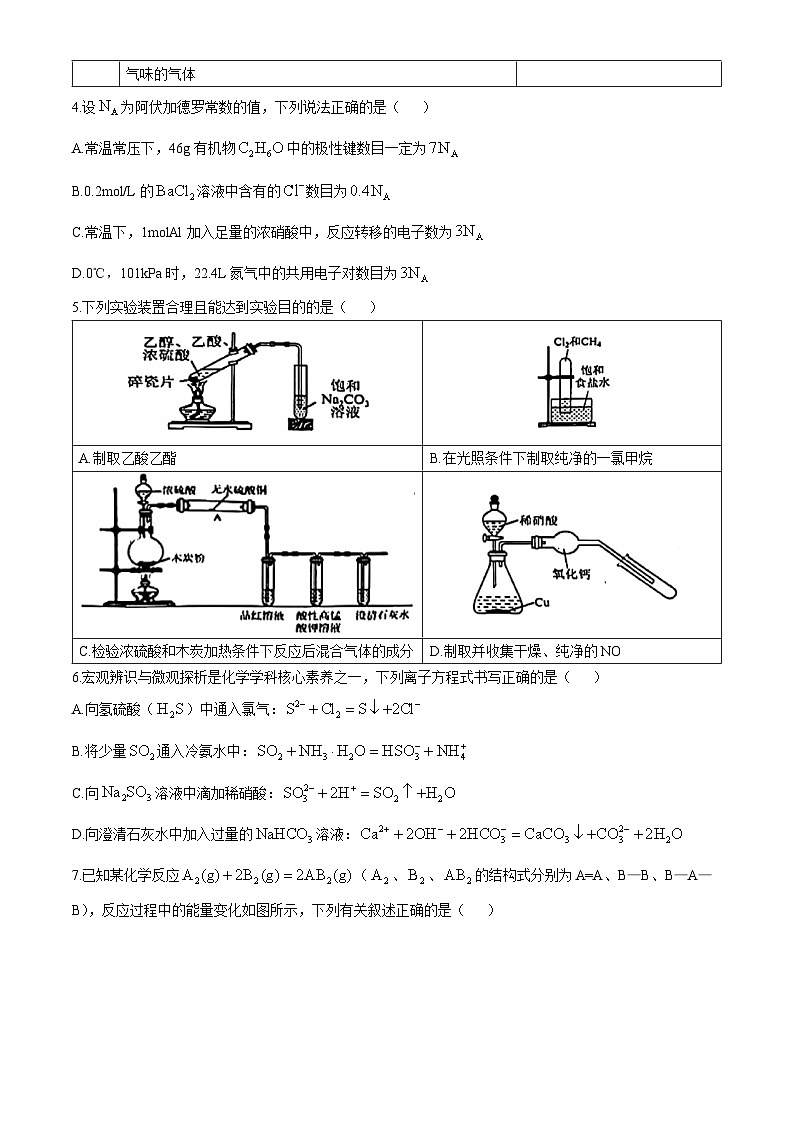
5.下列实验装置合理且能达到实验目的的是( )
6.宏观辨识与微观探析是化学学科核心素养之一,下列离子方程式书写正确的是( )
A.向氢硫酸()中通入氯气:
B.将少量通入冷氨水中:
C.向溶液中滴加稀硝酸:
D.向澄清石灰水中加入过量的溶液:
7.已知某化学反应(、、的结构式分别为A=A、B—B、B—A—B),反应过程中的能量变化如图所示,下列有关叙述正确的是( )
A.该反应过程中有非极性键的断裂和生成
B.该反应若生成2ml,则放出的热量为
C.该反应断开化学键吸收的总能量大于形成化学键放出的总能量
D.铜和稀硝酸反应的能量变化和上图相似
8.一种双极膜电池可长时间工作,其工作原理如图所示.已知双极膜中间层中的解离为和.下列说法错误的是( )
A.电极是该电池的正极
B.电极的电极反应式为
C.双极膜中解离出的透过膜q向Cu电极移动
D.双极膜中质量每减少36g,左侧溶液中硫酸质量减少98g
9.适当补充线粒体调节剂尿石素a,可以调节“老年”造血干细胞的血液再生能力.尿石素a的结构如图,下列关于尿石素a的说法错误的是( )
A.分子式为B.分子中所有原子可能在同一平面上
C.尿石素a可以和乙酸发生酯化反应D.分子中含有3种含氧官能团
10.硫酸钴()主要用于电镀、碱性电池、生产含钴颜料和其他钴产品,可利用COOH与葡萄糖制备,反应的化学方程式为(未配平).设为阿伏加德罗常数的值,下列说法错误的是( )
A.1ml葡萄糖中含有C—H键的数目为
B.氧化剂与还原剂的物质的量之比为
C.生成2.24L(标准状况)时,转移电子数为
D.氧化性:
11.海洋中有丰富的矿产、能源、水产……等资源,部分化学资源获取途径如下:
下列有关说法正确的是( )
A.在第②、③、④步骤中,溴元素均被氧化
B.步骤①制得的晶体转移到新过滤器中,需用大量水进行洗涤
C.除去粗盐中杂质离子加入的试剂先后顺序可以为NaOH、、
D.海水中还含有碘元素,将海水中的碘升华可直接制备单质碘
12.温度时,向容积为2L的密闭容器中加入A(足量)和B,发生反应,第15min时,温度调整到(忽略调整温度时所用的时间且反应中没有使用催化剂).测得各时刻B的物质的量如下表所示.下列说法正确的是( )
A.0~10min,用A表示该反应的平均化学反应速率为
B.混合气的密度保持不变时,无法判断反应是否达到平衡
C.由表中数据可知
D.若30min时反应达到平衡,B的转化率为39.0%
13.催化还原NO,其中一种催化机理如图所示,下列说法错误的是( )
A.1个中含有电子的数目为10个
B.反应过程中Ⅲ和Ⅳ发生的是氧化还原反应
C.总反应离子方程式为:
D.是催化剂且在反应过程中化合价发生了变化
14.在一定量的稀硝酸中,加入一定量的镁和铜组成的混合物,充分反应后金属完全溶解(假设还原产物只有NO),向溶液中继续加入1.5ml/LNaOH溶液至沉淀完全,测得生成沉淀质量比原金属质量增加15.3g,则下列叙述正确的是( )
A.当金属全部溶解时,收集到标准状况下8.96LNO
B.参加反应的金属总质量可能为28.8g
C.整个反应过程中消耗硝酸的物质的量为1.2ml
D.当生成沉淀的量最多时,消耗NaOH溶液体积可能为600mL
二、非选择题:本题共4小题,共58分.
15.(14分)在生产生活中,化学反应通常伴随着能量的变化,人们关注化学反应进行的快慢和程度,以提高生产效率和调控反应条件.
(1)下列变化中属于放热反应的是________(填字母).
①浓硫酸溶于水 ②碳酸氢钠与稀盐酸反应 ③苛性钠固体溶于水 ④氯酸钾分解制氧 ⑤生石灰跟水反应生成熟石灰 ⑥将胆矾加热变为白色粉末
A.①②B.②④C.⑤D.①⑥
(2)已知反应.若要加快该反应的速率,在其他条件不变的情况下,下列措施可行的是________(填字母).
A.适当地升高温度B.改稀硫酸为98%的浓硫酸
C.将纯铁改为生铁D.往稀硫酸中加入少量
(3)在300℃时,X、Y、Z三种气体在恒容密闭容器中反应时的浓度变化如图所示:
请回答下列问题:
①该反应0~2min内的反应速率________________
②下列事实能表明300℃时该反应处于平衡状态的是________(填序号).
A.容器内气体压强保持不变B.混合气体的平均摩尔质量保持不变
C.D.
(4)乙醇可作为燃料使用,用乙醇和组合形成的质子交换膜燃料电池的结构示意图如下:
①则电极d是________(填“正极”或“负极”),电极c的电极反应式为________________.
②若电池中通过质子交换膜的物质的量为5ml,则该燃料电池理论上消耗的在标准状况下的体积为________________.
16.(14分)金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀,而被广泛用作高新科技材料,并被誉为“未来金属”,但在高温时钛化合能力极强,可以与氧、碳、氮及其他元素化合.以钛铁矿(主要成分,钛酸亚铁)为主要原料冶炼金属钛,同时获得副产品甲的工业生产流程如下:
回答下列问题:
(1)为使①反应进行得更充分,可采取的措施是________________________(写出两种);
已知反应①钛铁矿和浓反应的产物之一是,写出该反应的化学方程式:________________________________.
(2)写出上述反应②的化学方程式:________________________________.
(3)反应④要在氩气氛围中进行的理由是________________________,最终所得到的金属钛中会混有少量杂质,可加入________________________溶解后除去.
(4)工业上用电解熔融的氯化镁制取镁单质,该反应的化学方程式为________________.
(5)如果取钛铁矿m吨,杂质的百分含量为w,最终生产出钛n吨(不考虑损耗),则m、n、w三者之间的数学关系是________________________(已知Ti的相对原子质量为48).
17.(14分)氮化镁()是一种易水解的浅黄色粉末,常用于制备高硬度、高热导、抗腐蚀、抗磨损和耐高温的其他元素的氮化物时作为催化剂.实验室可用如图装置制取并与金属镁反应制取氮化镁.
(1)实验室用熟石灰和氯化铵加热制取氨气的化学方程式为________________________.
(2)装置C中氧化铜的作用是氧化氨气制取,其反应的化学方程式为________________.
(3)装置D的作用是________________.
(4)实验开始时点燃A处酒精灯,等到C中固体变为红色后再点燃E处酒精灯,原因是________________.
(5)上述实验所需的氨气还可用下图装置制备,其中a仪器的名称为________________,b导管的作用是________________________.
(6)若取18.0g镁粉放入装置E中,实验结束将固体产物与水充分反应,经过滤、洗涤、干燥得到35.85g固体,则镁粉与氮气反应的转化率为________________.
18.(16分)工业中很多重要的原料都是来源于石油化工,根据流程回答下列问题:
已知:①制备硝基苯的反应为
请回答下列问题:
(1)D的结构简式为________.
(2)①②反应的反应类型分别为_____________________,_____________________.
(3)下列有关丙烯酸()的说法正确的是( )
①含氧官能团为羧基 ②加聚反应后的产物能发生加成反应
③具有酸的通性 ④能发生氧化反应 ⑤有羧酸类的同分异构体
A.只有①③B.只有①③④C.只有①③④⑤D.①②③④⑤
(4)写出下列反应方程式
①反应④的方程式________________________________;
②丙烯酸________________________________.
(5)B和C制备乙酸乙酯,原子利用率为________%(保留整数).
(6)与乙酸乙酯互为同分异构体,且能和氢氧化钠溶液反应的结构有________种.选项
实验操作和现象
结论
A
向溶液中通入,溶液变为浅绿色
还原性:
B
向盛有某盐溶液的试管中滴入氢氧化钠溶液后,试管口处湿润的红色石蕊试纸未变蓝
该盐中一定不含
C
将氧气通入的水溶液中,溶液变浑浊
氧的非金属性大于硫
D
向蔗糖中加入浓硫酸,搅拌得黑色海绵状固体,并放出刺激性气味的气体
浓硫酸体现吸水性和强氧化性
A.制取乙酸乙酯
B.在光照条件下制取纯净的一氯甲烷
C.检验浓硫酸和木炭加热条件下反应后混合气体的成分
D.制取并收集干燥、纯净的NO
t/min
0
5min
10min
15min
20min
25min
30min
n/ml
2.00
1.50
1.25
1.15
1.00
0.88
0.78
江西省新余市2023-2024学年高一上学期期末质量检测化学试卷(Word版附答案): 这是一份江西省新余市2023-2024学年高一上学期期末质量检测化学试卷(Word版附答案),共10页。试卷主要包含了下列“类比”合理的是,如图是部分短周期元素原子等内容,欢迎下载使用。
江西省新余市2023-2024学年高二上学期期末质量检测化学试卷(Word版附答案): 这是一份江西省新余市2023-2024学年高二上学期期末质量检测化学试卷(Word版附答案),共11页。试卷主要包含了25℃时,用图1装置进行实验等内容,欢迎下载使用。
江西省新余市第一中学2022-2023学年高二下学期期末质量检测化学试题word版附答案: 这是一份江西省新余市第一中学2022-2023学年高二下学期期末质量检测化学试题word版附答案,文件包含江西省新余市第一中学2022-2023学年高二下学期期末质量检测化学试题docx、高二化学参考答案docx等2份试卷配套教学资源,其中试卷共12页, 欢迎下载使用。












