



2024山东中考化学二轮专题复习 微专题 盐和化肥的基础知识(课件)
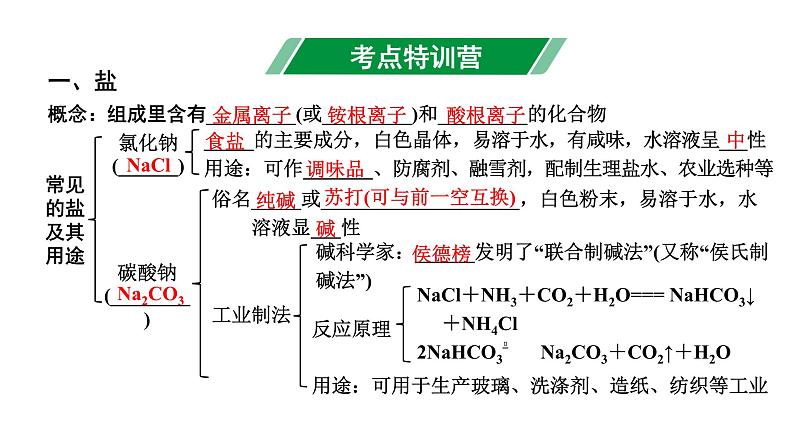
展开概念:组成里含有_________(或_________)和_________的化合物
氯化钠(______)
_____的主要成分,白色晶体,易溶于水,有咸味,水溶液呈___性用途:可作_______、防腐剂、融雪剂,配制生理盐水、农业选种等
碳酸钠(________)
俗名_____或____________________,白色粉末,易溶于水,水 溶液显___性工业制法
碱科学家:______发明了“联合制碱法”(又称“侯氏制碱法”)
苏打(可与前一空互换)
NaCl+NH3+CO2+H2O=== NaHCO3↓ +NH4Cl2NaHCO3 Na2CO3+CO2↑+H2O
用途:可用于生产玻璃、洗涤剂、造纸、纺织等工业
碳酸氢钠(________)
俗名_______,白色固体,能溶于水,水溶液显___性,受热 易分解
焙制糕点所用发酵粉的主要成分之一治疗胃酸过多,化学方程式为____________________________________
NaHCO3+HCl=== NaCl+CO2↑+H2O
碳酸钙(_______)
石灰石、大理石的主要成分,白色固体,___溶于水用途:可用作_________、补钙剂,实验室和工业上都用来制取CO2 工业上制取CO2的化学方程式为______________________
CaCO3 CaO+CO2↑
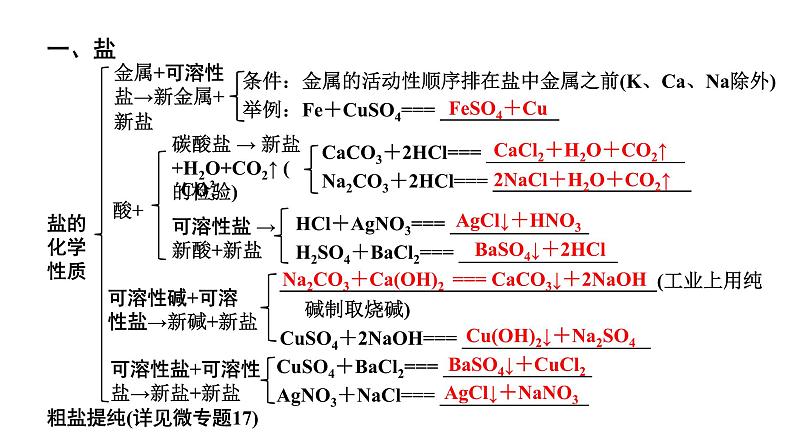
条件:金属的活动性顺序排在盐中金属之前(K、Ca、Na除外)举例:Fe+CuSO4=== ____________
金属+可溶性盐→新金属+新盐
CaCO3+2HCl=== ____________________Na2CO3+2HCl=== ____________________
可溶性盐 → 新酸+新盐
HCl+AgNO3=== ______________H2SO4+BaCl2=== ________________
2NaCl+H2O+CO2↑
BaSO4↓+2HCl
CaCl2+H2O+CO2↑
______________________________________(工业上用纯 碱制取烧碱)CuSO4+2NaOH=== ___________________
可溶性盐+可溶性盐→新盐+新盐
CuSO4+BaCl2=== _______________AgNO3+NaCl=== _______________
可溶性碱+可溶性盐→新碱+新盐
Na2CO3+Ca(OH)2 === CaCO3↓+2NaOH
Cu(OH)2↓+Na2SO4
BaSO4↓+CuCl2
AgCl↓+NaNO3
粗盐提纯(详见微专题17)
定义:由两种________相互交换成分,生成另外两种________的反应特点:双交换,价不变表达式:AB+CD→AD+CB条件:两种化合物相互交换成分,生成物中有______或____ 或_____________________时,复分解反应才可以发生常见盐的溶解性口诀:钾钠铵硝皆可溶、盐酸盐中银不溶、 硫酸盐中钡不溶、其他碳酸盐都不溶
沉淀(可与上两空互换)
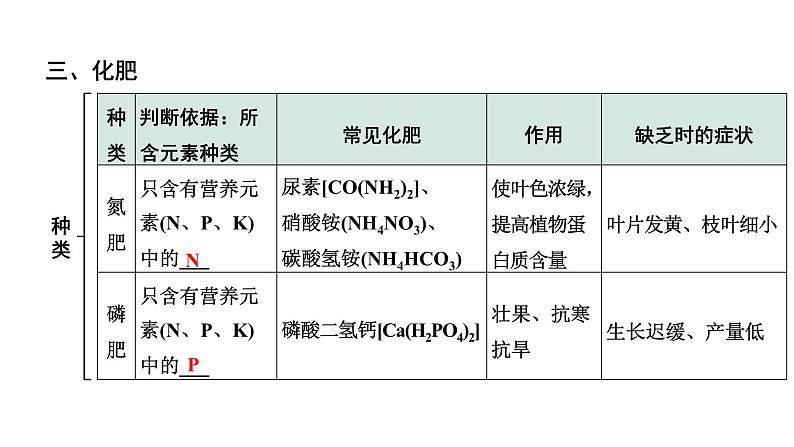
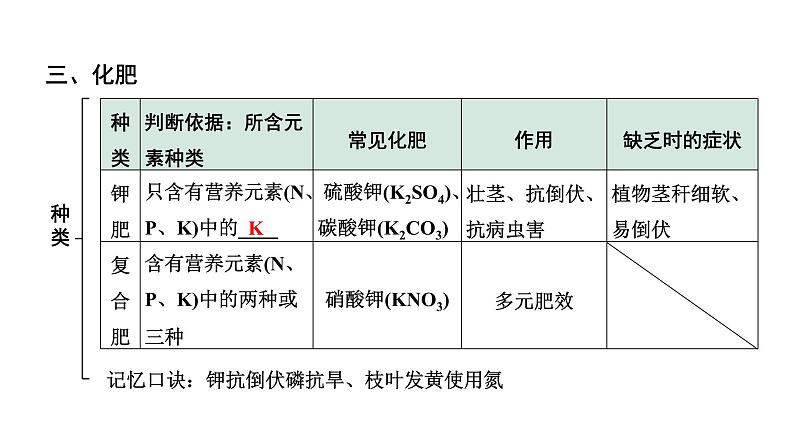
记忆口诀:钾抗倒伏磷抗旱、枝叶发黄使用氮
看外观:氮肥、钾肥为白色晶体,磷肥为____________状加水溶解:___________都可溶,______大多不溶或部分可溶
加_______研磨,产生_____________的气体与碱溶液共热产生能使湿润的红色石蕊试纸变蓝的气体
造成大气污染(产生氮化物和硫化物气体) 水体污染(氮、磷含量升高使水体富营养化) 土壤污染(使土壤酸化、板结)【知识补充】农药使用不当会造成环境污染,农产品上残留的农药会危害人体健康
不合理使用化肥对环境的影响
判断下列说法的正误。①盐中一定含有金属元素。( )②纯碱属于盐,其溶液不能使指示剂变色。( )
【提示】盐中不一定含有金属元素,如NH4Cl。
【提示】碳酸钠溶液显碱性,能使无色酚酞溶液变红,使紫色石蕊溶液变蓝。
【提示】能与稀盐酸反应产生气泡的不一定是碳酸盐,也可能是较活泼的金属。
【提示】可溶性碳酸盐也能与氯化钡溶液反应产生沉淀。
⑤中和反应一定是复分解反应,但复分解反应不一定是中和反应。 ( )⑥所有的氮肥与碱混合研磨均放出氨气。( )⑦将硝酸铵和熟石灰混合施用,既能给农作物提供营养元素,又降低土壤酸性。( )
【提示】只有铵态氮肥与碱混合研磨时才放出氨气,如尿素[CO(NH2)2]与碱混合研磨不会放出氨气。
【提示】硝酸铵是铵态氮肥,熟石灰呈碱性,熟石灰与铵态氮肥混合使用,有氨气放出,降低了肥效。
一、以碳酸钠(Na2CO3)为中心的转化1. 请写出下列物质的化学式:A. _____(可用于灭火)。
2. 写出图中涉及的化学方程式①_______________________________________;②____________________________________;③______________________________________;
Na2CO3+Ba(OH)2=== BaCO3↓+2NaOH
Na2CO3+BaCl2=== BaCO3↓+2NaCl
Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH
④____________________________________;⑤______________________________________;⑥_______________________________。
Na2CO3+CaCl2=== CaCO3↓+2NaCl
Na2CO3+2HCl=== 2NaCl+CO2↑+H2O
CO2+2NaOH=== Na2CO3+H2O
二、含钙化合物之间的转化1. 请写出下列物质的化学式:A. ______;B. ______。
2. 写出图中涉及的化学方程式①___________________________;②_________________________;③_________________________________;
CaO+H2O=== Ca(OH)2
Ca(OH)2+2HCl=== CaCl2+2H2O
④_____________________________________;⑤_____________________________________;⑥_________________________________;⑦____________________________。
CaCl2+Na2CO3=== CaCO3↓+2NaCl
CaCO3+2HCl=== CaCl2+CO2↑+H2O
Ca(OH)2+CO2=== CaCO3↓+H2O
CaO+2HCl=== CaCl2+H2O
1. 镧(La)是一种活动性比锌更强的元素,它的氧化物的化学式是La2O3,La(OH)3是不溶于水的碱,LaCl3、La(NO3)3都可溶于水。由此推断下列几组物质组合,不能直接反应制取LaCl3的是( )A. La和稀盐酸 B. La2O3和稀盐酸C. La(OH)3和稀盐酸 D. La(OH)3和氯化钾溶液
常见盐的性质及其用途(日照、潍坊均5考)
2. (2023潍坊15题2分)下列实验方案不能达到实验目的的是( )
山东其他地市真题精选3. (2021临沂26题4分)如图是“盐的化学性质”思维导图,如表是部分物质的溶解性表(室温)。利用图表中提供的信息回答下列问题。
(1)如果反应①中金属为铝,选用的盐是______(填化学式)。(2)若反应②、③发生复分解反应,发生反应的实质是__________________________________。(3)写出一个符合反应④的化学方程式_____________________________________。
两种物质相互交换成分,有沉淀生成
CaCO3+2HCl=== CaCl2+CO2↑+H2O
Cu(NO3)2+2NaOH===Cu(OH)2↓+2NaNO3
5.化学课堂上,同学们分小组合作探究碳酸钠的性质,请你参与探究并填空。【实验记录与分析】
碳酸钠能与氯化钙发生反应
【反思与拓展】(1)甲同学分析实验一得出:盐溶液_______(选填“一定”或“不一定” )显中性。(2)乙同学用稀硫酸代替实验二中的稀盐酸进行探究,发现实验现象相同。从微观角度分析,这是因为稀盐酸和稀硫酸中都含有_______。(3)丙同学对比实验三和实验四的现象,从微观角度分析,两个反应的实质相同,溶液中相互结合的离子都是___________________。
6. (2022日照10题3分)将粗盐溶解、过滤,除去泥沙后,溶液中仍含有少量的CaCl2、MgCl2、Na2SO4,为除去这些杂质,需用到①BaCl2溶液 ②Na2CO3溶液 ③NaOH溶液三种试剂(为将杂质除尽,所加试剂均稍过量,且过量物质须在后续操作中被除去),充分反应后,过滤,再向滤液中加入适量的稀盐酸,加热蒸发,即可获得较为纯净的NaCl晶体。以上三种试剂的加入顺序不正确的是( )A. ①②③ B. ①③② C. ②③① D. ③①②
粗盐提纯(日照2考;潍坊3考)
7. (2021潍坊25题10分)某兴趣小组进行粗盐(杂质只含有泥沙)提纯实验,并利用所得精盐配制100 g溶质质量分数为15%的氯化钠溶液。请完成下列问题:实验一:如图是甲同学进行粗盐提纯实验的操作示意图。
(1)进行操作③时,当观察到_____________时,停止加热。(2)操作④中玻璃棒的作用是_______________。(3)操作⑤中有一处明显的错误,请你帮他们指出来________________。图中错误改正后, 粗盐提纯实验的正确操作顺序为______________(填操作示意图的序号)。
实验二:乙同学用提纯得到的精盐配制100 g溶质质量分数为15%的氯化钠溶液(假设称量氯化钠时1 g以下用游码)。(4)配制时,除图中提供的仪器外,还需要试剂瓶、镊子和_________(填一种仪器名称)。(5)称量氯化钠时如果发现指针偏向右侧,正确的操作是__________________________,如果称量时氯化钠和砝码位置颠倒了,其它操作步骤均正确,则所配制溶液的溶质质量分数_____(填“大于”“等于”或“小于”) 15%。(6)量水时应选择量筒的规格是____mL(填“10”“50” 或“100”)。
继续添加氯化钠至天平平衡
【反思拓展】(7)经检测所配溶液的溶质质量分数偏小,原因可能是_____________________________(列举一条即可)。(8)海水晒盐采用操作③的原理而不用冷却氯化钠热饱和溶液的方法,原因是_____________________________。
量取水时,仰视读数(合理即可)
氯化钠的溶解度受温度影响不大
8. 现有含杂质氯化镁的氯化钾,欲除去杂质,配制氯化钾溶液,操作流程见下图。
请回答下列问题:(1)加入氢氧化钾溶液,反应的化学方程式是__________________________________。
MgCl2+2KOH === 2KCl+Mg(OH)2↓
(2)过滤。有关过滤操作的叙述不正确的是___(填写字母标号)。A. 用少量水润湿滤纸,并使滤纸与漏斗壁之间留有气泡B. 漏斗下端的管口要紧靠烧杯内壁C. 玻璃棒要靠在三层滤纸的一边D. 滤纸边缘要低于漏斗口,液面要低于滤纸边缘(3)蒸发。把液体倒入蒸发皿,进行加热,在加热过程中,用玻璃棒不断搅拌,目的是______________________________。
防止液体局部过热导致液滴飞溅
(4)天平调零。如图所示,先把游码移至零刻度线处,如果指针静止时偏向右侧,则应该把右端的平衡螺母往___旋动(填写“左”或“右”)。
【温馨提示】更多试题详见微专题17
9. 将下列各组物质放入足量的水中、充分搅拌后,得到无色溶液的是( )A. 硝酸钾和氯化铁 B. 氢氧化钾和盐酸C. 硫酸铜和氢氧化钠 D. 硫酸钠和氯化钡
复分解反应的应用(潍坊2考)
12. 向盛有CuSO4和H2SO4混合溶液的烧杯中,逐滴加入NaOH溶液至过量,沉淀质量、溶质质量和溶剂质量随NaOH溶液质量变化关系如图所示。下列说法错误的是( )A. 乙代表溶质质量B. Q点溶液中溶质为Na2SO4C. 0→P过程反应的化学方程式为2NaOH+H2SO4=== Na2SO4+2H2OD. 原溶液中CuSO4和H2SO4质量相等
(1)丙代表的是________。(2)甲代表的是________,P→Q过程发生反应的化学方程式为____________________________________。(3)加入2a g NaOH溶液后,溶液中含有的微粒有________________。
CuSO4+2NaOH=== Na2SO4+Cu(OH)2↓
13. 实验室有一包白色固体,其中除了碳酸钠以外,还可能含有硝酸钡、硫酸钠、氢氧化钠中的一种或几种。为确定其组成进行如下实验:①取少量白色固体于烧杯中,向烧杯中加入足量水并不断搅拌,固体部分溶解;②继续向烧杯中逐滴加入足量稀硝酸并不断搅拌,此时固体质量变化如图。下列说法正确的是( )A. A→B段对应的实验现象是固体部分溶解,无气泡冒出B. B→C段对应溶液pH逐渐变大C. 原白色固体中一定含有碳酸钠、硫酸钠、硝酸钡D. C点对应溶液中一定含有的溶质是硝酸、硝酸钠、碳酸 钠、硝酸钡
14. 酸、碱、盐是我们身边重要的化合物,在生活和生产中具有广泛的应用。(1)锅炉水垢既会降低燃料的利用率,影响锅炉的使用寿命,还可能造成安全隐患。某锅炉水垢的主要成分有CaCO3、Mg(OH)2、Fe2O3,用“酸洗”法可除去该水垢。①“酸洗”时,一般不选用稀硫酸的原因是________________________________________________________。②写出稀盐酸与氧化铁反应的化学方程式_____________________________。
稀H2SO4与CaCO3反应生成微溶物CaSO4,阻碍反应的继续进行
6HCl+Fe2O3=== 2FeCl3+3H2O
(2)两种抗胃酸药剂的主要成分及建议每次剂量如表:服用Mg(OH)2的药效比服用NaHCO3“强”的原因是______________________________________________________________。
0.3 g Mg(OH)2比0.5 gNaHCO3能中和更多的HCl,所以药效强于NaHCO3
(3)某校化学兴趣小组在课外活动中,对三种溶液进行了检验,检验的结果如下表所示:其中第_____组结果肯定不正确。(4)在CuO和Fe的混合物中加入一定量的稀硫酸,微热,待反应停止后过滤,滤出不溶物后再往滤液里加入一枚铁钉,若铁钉无变化,不溶物中一定含有____,滤液中含有的溶质是_______。
15. 实验桌上有NaOH、Ba(OH)2、Na2CO3、稀硫酸四种溶液,它们只有编号却没有标签。某同学按下列步骤鉴别四种溶液。(分别取少量四种溶液于四支试管中,试管的编号与对应试剂瓶的编号相同)
①写出反应Ⅲ的化学方程式__________________________________。
Ba(OH)2+H2SO4=== BaSO4↓+2H2O
(1)A是________。(写化学式)(2)写出反应Ⅱ的化学方程式_____________________________________,该反应的基本反应类型是___________。(3)C可以转化为B,请写出转化发生的化学方程式为____________________________________。(任写一个)
Na2CO3+H2SO4=== Na2SO4+H2O+CO2↑
Na2CO3+Ca(OH)2=== CaCO3↓+2NaOH
16. NH4NO3是一种化学肥料,某NH4NO3溶液的pH=4。以下说法错误的是( )A. NH4NO3是一种复合肥料B. NH4NO3不能与熟石灰混合使用C. 久施NH4NO3的土壤可能被酸化D. 盐溶液也可能使酸碱指示剂变色
化肥(日照2考;潍坊4考)
17. (山东真题组合)(1)为增强杨桃的抗旱抗寒能力,可以追施___(填“氮”“磷”或“钾”)肥。[潍坊:2021.21(5)](2)在农业上碳酸氢铵可用做___肥,但不能跟碱性物质混用,原因是____________________________________________________。[潍坊:2018.21(3)②]
铵态氮肥跟碱性物质混用会发生反应放出氨气,降低肥效
山东其他地市真题精选18. 今年我市部分地区的小麦得了“软骨病”,出现倒伏现象,为预防这种现象的发生,应提前施用的化肥是( )A. NH4H2PO4 B. CO(NH2)2C. K2CO3 D. NH4HCO3
19. 今年夏粮又获丰收,再显中国饭碗自信,其中化肥功不可没。下列说法错误的是( )A. 尿素[CO(NH2)2]能使作物枝叶繁茂、叶色浓绿B. 磷酸二氢铵(NH4H2PO4)属于复合肥C. 含氮量为31.5%的硝酸铵(NH4NO3)化肥样品为纯净物D. 化肥虽好不能滥用,过度施肥会造成土壤退化和水体污染
2024山东中考化学二轮专题复习 微专题 酸和碱的基础知识(课件): 这是一份2024山东中考化学二轮专题复习 微专题 酸和碱的基础知识(课件),共55页。PPT课件主要包含了常见的酸,浓硫酸,氢离子或H+,化合物,刺激性,干燥剂,不断搅拌,酸的化学性质,ZnCl2+H2↑,固体溶解有气泡产生等内容,欢迎下载使用。
2024山东中考化学二轮专题复习 微专题 酸、碱、盐之间的转化(课件): 这是一份2024山东中考化学二轮专题复习 微专题 酸、碱、盐之间的转化(课件),共20页。PPT课件主要包含了单质或金属,Na2CO3,NH4Cl,CuCl2,复分解反应等内容,欢迎下载使用。
2024贵州中考化学二轮专题复习 主题8 盐 化肥(课件): 这是一份2024贵州中考化学二轮专题复习 主题8 盐 化肥(课件),共16页。PPT课件主要包含了常见的盐,小苏打,常见盐的性质和用途,+H2O,NaHCO3,CaCO3,CO2↑,盐的化学性质,a与某些金属反应,FeSO4+Cu等内容,欢迎下载使用。












