





2024沈阳中考化学二轮专题突破 常见的酸和碱(课件)
展开
这是一份2024沈阳中考化学二轮专题突破 常见的酸和碱(课件),共60页。PPT课件主要包含了沈阳近年真题及拓展,不断运动,氢氧化钠,OH-,H2O,+Na2SO4,稀盐酸或,KOH,出氢氧化钠固体,常见的酸等内容,欢迎下载使用。
常见酸的性质和用途(10年10考)
1. (2021北京)下列物质能除铁锈的是( )A. 盐酸 B. 植物油C. NaOH溶液 D. 食盐水
2. (2021深圳)小明在探究稀硫酸性质时,下列说法正确的是( )A. 稀H2SO4与紫色石蕊试液反应后,溶液变蓝B. 若能与X反应制取H2,则X是CuC. 和金属氧化物反应,有盐和水生成D. 若与Y发生中和反应,则Y一定是NaOH
3. (2022沈阳19题2分)在“探究浓盐酸物理性质”实验过程中,打开瓶塞,会观察到瓶口有______出现,这一现象能够体现微粒具有的性质是__________。
常见碱的性质和用途(10年10考)
4. (2023沈阳4题1分)下列描述属于氢氧化钙化学性质的是( )A. 白色固体 B. 微溶于水C. 溶液有滑腻感 D. 能与CO2反应
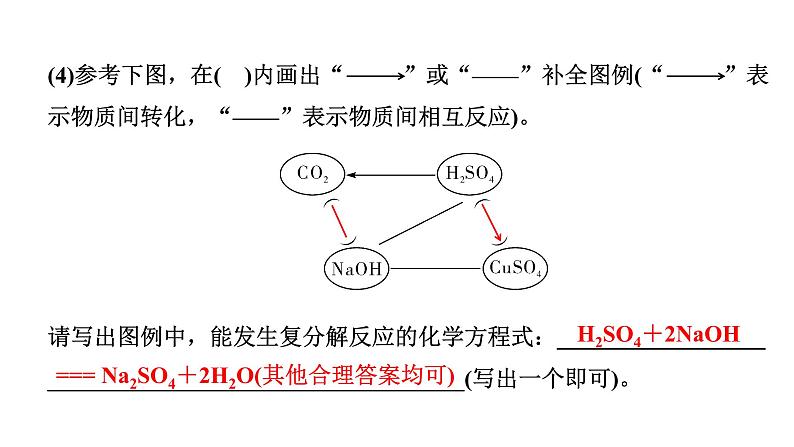
(4)参考下图,在( )内画出“ ”或“——”补全图例(“ ”表示物质间转化,“——”表示物质间相互反应)。
请写出图例中,能发生复分解反应的化学方程式:______________________________________________________(写出一个即可)。
=== Na2SO4+2H2O(其他合理答案均可)
H2SO4+2NaOH
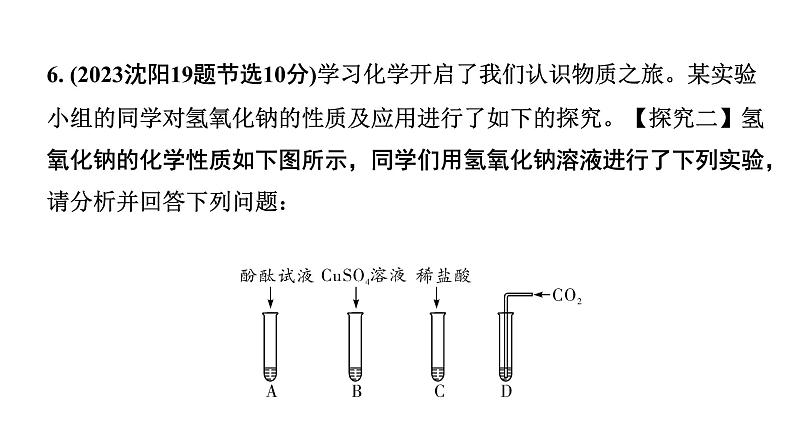
6. (2023沈阳19题节选10分)学习化学开启了我们认识物质之旅。某实验小组的同学对氢氧化钠的性质及应用进行了如下的探究。【探究二】氢氧化钠的化学性质如下图所示,同学们用氢氧化钠溶液进行了下列实验,请分析并回答下列问题:
(1)A试管中观察到的现象是__________________________________。(2)B试管中发生反应的化学方程式:_________________________________________。
溶液由无色变红色(其他合理答案均可)
2NaOH+CuSO4 === Cu(OH)2↓
(3)C、D试管中均无明显现象。①为了证明D中已发生化学反应,向该试管中再加入足量的______________________________________,观察到有气泡产生。②为了证明氢氧化钠溶液和稀盐酸能发生化学反应,同学们设计并进行了如下实验:(所用稀盐酸经估算确保过量)整个实验过程中无明显现象,证明氢氧化钠溶液和稀盐酸能发生化学反应。请写出步骤Ⅱ中所加试剂______________________________________________________。
稀硫酸,其他合理答案均可)
酚酞试液(或硫酸铜溶液、氯化铁溶液,其他合理答案均可)
【探究三】氢氧化钠的应用(1)实验室中的应用实验室中能用氢氧化钠溶液吸收的气体是_____(填字母)。a. 二氧化碳 b. 水蒸气 c. 氯化氢 d. 氧气吸收上述所选气体,一般不用氢氧化钙溶液,主要是因为氢氧化钠和氢氧化钙的_________________________不同。
溶解性(其他合理答案均可)
(2)工业中的应用氢氧化钠常用于制造人造丝、造纸、炼油、纺织、印染与橡胶工业。某造纸厂废水中NaOH的质量分数为1.6%,现有废硫酸4.9 t(H2SO4的质量分数为20%),可以处理的废水质量是____t。
结合化学方程式中的数据分析:若将等质量、等溶质质量分数的稀硫酸和氢氧化钠溶液混合,充分反应后,请判断溶液中一定含有的溶质,并简述你的判断理由:_________________________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
一定有的溶质为Na2SO4和NaOH;NaOH和H2SO4反应后有Na2SO4生成,所以溶液中一定有Na2SO4,根据化学方程式可知每98份质量的H2SO4与80份质量的NaOH恰好完全反应,当加入的两种物质质量相等时,NaOH有剩余,所以溶液中一定有氢氧化钠(其他合理答案均可)
7. (2023辽宁15题8分)某化学小组初步探究氢氧化钠的性质、变化和获得方法。查阅相关资料:Ⅰ. 部分酸、碱和盐的溶解性表(室温) 说明:“溶”表示那种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性,“—”表示那种物质不存在或遇到水就分解了。
(2)完成下列物质转化,各写出一个符合要求的化学方程式。①_______________________________________。② _______________________________________。
【实践与应用】工业上常用电解氯化钠饱和溶液的方法生产氢氧化钠。
HCl+NaOH === NaCl+H2O(合理即可)
Ca(OH)2+Na2CO3 === CaCO3↓+2NaOH
(3)某化工厂计划生产16 t氢氧化钠,请计算:①氢氧化钠的相对分子质量是____;②理论上需要氯化钠的质量是_______。(4)工业生产中可制得含NaOH溶质质量分数约为45%的液碱产品,经进一步处理还可以制得固体氢氧化钠产品。请根据已有知识,对“进一步处理”中使用的方法提出设想并简要说明理由。_____________________________________________________________________________。
蒸发结晶;蒸发溶剂使不饱和溶液变成饱和溶液,继续蒸发溶剂会析
(5)工业固体氢氧化钠的质量指标如图所示,请对产品中的杂质来源作出合理分析。
工业固体氢氧化钠质量指标(合格品)氢氧化钠(NaOH)/%≥98.0碳酸钠(Na2CO3)/% ≤1.0氯化钠(NaCl)/% ≤0.08
①碳酸钠:_______________________________________。②氯化钠:_________________________________。
氢氧化钠与空气中二氧化碳反应生成碳酸钠
原料中的氯化钠没有全部转化为产品
中和反应及其应用(10年7考)
8. (2023沈阳10题1分)农业上改良酸性土壤,应在土壤中施加适量的( )A. 硫酸 B. 盐酸 C. 氢氧化钠 D. 熟石灰9. (2022沈阳11题1分)下列关于中和反应的说法,正确的是( )A. 纯碱和稀盐酸混合后发生中和反应B. 有盐和水生成的反应一定是中和反应C. 工厂废水中含有的硫酸可以用氨水中和D. 中和反应的发生必须借助酸碱指示剂进行判断
10. (2022沈阳20题实验二6分)某化学小组初步探究“氢氧化钠溶液与盐酸发生中和反应时溶液温度的变化情况”。实验二:在一定体积的10%的氢氧化钠溶液中滴加10%的盐酸(室温下),反应中溶液温度的变化如下:
(1)表中Δt的值为____。(2)试绘出溶液温度变化与加入盐酸体积之间的关系图。
(3)根据所绘曲线分析,加入盐酸的体积在0~10 mL时,溶液温度变化的趋势及其原因是__________________________________________________________________________________________________________________________。
溶液温度变化逐渐增大,其原因是中和反应为放热反应,随着盐酸体积的增加,反应继续进行,放出的热量在不断增加(其他合理答案均可)
(4)其他条件不变,若改用20%的盐酸进行滴加,结合对上述曲线的分析,大胆猜想新曲线的最高点位置(不考虑溶液密度和比热容的变化及热量散失等影响因素)。①横坐标及猜想理由:__________________________________________________________________________________________________________。
5,当恰好反应时,放出热量的最大值与原实验相同,此时所需20%盐酸的体积是原来的二分之一(坐标与对应理由合理均可)
②纵坐标及猜想理由:_____________________________________________________________________________________________________________________________________。
大于18.2的某值,当恰好反应时,放出热量的最大值与原实验相同,此时溶液总质量比原实验的小,故Δt最大值大于18.2 ℃(坐标与对应理由合理均可)
素材来源:HJ九下P51 T12
定义:在水溶液中解离时产生的阳离子全部是 的化合物,即酸 → +酸根离子 【易错警示】含有氢元素的物质不一定是酸
腐蚀性(化学性质):浓硫酸会使纸张、蔗糖______吸水性(______性质):在实验室常用来作干燥剂,但不能干燥NH3
向烧杯中先倒____,后倒_______,并用_______不断搅拌;不能“水入酸”的原因是_______________________________________________________________________________________________, 不断搅拌的原因是_________
水的密度较小,会浮在浓硫酸上面,浓硫酸稀释时放出的热量使水立刻沸腾,导致液滴飞溅,容易造成危险
化学性质(“酸五条”)
与酸碱指示剂反应:酸溶液能使紫色石蕊试液变___,不能使酚酞试液变色
与铝:___________________________(写化学方程 式,下同)
通式:稀酸+活泼金属→盐+H2↑(______反应)
__________________________现象:____________
_________________________现象:_________________________________
与铝:________________________________
2Al+6HCl === 2AlCl3+3H2↑
Fe+2HCl === FeCl2+H2↑
有气泡产生,溶液由无色变成浅绿色
Zn+H2SO4 === ZnSO4+H2↑
2Al+3H2SO4 === Al2(SO4)3+3H2↑
通式:酸+金属氧化物→盐+H2O(_______反应)
__________________________________现象:________________________________________________现象:___________________
稀盐酸+氢氧化钠:____________________________稀硫酸+氢氧化镁:__________________________________
通式:酸+碱→盐+H2O(_______反应)
Fe2O3+3H2SO4 === Fe2(SO4)3+3H2O
CuO+2HCl === CuCl2+H2O
NaOH+HCl === NaCl+H2O
H2SO4+Mg(OH)2 === MgSO4+2H2O
通式:酸+盐→新酸+新盐(_______反应)
稀硫酸+碳酸钠:________________ _________________________稀盐酸+碳酸钙:________________ _________________________
现象:______ ______
【易错警示】与酸反应放出气体的物质不一定是碳酸盐
酸溶液具有许多共同化学性质是因为_______________________
Na2CO3+H2SO4
=== Na2SO4+H2O+CO2↑
=== CaCl2+H2O+CO2↑
酸溶液中都含有大量H+
【补充】a.氨水是有氨臭气味的水溶液;b.氧化钙俗称________,有强烈的吸水性, 极易跟水反应,生成_________且放出大量的热,反应的化学方程式为 ________________________,因此可用来作_______
化学性质(“碱四条”)
与酸碱指示剂反应:碱溶液能使紫色石蕊试液变____,能使无色酚酞试液 变____
通式:碱(可溶)+非金属氧化物→盐+H2O
:________________________________
_________________________________现象:________________
CO2+2NaOH === Na2CO3+H2O
CO2+Ca(OH)2 === CaCO3↓+H2O
CaO+H2O === Ca(OH)2
氢氧化钠、氢氧化钙变质的探究(详见微专题6)
举例:氢氧化铝+稀盐酸:______________________________
通式:碱+酸→盐+H2O(_______反应)
举例:氢氧化钙+硫酸铜
通式:碱(可溶)+盐(可溶)→新碱+新盐(_______反应)
______________________________________现象:_______________(利用此反应可以配制 波尔多液)
碱溶液具有许多共同化学性质是因为__________________________
Al(OH)3+3HCl === AlCl3+3H2O
Ca(OH)2+CuSO4 === CaSO4+Cu(OH)2↓
碱溶液中都含有大量的OH-
定义:____和____作用生成____和____的反应,中和反应属于复分解反应
表达式:酸+碱→盐+H2O
a.处理工厂废水,如用氨水中和含硫酸的废水b.改良土壤的酸碱性,如用________改良酸性土壤c.用于医药,如被蚂蚁、蚊子叮咬后涂上稀氨水或肥皂水来止痛、消肿
【易错警示】a. 中和反应不属于四大基本反应类型之一b. 有盐和水生成的反应不一定是中和反应
酸碱中和反应(详见实验突破栏目)
一、常见酸(稀盐酸、稀硫酸)的化学性质:“酸五条”
1. 请写出化学式A_______ B_________ C_________
2. 请写出化学方程式① 稀硫酸+铁:_____________________________② 稀盐酸+烧碱:___________________________③ 稀硫酸+石灰石:_______________________________________
CaCO3+H2SO4 === CaSO4+CO2↑+H2O
Fe+H2SO4 === FeSO4+H2↑
NaOH+HCl === NaCl+H2O
④ 稀盐酸+氧化铁:______________________________⑤ _________________________________⑥ _________________________________
AgNO3+HCl === AgCl↓+HNO3
Fe2O3+6HCl === 2FeCl3+3H2O
BaCl2+H2SO4 === BaSO4↓+2HCl
二、常见碱(氢氧化钠、氢氧化钙)的化学性质:“碱四条”
1. 请写出化学式A__________2. 请写出化学方程式①___________________________ ____________ ___________________________ ____________
CuSO4+2NaOH === Na2SO4+Cu(OH)2↓
CuSO4+Ca(OH)2 === CaSO4+Cu(OH)2↓
②__________________________________ __________________________________③______________________________________
CO2+2NaOH === Na2CO3+H2O
Na2CO3+Ca(OH)2 === CaCO3↓+2NaOH
酸碱中和反应(10年3考)
1. 实验目的通过探究,认识酸碱中和反应。2. 实验原理(1)定义:酸与碱作用生成盐和水。(2)反应的化学方程式:___________________________(以NaOH和HCl反应为例)。
HCl+NaOH === NaCl+H2O
(1)如图1,向盛有氢氧化钠溶液的烧杯中滴加2~3滴酚酞试液,插入温度计和pH计(图中略),溶液变为____色。(2)用胶头滴管逐滴滴入稀盐酸,并用玻璃棒不断搅拌,至溶液颜色刚好变为____色。
(3)取少许反应后溶液于另一试管中,滴加1滴稀氢氧化钠溶液,观察到溶液变为____色。(4)继续滴加稀盐酸,测量整个实验过程中溶液温度和pH并绘制变化曲线如图2、3所示:
4. 实验分析(1)氢氧化钠溶液能使酚酞试液______,当逐滴加入稀盐酸时,溶液颜色__________,最后变为____色,说明溶液中的氢氧化钠反应完全。(2)温度变化图像分析(图2):(2022.20实验二)①随着反应的进行,溶液温度不断______,反应完全后溶液温度开始下降。
②当实验进行到约_____s时,酸和碱恰好完全反应。③从能量变化的角度看,该反应属于_______(填“吸热”或“放热”)反应。
(3)pH变化图像分析(图3):[2022.15(2)]①由图可知:稀盐酸和氢氧化钠已发生中和反应的判断依据是___________________________________;②A点:pH>7,此时溶液中的溶质为________;
pH由大于7逐渐减小到小于 7
③A~B段:pH逐渐减小,但仍大于7,此时溶液中的溶质为_________________;④B点:pH=7(反应结束),此时溶液中溶质为_______;⑤B~C段:pH逐渐减小,pH<7,此时溶液中的溶质为 ____________。
5. 实验反思(1)上述实验过程及现象中(3)的目的是_______________________________________。(2)不能向滴有酚酞的稀盐酸中滴加氢氧化钠溶液来判断二者是否恰好完全反应,是因为________________________________________________。(3)若用紫色石蕊试液代替酚酞试液且滴入盐酸过量,则整个实验过程中的现象为_____________________________________,反应结束后烧杯中的物质为___________。
检验盐酸和氢氧化钠是否恰好
当观察到溶液由无色变为红色时,氢氧化钠已经过量
溶液由蓝色变为紫色,又由紫色变为红色
6. 实验拓展(1)图 4 为酸碱中和反应的微观示意图,请从粒子的角度具体分析该反应的实质__________________________________。
氢离子和氢氧根离子结合生成水分子
(2)酸、碱中和反应后溶液中溶质的检验(10年2考)
b. NaCl、HCl
c. 活泼金属,如Fe (合理即可)
d. NaOH、NaCl
例 如图是向盛有氢氧化钠溶液的烧杯中滴加稀盐酸的实验操作图及反应测得的pH曲线图。请回答下列问题:
(1)图1中发生反应的化学方程式为____________________________,当观察到____________________时,说明氢氧化钠与稀盐酸发生了反应。(2)(2023河南)图2中a点所示溶液中含有____种溶质,当滴入稀盐酸的体积为V2 时,溶液的pH_____(填“>” “<”或“=”)7。
(3)实验中酚酞试液的作用是______________________________________,有同学提出也可以用石蕊试液代替酚酞试液进行实验,你认为________ (填“酚酞试液”或“石蕊试液”)更适合用于验证稀盐酸和稀氢氧化钠溶液发生中和反应,你的理由是____________________________________________________________________________。(4)(2023青海)若实验前忘记滴加指示剂,取反应后溶液少许,加入少量______,若有气体放出,溶液变为浅绿色,则溶液呈酸性,若______________,则溶液呈中性或碱性。
帮助判断稀盐酸和氢氧化钠是否发生反应
紫色石试溶液遇碱性溶液变蓝,遇中性溶液
显紫色,紫色和蓝色界限不明显(合理即可)
(5)[意外现象]有同学在滴加稀盐酸的过程中发现有气泡产生,经询问老师得知该氢氧化钠溶液已变质,请你用化学方程式表示其变质的原因_______________________________。(6)[意外现象]在滴加盐酸时,溶液中有些地方已褪色,有些地方的颜色却一点没有改变,可能的原因___________________________________________________(写一条)。
2NaOH+CO2 === Na2CO3+H2O
未用玻璃棒搅拌,使得酸和碱没有充分
(7)[意外现象]有同学把烧杯改为试管,一边滴加稀盐酸,一边振荡试管,待试管内溶液恰好变为红色时,实验测得试管内溶液的pH”“
相关课件
这是一份2024宁夏中考化学二轮重点专题突破 主题15 化学与生活(课件),共32页。PPT课件主要包含了宁夏近年真题及拓展,表皮角质化和癌症,铁或Fe,钙或Ca,维生素C,甲状腺肿大,合成纤维,塑料凳子,答案B,人类重要的营养素等内容,欢迎下载使用。
这是一份2024宁夏中考化学二轮重点专题突破 主题5 常见的溶液(课件),共41页。PPT课件主要包含了宁夏近年真题及拓展,汽油或洗洁精,溶解或乳化,乙<甲<丙,酸钾固体逐渐减少,操作①俯视读数,配制前烧杯,中有水,溶液10年4考,混合物等内容,欢迎下载使用。
这是一份2024宁夏中考化学二轮重点专题突破 主题2 空气 氧气(课件),共45页。PPT课件主要包含了宁夏近年真题及拓展,达到它的着火点,集气瓶内氧气耗,尽或缺少氧气,分解反应,操作简便节能,将带火星的木,在试管,口放一团棉花,①③②等内容,欢迎下载使用。








