
所属成套资源:全套高考化学一轮复习微专题学案
高考化学一轮复习微专题4热重曲线分析及其应用学案
展开
这是一份高考化学一轮复习微专题4热重曲线分析及其应用学案,共4页。试卷主要包含了解题思路,实例分析等内容,欢迎下载使用。
热重曲线分析的思维步骤
1.解题思路
(1)设晶体的物质的量为1 ml,质量为m。
(2)失重一般是先失水,再失非金属氧化物。
(3)计算每步固体剩余的质量(m余)
样品的固体残留率= eq \f(固体样品的剩余质量,固体样品的起始质量) ×100%。
(4)晶体中金属元素质量不会减少,仍在m余中。
(5)失重最后一般为金属氧化物,由质量守恒可得m氧,由n金属∶n氧,即可求出失重后物质的化学式。
2.实例分析
CaC2O4·H2O在氮气氛围中的热重曲线示意图:
【练真题】
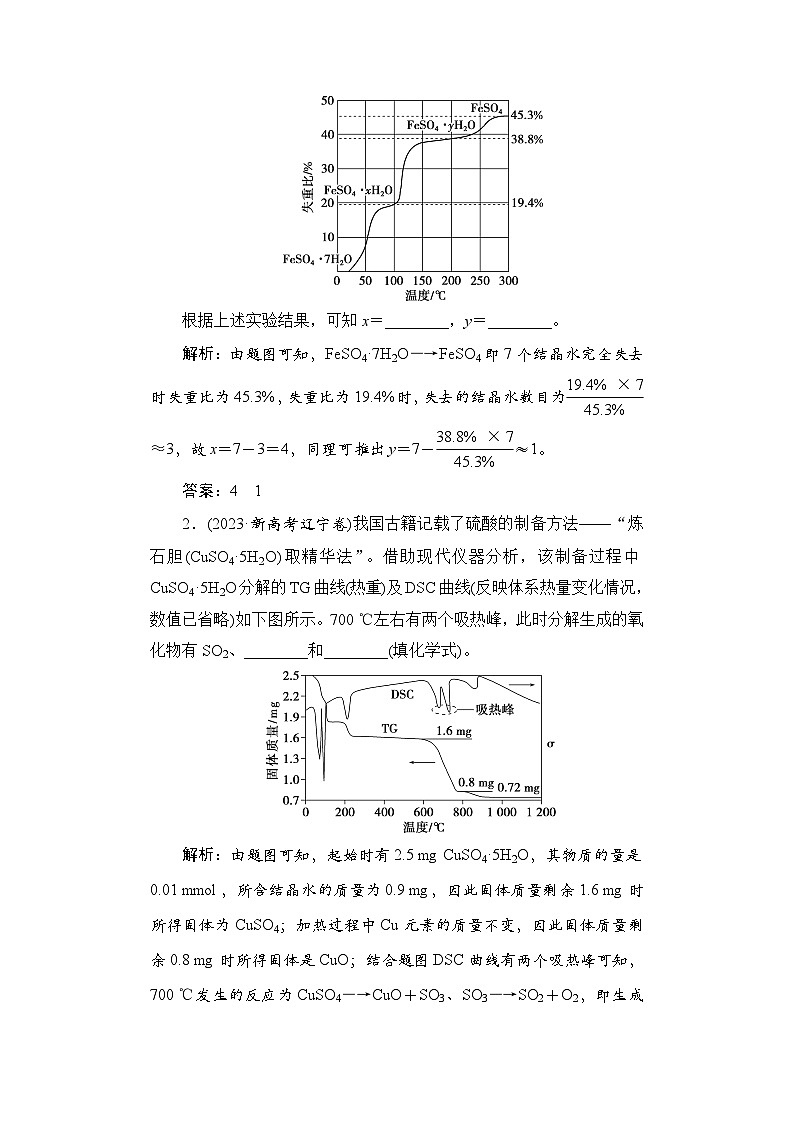
1.(2023·新高考全国乙卷)在N2气氛中,FeSO4·7H2O的脱水热分解过程如下图所示:
根据上述实验结果,可知x=________,y=________。
解析:由题图可知,FeSO4·7H2O―→FeSO4即7个结晶水完全失去时失重比为45.3%,失重比为19.4%时,失去的结晶水数目为 eq \f(19.4%×7,45.3%) ≈3,故x=7-3=4,同理可推出y=7- eq \f(38.8%×7,45.3%) ≈1。
答案:4 1
2.(2023·新高考辽宁卷)我国古籍记载了硫酸的制备方法——“炼石胆(CuSO4·5H2O)取精华法”。借助现代仪器分析,该制备过程中CuSO4·5H2O分解的TG曲线(热重)及DSC曲线(反映体系热量变化情况,数值已省略)如下图所示。700 ℃左右有两个吸热峰,此时分解生成的氧化物有SO2、________和________(填化学式)。
解析:由题图可知,起始时有2.5 mg CuSO4·5H2O,其物质的量是0.01 mml,所含结晶水的质量为0.9 mg,因此固体质量剩余1.6 mg时所得固体为CuSO4;加热过程中Cu元素的质量不变,因此固体质量剩余0.8 mg时所得固体是CuO;结合题图DSC曲线有两个吸热峰可知,700 ℃发生的反应为CuSO4―→CuO+SO3、SO3―→SO2+O2,即生成的氧化物除SO2外,还有CuO、SO3。
答案:SO3 CuO
【练模拟】
3.(2024·广州高三阶段训练)过硼酸钠晶体(NaBO3·4H2O)也可用作无毒漂白剂,加热至70 ℃以上会逐步失去结晶水。实验测得过硼酸钠晶体的质量随温度变化的曲线如图所示,则T2~T3 ℃所对应的化学方程式为_________________________________________________
__________________________________________________。
解析:30.8 g NaBO3·4H2O的物质的量为 eq \f(30.8 g,154 g/ml) =0.2 ml,0~T2 ℃,失去结晶水的质量为30.8 g-27.2 g=3.6 g,物质的量为0.2 ml,所得晶体为NaBO3·3H2O,T2~T3 ℃失去结晶水的质量为27.2 g-20.0 g=7.2 g,物质的量为0.4 ml,所得晶体为NaBO3·H2O,所以T2~T3 ℃所对应的化学方程式为NaBO3·3H2O eq \(=====,\s\up7(△)) NaBO3·H2O+2H2O。
答案:NaBO3·3H2O eq \(=====,\s\up7(△)) NaBO3·H2O+2H2O
4.实验测得25.0 g CuSO4·5H2O受热分解过程中的热重曲线如下图所示。
(1)172 ℃时,剩余固体的化学式为_______________________________________________________。
(2)由胆矾分解制备CuO时,控制的合适温度范围为__________。
解析:(1)25.0 g CuSO4·5H2O的物质的量为0.1 ml,若结晶水全部失去,则剩余固体为0.1 ml CuSO4,质量为16.0 g。由题图可知,172 ℃时,剩余固体的质量为17.8 g>16.0 g,因此该温度下剩余固体为CuSO4的结晶水合物,由关系式CuSO4·5H2O~CuSO4·xH2O,列式得 eq \f(160+18x,250) = eq \f(17.8,25.0) ,解得x=1,故剩余固体的化学式为CuSO4·H2O。(2)由Cu元素守恒可知,25.0 g CuSO4·5H2O能制得8.0 g CuO,由题图可知,控制的合适温度范围为700~810 ℃。
答案:(1)CuSO4·H2O (2)700~810 ℃
相关试卷
这是一份2025版高考化学一轮总复习提升训练第三章金属及其化合物第十讲金属材料与金属的冶炼考点四金属及其化合物的综合应用微考点三热重曲线及分析,共3页。试卷主要包含了3%,6%,不是80等内容,欢迎下载使用。
这是一份微主题热练14 反应过程曲线分析(含解析)-2024年高考化学二轮复习,共8页。试卷主要包含了 常温下,用200 mL 0, 室温下,用0, 常温下,向20等内容,欢迎下载使用。
这是一份专题7.3 热重曲线的相关问题-备战2023年高考化学新编大一轮复习讲义(解析版),共20页。








