

黑龙江省哈尔滨市第十一中学校2023-2024学年高二下学期期末考试化学试题(含答案)
展开分数:100分 时间:75分钟
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23
一、单项选择题:(每题3分,共60分)
1.龙舟节即端午节,为中国国家法定节假日之一,并被列人《人类非物质文化遗产代表作名录》。下列有关端午节习俗中化学知识的说法错误的是
A.黄米小枣粽子富含支链淀粉B.香囊缝制过程中发生了化学变化
C.艾蒿中的纤维素可水解生成葡萄糖D.龙舟表面涂上桐油可增强其耐腐蚀性
2.生活中处处有化学,下列叙述错误的是
A.阿司匹林是一种重要的合成高分子药物,具有解热镇痛作用
B.山梨酸钾可用作食品防腐剂
C.味精是一种常用的增味剂,其主要成分为谷氨酸钠
D.维生素C可用作水果罐头中的抗氧化剂
3. 下列化学用语或表述正确的是
A. 中子数为1的氦核素:B. 的晶体类型:分子晶体
C. 的共价键类型:键D. 的空间结构:平面三角形
4. 下列实验操作或处理方法错误的是
A. 点燃前,先检验其纯度 B. 金属K着火,用湿抹布盖灭
C. 温度计中水银洒落地面,用硫粉处理 D. 苯酚沾到皮肤上,先后用乙醇、水冲洗
5.化学为科技强国作出巨大贡献。下列有关说法正确的是
A.不粘锅内壁涂附的聚四氟乙烯能使溴水褪色
B.用质谱法确定青蒿素分子中的官能团
C.船舶外壳镶嵌锌块以防船体被腐蚀
D.用于制作C919飞机门帘的国产芳砜纶纤维属于天然纤维
6.如下图形表示四种烷烃分子,下列说法不正确的是
A.a的分子构型是正四面体
B.d和c互为同分异构体,物理性质和化学性质均相同
C.b中含有极性共价键和非极性共价键
D.c是b的同系物
7.关于有机物分析检测,下列说法不正确的是
A.通过X射线衍射可确定乙酸的空间结构
B.用溴的四氯化碳溶液,可以鉴别己烯和己醛
C.红外光谱图可获得分子中所含有的化学键或官能团的信息
D.卤代烃与氢氧化钠溶液共热、滴加溶液后根据沉淀颜色可判断卤原子种类
8. 反应可以应用于检验氯气管道的泄漏。下列说法正确的是
A.分子的VSEPR模型:
B.基态Cl原子的核外电子排布式:
C.的电子式:
D.基态N原子的核外电子轨道表示式:
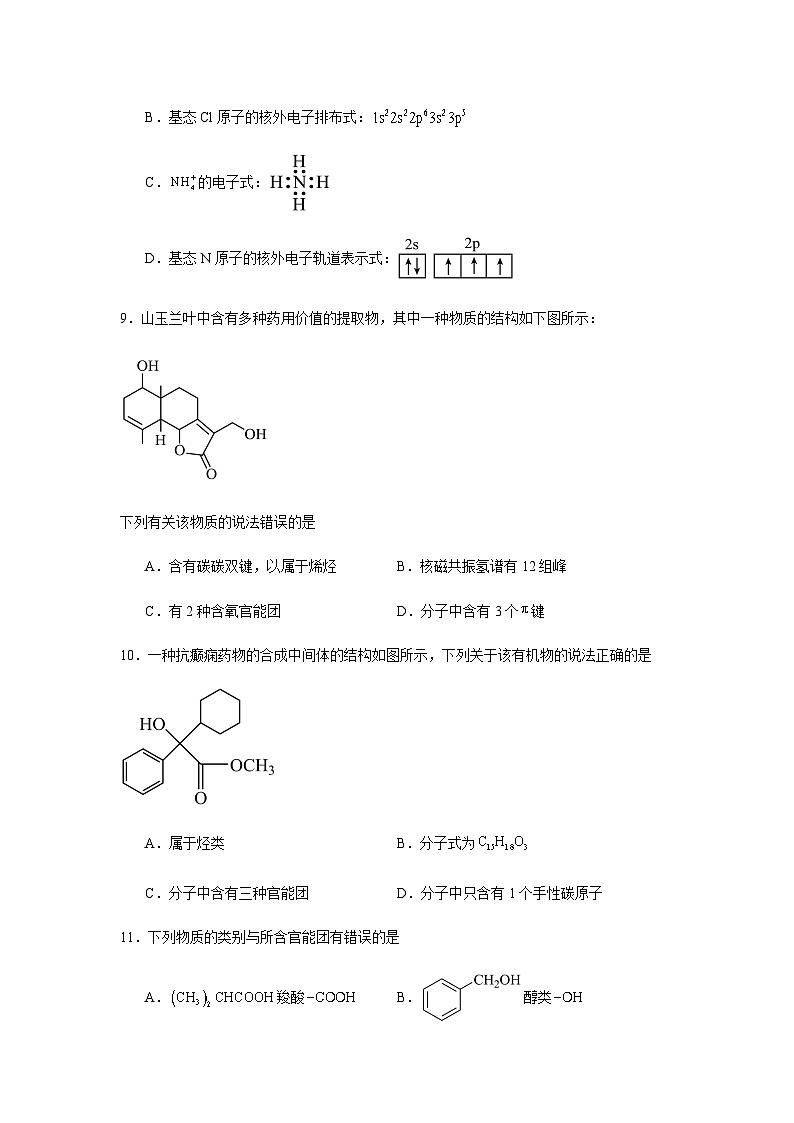
9.山玉兰叶中含有多种药用价值的提取物,其中一种物质的结构如下图所示:
下列有关该物质的说法错误的是
A.含有碳碳双键,以属于烯烃B.核磁共振氢谱有12组峰
C.有2种含氧官能团D.分子中含有3个键
10.一种抗癫痫药物的合成中间体的结构如图所示,下列关于该有机物的说法正确的是
A.属于烃类B.分子式为
C.分子中含有三种官能团D.分子中只含有1个手性碳原子
11.下列物质的类别与所含官能团有错误的是
A.羧酸B.醇类
C.醛类D.烯烃()
12.有机物X是一种合成中间体,其结构简式如图所示。下列有关说法正确的是
A.分子中含有4种含氧官能团
B.能发生加成反应,不能发生水解反应
C.可用酸性KMnO4溶液检验X中的碳碳双键
D.与X互为同分异构体
13.阿司匹林是一种重要的药物,化学名称为乙酰水杨酸(),水杨酸()和乙酸酐()在一定的条件下发生取代反应可制得乙酰水杨酸及物质X,下列说法正确的是
A.水杨酸含有三种官能团
B.乙酰水杨酸的分子式为
C.物质X为
D.标准状况下,1ml水杨酸和金属钠完全反应能产生11.2L氢气
14.化学在物质的分离和合成等方面有重要应用。下列说法错误的是
A.超分子“杯酚”具有分子识别的特性,利用此特性可分离和
B.色谱法是有机化学中获得分子中所含化学键或官能团信息的方法之一
C.与合成可降解塑料的单体的反应原子利用率100%
D.纤维素与硝酸作用生成的硝酸纤维可用于生产火药、塑料和涂料
15.苹果酸的结构简式为,下列说法正确的是
A.苹果酸中能发生酯化反应的官能团有2种
B.1ml苹果酸可与3mlNaOH发生中和反应
C.1ml苹果酸与足量金属Na反应生成1mlH2
D.与苹果酸互为同分异构体
16.聚乳酸是一种新型的生物可降解高分子材料,其合成路线如下:
下列说法不正确的是
A.聚乳酸的重复单元中有两种官能团
B.合成聚乳酸的反应是缩聚反应
C.乳酸与足量的反应生成
D.聚乳酸中存在手性碳原子
17.阿魏酸结构简式为。在阿魏酸溶液中加入合适试剂可以加热,检验其官能团。下列试剂、现象、结论中都正确的是
A.AB.BC.CD.D
18.姜黄素是我国古代劳动人民从姜黄根茎中提取得到的一种黄色食用色素。下列关于姜黄素说法不正确的是
A.分子式为C21H22O6
B.分子中不存在手性碳原子(连有四个不同原子或原子团的碳原子)
C.分子中存在3种含氧官能团
D.既能发生取代反应,又能发生加成反应
19.L-抗坏血酸(维生素C)易溶于水,能促进生长和增强对疾病的抵抗力。下列说法正确的是
A.X分子中所有原子共平面B.1mlY充分燃烧至少需要
C.X分子中含3种含氧官能团D.1mlY转变成X至少需要
20.某物质其结构简式如图所示。下列说法正确的是
A.该物质分子中的两个碳原子的杂化方式相同
B.该物质分子中σ键和π键的个数比为3∶1
C.该物质分子中每个原子最外层均达到8电子稳定结构
D.该物质分子中含有手性碳原子
二、填空题
21.回答下列问题:
(1)下列各物质中,互为同分异构体的是 (填序号。下同);互为同系物的是 。
①NO2和N2O4
②12C和14C
③和
④和CH3CH2CH2CH2Cl
⑤和
⑥和
(2)一种有机物Y的键线式如图所示:
Y的分子式为 ;Y的一氯代物有 种。
(3)化合物它的名称是 。
(4)充分燃烧2.8g某有机物A,生成8.8gCO2和3.6gH2O,这种有机物蒸气的相对密度是相同条件下N2的2倍。求有机A的分子式 。
(5)新制氢氧化铜检验乙醛的化学方程式 。
22.苯甲酸乙酯()(密度1.05g·cm-3),稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等。制备苯甲酸乙酯的过程如下:
①制备粗产品:如图所示装置中,在装置A中加入8.0g苯甲酸、20mL乙醇(密度0.79g·cm-3)、15mL环己烷、3mL浓硫酸,摇匀,加沸石。接通冷凝水,水浴回流约2h,反应基本完成。
②粗产品纯化:加水30mL,分批加入饱和NaHCO3溶液。分液,然后水层用20mL石油醚分两次萃取。合并有机层,用无水硫酸镁干燥。回收石油醚,加热精馏,收集210~213℃馏分。
相关数据如下:
根据以上信息和装置图回答下述实验室制备有关问题:
(1)仪器A名称是 ;仪器B的名称是 ;仪器C的名称是 。
(2)写出制备苯甲酸乙酯反应的化学方程式 。
(3)采用水浴加热的优点是 。
(4)加入饱和NaHCO3溶液的作用除降低苯甲酸乙酯溶解度外,还有中和 。
(5)经精馏得210~213℃馏分6.0mL,则实验中苯甲酸乙酯的产率为 。(保留两位有效数字)
23.化合物是一种医药中间体,可用于制备冠心病药物心可定,也是合成解痉药米尔维林的主要原料,该化合物的合成路线如图所示,已知均为芳香族化合物,且和上表中的乙为同种物质:
(1)的分子式为 。
(2)分子中 手性碳原子(填“有”或“无”)。
(3)步骤所需的试剂和反应条件为 。
(4)下列有关说法正确的是___________。
A.可以使酸性溶液褪色B.中有碳碳双键和碳碳单键交替的结构
C.C可与溶液发生反应D.有6种不同化学环境的原子
(5)的反应类型为 ,化学方程式为 。
参考答案
1-5 BACBC
6-10 BDBAD
11-15 CDCBA
16-20 AAADB
21.【答案】(1) ④ ⑤
(2) 2
(3)2-氯丁烷
(4)C4H8
(5)CH3CHO+2Cu(OH)2+NaOH→CH3COONa+Cu2O↓+3H2O
22.【答案】(1) 三颈烧瓶 球形冷凝管 恒压分液漏斗
(2)+C2H5OH+H2O
(3)水浴加热不但受热均匀,而且温度易于控制
(4)硫酸以及未反应的苯甲酸
(5)
23.【答案】(1)C9H8O2 (2)无 (3)NaOH水溶液、加热 (4)AD
(5) 氧化反应 2+O22+2H2O
选项
试剂
现象
结论
氯化铁溶液
溶液变紫色
它含有酚羟基
银氨溶液
产生银镜
它含有醛基
碳酸氢钠溶液
产生气泡
它含有羧基或酚羟基
溴水
溶液褪色
它含有碳碳双键
物质
苯甲酸
苯甲酸乙酯
石油醚
水
乙醇
环己烷
共沸物(环己烷—水—乙醇)
沸点(℃)
249
212.6
40~80
100
78.3
80.75
62.6
黑龙江省哈尔滨市第三十二中学校2023-2024学年高二下学期4月期中考试化学试题(含答案): 这是一份黑龙江省哈尔滨市第三十二中学校2023-2024学年高二下学期4月期中考试化学试题(含答案),共4页。试卷主要包含了2章,C2H4等内容,欢迎下载使用。
黑龙江省哈尔滨市第一中学2023-2024学年高二上学期期中考试化学试题含答案: 这是一份黑龙江省哈尔滨市第一中学2023-2024学年高二上学期期中考试化学试题含答案,共12页。试卷主要包含了选择题,实验题,填空题等内容,欢迎下载使用。
黑龙江省哈尔滨市第四中学校2023-2024学年高二上学期期末考试化学试卷含答案: 这是一份黑龙江省哈尔滨市第四中学校2023-2024学年高二上学期期末考试化学试卷含答案,共8页。试卷主要包含了5 Ti-48,对于可逆反应,1氯化铵溶液的pH约为4, 25℃时,用0,下列实验不能达到实验目的的是,80等内容,欢迎下载使用。












