

高中化学人教版 (2019)必修 第一册第二节 元素周期律精品课时练习
展开第二课时 元素周期表和元素周期律的应用
【学习目标】1.通过对元素周期性变化规律的再认识,理解基于元素“位置-结构-性质”认识元素性质,基于“结构-性质-用途”认识物质性质,基于元素性质递变的本质原因认识物质世界的基本方法。
2.通过讨论交流,归纳总结,掌握利用元素周期律,推测元素单质及其化合物性质的基本方法,提高逻辑推理能力,发展证据推理与模型认知的化学核心素养。
3.通过信息分析,问题探究,进一步认识和理解元素周期表是元素周期律的具体体现,体会元素周期律(表)在学习元素单质及其化合物知识、科学研究中的重要作用。
【学习重点】同周期、同主族元素性质的递变规律;元素“位、构、性”三者之间的关系及应用。
【学习难点】元素性质与原子结构的关系及应用。
【课前预习】
旧知回顾:1.同周期元素从左到右,原子半径逐渐 ,元素原子失电子能力逐渐 ,得电子能力逐渐 ,元素的金属性逐渐 ,非金属性逐渐 。
2.同主族元素从上到下,原子半径逐渐 ,元素原子失电子能力逐渐 ,得电子能力逐渐 ,元素的金属性逐渐 ,非金属性逐渐 。
新知预习:1.1~20号元素中,非金属性最强的元素形成的单质是 ,金属性最强的元素形成的单质是 ,原子半径最小的是 元素,最高正价与最低负价代数和为0的是 元素。
2.不同周期、不同主族元素的性质:
①金属性:Mg Al,Ca Mg,则碱性:Ca(OH)2 Mg(OH)2 Al(OH)3;
②非金属性:C Si,O C,则氢化物稳定性:H2O CH4 SiH4。
③已知卤族元素的性质递变规律,可推知未学元素砹(At)的化合物的性质HAt 不稳定 ,水溶液呈 强酸 性,AgAt 溶于水。
【课中探究】
情景导入:元素周期表是元素周期律的具体表现形式,是学习化学的一种重要工具。门捷列夫在研究元素周期表时,科学地预言了11种尚未发现的元素,为它们在周期表中留下了空位。例如,他认为在铝的下方有一个与铝类似的元素“类铝”,并预测了它的性质。1875年,法国化学家发现了这种元素,将它命名为镓。镓的性质与门捷列夫推测的一样。门捷列夫还预测在硅和锡之间存在一种元素——“类硅”,15年后该元素被德国化学家文克勒发现,为了纪念他的祖国,将其命名为“锗”。本节课我们将进一步探究元素性质、原子结构和元素在周期表中的位置之间的密切关系,以及利用这些关系可以解决那些问题。
一、元素周期表与元素周期律的关系
活动一、金属元素与非金属元素的分区及性质递变规律
任务一、阅读教材P110页4、5自然段,观察图4-3(如下图),思考金属元素与非金属元素的分区及性质有何递变规律?可得到什么结论?
结论:
任务二、请根据上图中序号所示相关内容,结合元素周期律分析,在现有元素中金属性和非金属性最强的分别是什么元素?
任务三、总结归纳:元素周期表中金属元素与非金属元素的分区有哪些特点及规律?
【对应训练】1.元素周期表中某区域的一些元素多用于制造半导体材料,它们是( )
A.左下方区域的金属元素
B.右上方区域的非金属元素
C.金属元素和非金属元素分界线附近的元素
D.稀有气体元素
2.元素在周期表中的位置,反映了元素的原子结构和元素的性质,下列说法正确的是( )
A.同一元素不可能既表现金属性,又表现非金属性
B.第三周期元素的最高正化合价等于它所处的主族序数
C.短周期元素形成离子后,最外层电子都达到8电子稳定结构
D.同一主族元素的原子,最外层电子数相同,化学性质完全相
活动二、元素的化合价与元素在周期表中的位置关系
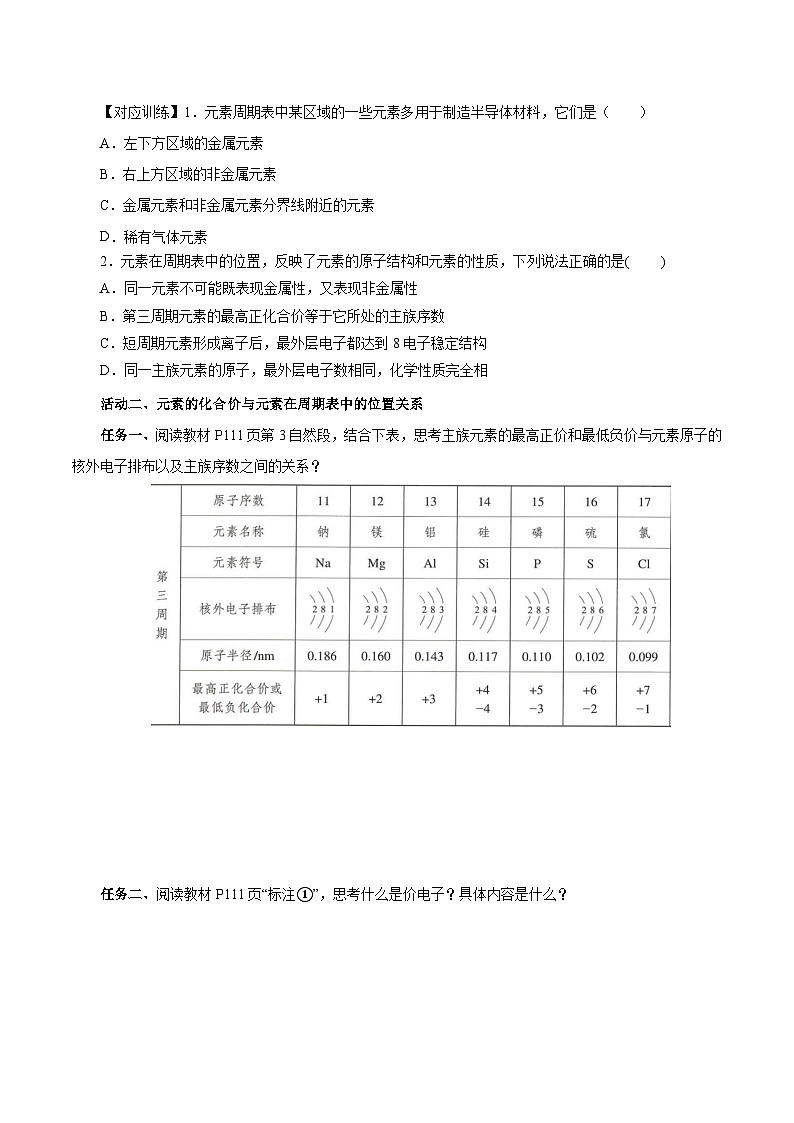
任务一、阅读教材P111页第3自然段,结合下表,思考主族元素的最高正价和最低负价与元素原子的核外电子排布以及主族序数之间的关系?
任务二、阅读教材P111页“标注①”,思考什么是价电子?具体内容是什么?
【对应训练】1.X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示。下列说法错误是( )
A.Q位于第三周期IA族
B.X、Y、Z三种元素组成的化合物可能是盐或碱
C.Z与M的最高价氧化物对应水化物均为强酸
D.简单离子半径:M--> Q+ > R2+
2.砷为第4周期第ⅤA族元素,根据它在周期表中的位置推测,砷不可能具有的性质是( )
A.砷的非金属性比磷弱 B.可以存在-3、+3、+5等多种化合价
C.As2O5对应水化物的酸性比H3PO4弱 D.AsH3比NH3稳定
活动三、判断金属性与非非金属性强弱的方法
任务一、讨论交流:金属性强弱的实质是什么?比较元素金属性强弱的方法有哪些?
【注意】
任务二、讨论交流:非金属性强弱的实质是什么?比较元素非金属性强弱的方法有哪些?
【对应训练】1.碲(Te)是52号元素,位于周期表中VIA族,处于金属区与非金属区的交界线上。下列叙述错误的是( )
A.碲的单质具有半导体的性能 B.碲化氢(H2Te)比H2S更稳定
C.碲可在空气中燃烧生成二氧化碲(TeO2) D.H2TeO4的酸性比H2SO4弱
2.请运用元素周期表的有关理论分析判断,下面几种元素及其化合物性质的推断中正确的是 ( )
A.铊(Tl)的氧化物的水化物可能具有两性
B.砹(At)为无色固体,HAt不稳定,AgAt具有感光性,且不溶于水
C.硫酸锶(SrSO4)是难溶于水的白色固体
D.H2Se 是无色、有毒、比H2S稳定的气体
二、元素周期表和周期律的应用
活动一、根据元素周期表和周期律预测元素的性质
任务一、讨论交流:根据元素周期表中同周期、同主族元素性质的相似性和递变性,完成表格内容。
任务二、根据元素周期表和元素周期律,预测元素“硒(Se)”的相关性质,并填写下表内容。
【对应训练】1.如图是元素周期表的一部分,关于元素X、Y、Z的叙述正确的是( )
A.Y的最高价氧化物对应的水化物是强酸
B.X、Y的气态氢化物的水溶液的酸性:X>Y
C.Z的单质在常温下是固体,可与铁粉反应
D.Z所在的周期中含有26种元素
2.下列比较中正确的是( )
A.离子的还原性:S2->Cl->Br->F-
B.热稳定性:HF>HCl>H2S
C.酸性:HClO>H2SO4>H3PO4
D.碱性:Al(OH)3>Mg(OH)2>Ca(OH)2
活动二、元素周期表和周期律的应用
任务一、阅读教材P111页内容,思考如何根据元素周期表和周期律寻找新物质?
①
②
③
任务二、讨论交流:如何根据元素周期表和周期律指导新元素的发现及预测它们的原子结构和性质?
任务三、问题探究:如何根据元素周期表和周期律中元素“位、构、性”的关系比较元素的性质?
【对应训练】1.下列说法错误的是( )
A.作半导体材料的元素大多数位于周期表中金属元素和非金属元素的交界处
B.农药中常含有的元素通常在元素周期表的右上方区域内
C.构成催化剂的元素通常在元素周期表的左上方区域内
D.在过渡元素中可以寻找作耐高温和耐腐蚀的合金材料的元素
2.下表显示了元素周期表中的一部分,其中①-⑦为短周期元素,已知③与氢元素能组成生活中最常见的化合物,有关叙述错误的是( )
A.最高价氧化物对应水化物酸性:①<②
B.③与氢元素形成10电子化合物呈中性
C.离子半径:⑤>④
D.⑦位于金属与非金属分界线附近,可作半导体材料
【课后巩固】1.(易)教材作业:P112页练习3、4、5、6、7
2.(易)应用元素周期律分析下列推断,其中错误的是( )
①电子层数相同的元素的最高正价随原子序数的增大而升高
②电子层数为2的非金属元素的气态氢化物溶于水后,水溶液均为酸性
③原子核外有3层电子的金属元素的最高价氧化物对应的水化物,其碱性随原子序数的增大而减弱
A.①②B.①③C.②③D.只有③
3.(易)科学家根据元素周期律和原子结构理论预测原子序数为114的元素位于第7周期IVA族,称为类铅元素。下面关于它的原子结构和性质预测正确的是( )
A.类铅元素原子的最外层电子数为6 B.其常见价态为+4、-4
C.它的金属性比铅强 D.它的原子半径比铅小
4.(中)部分短周期元素的原子半径及主要化合价如下,根据表中信息,判断以下叙述正确的是( )
A.氢化物的稳定性为H2T
D.最高价氧化物水化物的碱性 M > L
5.(中)元素的原子结构决定其性质和在周期表中的位置。下列说法正确的是( )
A.元素原子的最外层电子数等于元素的最高化合价
B.元素核外电子排布时,先排满K层,再排L层,先排满M层,再排N层
C.P、S、Cl得电子能力和最高价氧化物对应的水化物的酸性均依次增强
D.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
6.(易)元素周期表中的金属和非金属元素的分界线处用虚线表示。下列说法正确的是( )
A.事物的性质总在不断的发生明显的变化
B.紧靠虚线两侧的元素都是两性金属元素
C.可在虚线附近寻找半导体材料(如Ge、Si等)
D.可在虚线的右上方寻找耐高温材料
7.(难)X、Y、Z、M是四种短周期主族元素,其中X、Y位于同一主族,Y与M、X与Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比X原子的少1。M是同周期主族元素中半径最大的。下列说法错误的是
A.X、Y、Z的最简单氢化物中,X的最简单氢化物沸点最高
B.四种元素简单离子的半径大小为Y>X>Z>M
C.Y的最高价氧化物对应水化物的化学式可表示为HYO3
D.X、Y、M可以组成多种化合物
8.(中)元素周期表的一部分,按要求完成各小题。
(1)化学性质最不活泼的元素___________,(填元素符号,下同)非金属性最强的元素是_________,金属性最强的单质与水反应的离子方程式为______________________________________________________。
(2)①③⑤三种元素的最高价氧化物水化物中,碱性最强是_______________。
(3)①③⑤三种元素的原子半径由大到小的顺序为_______________________________。
(4)某元素的最高价氧化物的水化物既能与酸反应生成盐和水又能与碱反应生成盐和水,该元素是_____。
族
周期
ⅠA ⅡA ⅢA ⅣA ⅤA ⅥA ⅦA 0
1
2
3
4
5
6
7
性质
同周期
同主族
原子半径
得失电子能力
金属性、非金属性
单质氧化性、还原性
单质溶沸点
最高价氧化物水化物酸碱性
气态氢化物稳定性
元素名称
硒
元素符号
原子序数
34
金属还是非金属?
原子结构示意图
最高正价
最低负价
常见中间价
气态氢化物化学式
最高价氧化物
最高价氧化物对应水化物
与硫酸比较酸性
与硫化氢比较稳定性
元素代号
L
M
Q
R
T
原子半径/nm
0.160
0.143
0.089
0.102
0.074
主要化合价
+2
+3
+2
+6、-2
-2
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
二
⑥
⑦
⑪
三
①
③
⑤
⑧
⑩
四
②
④
⑨
人教版 (2019)必修 第一册第二节 元素周期律精品课后测评: 这是一份人教版 (2019)必修 第一册<a href="/hx/tb_c161998_t7/?tag_id=28" target="_blank">第二节 元素周期律精品课后测评</a>,共9页。试卷主要包含了下列说法正确的是等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 元素周期律精品达标测试: 这是一份高中化学人教版 (2019)必修 第一册<a href="/hx/tb_c161998_t7/?tag_id=28" target="_blank">第二节 元素周期律精品达标测试</a>,共4页。试卷主要包含了下列说法正确的是等内容,欢迎下载使用。
高中化学必修一 专题4.2.2 元素周期表和周期律的应用原卷版): 这是一份高中化学必修一 专题4.2.2 元素周期表和周期律的应用原卷版),共1页。













