

所属成套资源:【新课标】人教版化学选择性必修2PPT课件+教案+分层作业+导学案整册(含单元复习资料)
人教版 (2019)选择性必修2第一节 物质的聚集状态与晶体的常识精品课后复习题
展开
这是一份人教版 (2019)选择性必修2第一节 物质的聚集状态与晶体的常识精品课后复习题,共7页。试卷主要包含了硅烷SiH4可用于制造高纯硅,已知等内容,欢迎下载使用。
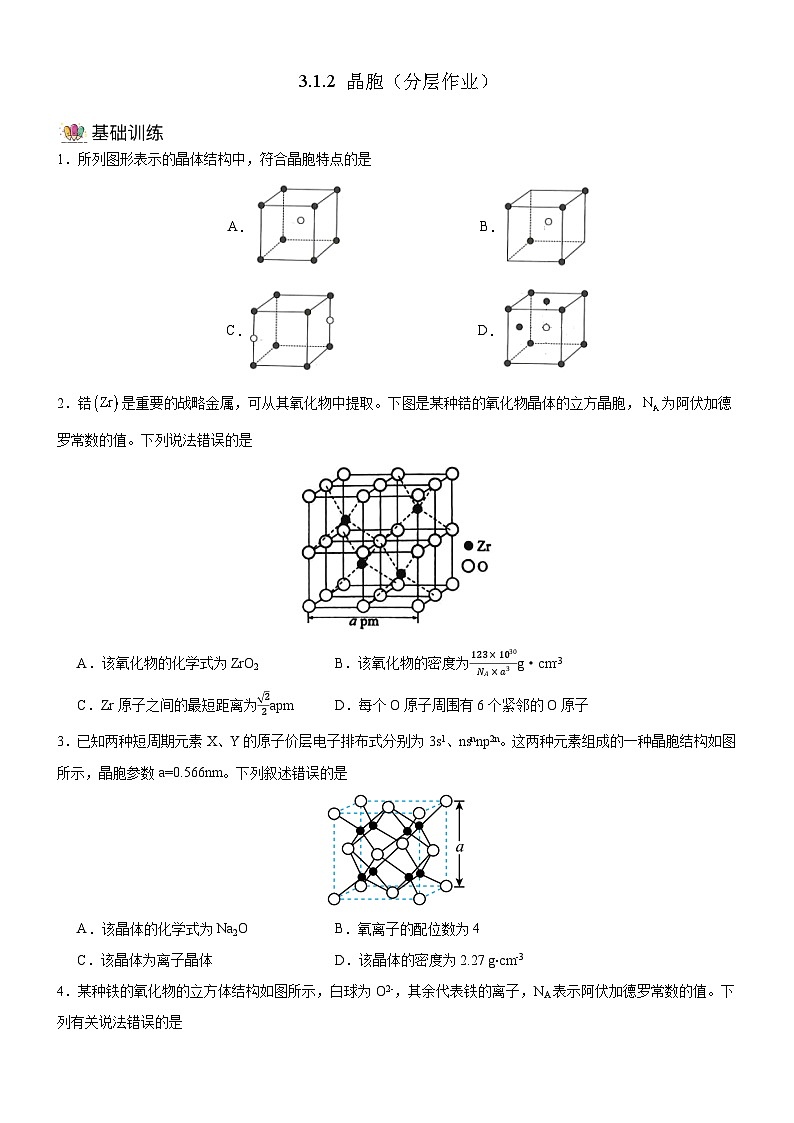
1.所列图形表示的晶体结构中,符合晶胞特点的是
A.B.
C.D.
2.锆是重要的战略金属,可从其氧化物中提取。下图是某种锆的氧化物晶体的立方晶胞,为阿伏加德罗常数的值。下列说法错误的是
A.该氧化物的化学式为ZrO2B.该氧化物的密度为123×1030NA×a3g·cm-3
C.Zr原子之间的最短距离为22apmD.每个O原子周围有6个紧邻的O原子
3.已知两种短周期元素X、Y的原子价层电子排布式分别为3s1、nsnnp2n。这两种元素组成的一种晶胞结构如图所示,晶胞参数a=0.566nm。下列叙述错误的是
A.该晶体的化学式为Na2OB.氧离子的配位数为4
C.该晶体为离子晶体D.该晶体的密度为2.27 g⋅cm-3
4.某种铁的氧化物的立方体结构如图所示,白球为O2-,其余代表铁的离子,NA表示阿伏加德罗常数的值。下列有关说法错误的是
A.Fe的离子均位于O2-构成的正八面体空隙中
B.该铁的氧化物的化学式为Fe3O4
C.设立方体的棱长为1,则点的坐标为(14,14,34)
D.若立方体棱长为dnm,则晶体密度计算式为232NA(d×10−7)3g⋅cm-3
5.下图是某富锂超离子导体的立方体晶胞,阿伏加德罗常数的值为 NA。下列说法错误的是
A.晶体的化学式为Li3OCl
B.图中氧原子的配位数为6
C.图中Cl-O原子的最近距离与Li-O原子的最近距离相等
D.图中晶体密度为72.5NA×a3×10−30g/cm3
6.一种广谱性熏蒸杀虫剂,其晶体熔点约2000℃,晶胞结构如图所示。已知该晶体的密度为表示阿伏加德罗常数的值。下列有关该晶体的说法错误的是
A.化学式为AIP
B.晶体类型为共价晶体
C.晶胞中AI原子的配位数为8
D.两个P原子间的最近核间距为22×358NA×4ρ×1010pm
7.硅烷SiH4可用于制造高纯硅。采用硅化镁法制备SiH4的化学方程式如下:
(1)硅在元素周期表中的位置是 ,基态硅原子占据的最高能级的符号是 。
(2)O、N、H的电负性由大到小的顺序是 。
(3)下列状态的氮中,电离最外层一个电子所需能量最小的是 (填序号)。
a. b. c.
(4)①的沸点比的 (填“高”或“低”),原因是 。
②中H—Si—H的键角 中H—N—H的键角(填“>”“
相关试卷
这是一份人教版 (2019)选择性必修2第四节 配合物与超分子精品练习,共6页。试卷主要包含了为阿伏加德罗常数的值,下列说法不正确的是,下列说法错误的是,设NA为阿伏加德罗常数的值,研究表明等内容,欢迎下载使用。
这是一份高中人教版 (2019)第二节 分子晶体与共价晶体精品课时作业,共5页。试卷主要包含了下列说法正确的是,耐高温高硬度的氮化硅制备反应为,是阿伏加德罗常数的值等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修2第二节 分子晶体与共价晶体优秀课后作业题,共5页。试卷主要包含了干冰的晶胞如图,下列说法不正确的是等内容,欢迎下载使用。










