











沪科技版(2020)必修第一册摩尔质量 气体摩尔体积优秀ppt课件
展开决定物质体积大小的因素
在科学研究或实际生产中,涉及气态物质时,测量体积往往比称量质量更方便。所以,气体一般都是测量体积,而不是称量质量。那么,气体体积与物质的量之间有什么关系呢?
2.单位: L/ml (L·ml-1) 和 m3/ml 。
3.影响因素: 温度和压强
4.标况下的气体摩尔体积:
标准状况下,1ml 任何气体的体积都约是22.4L 。
即标况下的气体摩尔体积是22.4 L/ml记作:Vm=22.4 L·ml-1
条件:标准状况(STP)0℃、 101k Pa 对象:任何气体包括混合气体物质的量:1ml
1.概念:单位物质的量的气体所占的体积叫做气体摩尔体积。符号:Vm
标准状况下的气体摩尔体积示意图
(0.8ml+0.4ml)×22.4L·ml-1=26.88L
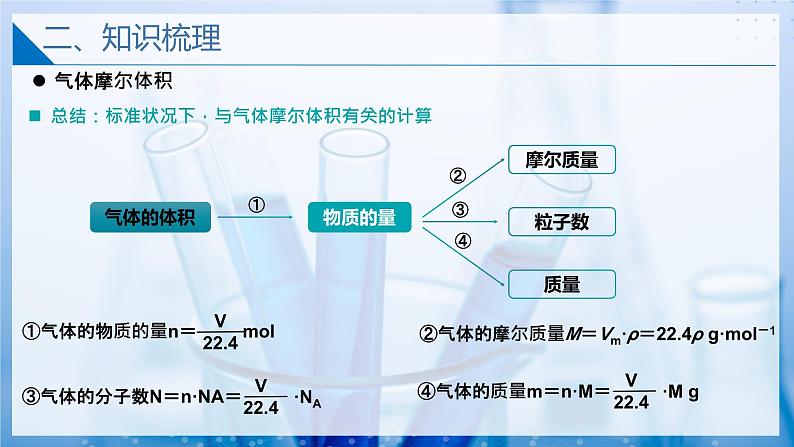
②气体的摩尔质量M=Vm·ρ=22.4ρ g·ml-1
总结:标准状况下,与气体摩尔体积有关的计算
(1)1 ml任何气体的体积都为22.4 L ( )(2)1 ml任何物质在标准状况下所占的体积都为22.4 L ( )(3)标准状况下,1 ml水所占的体积是22.4 L ( )(4)在常温常压下,11.2 L Cl2含有的分子数为0.5NA ( )(5)在常温常压下,1 ml氦气含有的原子数为NA ( )(6)标准状况下,H2的气体摩尔体积是22.4 L ( )
【问题1】请同学们认真思考并判断正误:
【问题3】下列说法正确的是( )A. 在标准状况下,1ml水和1mlH2的体积都约是22.4LB. 2gH2和44gCO2的体积相等C.1ml某气体的体积为22.4L,则该气体一定处于标准状况D. 在标准状况下,1gH2和11.2LO2的物质的量相等
相同条件下固体和液体的体积
1ml下列气体在00C 1.01×105Pa下的体积
为什么相同条件下,1ml不同固体和液体的体积不同,而1ml不同气体的体积几乎相同?物质的体积与什么因素有关?
决定物质体积大小的因素及阿伏加德罗定律
固体、液体物质粒子间间隔很小,在微粒数目相同的情况下,固体、液体的体积主要由粒子本身大小决定。
气体物质分子间间隔远大于分子本身大小,在微粒数目相同的情况下,气体的体积主要由微粒间的距离大小决定,而分子间的平均距离受温度和压强的影响。
粒子数目相同物质的体积关系
相同的温度和压强下,粒子数相同的任何气体都具有___________,也可以说,在相同的温度和压强下、相同体积的任何气体都含有相同数目的粒子。
阿伏加德罗定律适用于任何气体,包括混合气体,不适用于非气体;
同温、同压、同体积、同分子数,共同存在,相互制约,且“三同定一同”。
PV=nRTP:气体压强(单位:Pa )V:气体的体积(单位:L)n:气体分子的物质的量(单位:ml)T:温度(单位:K)R:常数
克拉珀珑方程(或理想气体状态方程)
阿伏加德罗定律的数学表达式
1ml任何气体只有在标准状况下其体积才约是22.4L吗?
例如:1ml任何气体在常温下(25℃),1.106×105Pa压强时
阿伏加德罗定律的推论及应用
1.下列关于决定物质体积的因素的说法不正确的是( )A. 物质的体积取决于粒子数目、粒子大小和粒子间距B. 相同条件下,粒子数相同的任何气体都具有相同体积C. 同温同压下,1 ml任何物质所占有的体积均相同D. 等质量的H2,压强越小、温度越高,气体所占体积越大
2.下列有关气体摩尔体积的描述中正确的是( )A.一定温度和压强下,单位物质的量的气体所占的体积就是气体摩尔体积B.通常状况下的气体摩尔体积约为22.4 LC.标准状况下的气体摩尔体积约为22.4 LD.标准状况下,1 ml O2的体积是22.4 L·ml-1
3.在同温同压(以0 ℃,1.01×105Pa即标准状况为例)下,完成下列问题。(1)1 ml O2的体积是______,2 ml H2的体积是______,V(O2):V(H2)=_______,由此可推知:同温同压下,气体的体积之比等于其__________之比。(2)44.8 L O2的物质的量是______,质量是_____,44.8 L H2的物质的量是______,质量是_____,m(O2):m(H2)=_____,由此可推知:同温同压下,同体积的气体的质量之比等于其__________之比。
(3)1 ml O2的质量是_____,体积是_______,ρ(O2)= =____________(列式不化简,下同)。1 ml H2的质量是_____,体积是_______,ρ(H2)= =_______________。 ρ(O2): ρ(H2) =_____,由此可推知:①同温同压下,气体的密度之比等于其_________之比。②在标准状况下,气体的密度= __________。
4.在一个密闭容器中盛有11 g X气体(X的摩尔质量为44 g·ml-1)时,压强为1×104 Pa。如果在相同温度下,把更多的气体X充入容器,使容器内压强增至5×104 Pa,这时容器内气体X的分子数约为( )A.3.3×1025 B.3.3×1024 C.7.5×1023 D.7.5×1022
5.在一定温度和压强下,2体积X2气体与3体积Y2气体恰好完全反应,生成2体积气体化合物Z,则Z的化学式可能是( )A.XY3 B.XY C.X3Y D.X2Y3
6.同温同压下等质量的SO2气体和CO2气体,下列有关比较的叙述中,正确的是( )①密度比为16∶11 ②密度比为11∶16 ③体积比为16∶11 ④体积比为11∶16A.①③ B.①④ C.②③ D.②④
7.某常见气体在标准状况下的密度为1.25 g·L-1。(1)该气体的相对分子质量为 。(2)若该气体的分子式为A2型,其名称为 ;若该气体的分子式为AB型,其名称为 。
化学第二单元 物质的化学计量完美版ppt课件: 这是一份化学第二单元 物质的化学计量完美版ppt课件,共32页。PPT课件主要包含了学习目标,物质的聚集状态,知识梳理,mol物质的体积,密度Vmρ,分析表中数据得到结论,粒子数目,粒子间距,粒子大小,约1700倍等内容,欢迎下载使用。
苏教版 (2019)专题1 物质的分类及计量第二单元 物质的化学计量教课内容ppt课件: 这是一份苏教版 (2019)专题1 物质的分类及计量第二单元 物质的化学计量教课内容ppt课件,共31页。PPT课件主要包含了学业基础,物质的量,L·mol-1,kPa,核心素养,学考评价等内容,欢迎下载使用。
人教版 (2019)必修 第一册第三节 物质的量课文内容课件ppt: 这是一份人教版 (2019)必修 第一册第三节 物质的量课文内容课件ppt,共25页。













