








所属成套资源:沪科版化学必修一课件+练习
沪科技版(2020)必修第一册第1章 化学研究的天地化学中常用的实验方法物质的制备一等奖ppt课件
展开
这是一份沪科技版(2020)必修第一册第1章 化学研究的天地化学中常用的实验方法物质的制备一等奖ppt课件,文件包含131物质的制备同步课件pptx、131物质的制备docx等2份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
在进行物质制备等化学实验时,同学们必须遵守实验规则和安全要求,必须在确保实验安全的前提下,来取得良好的实验效果。例如,我们要明确实验步骤、注意事项和操作规范,谨慎处理易燃、易爆、有毒、有腐蚀性的物质等。
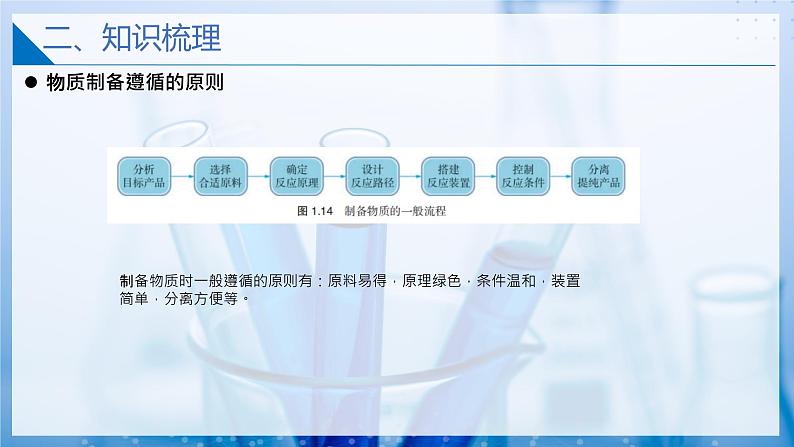
制备物质时一般遵循的原则有:原料易得,原理绿色,条件温和,装置简单,分离方便等。
化学方程式:________________________________________。
向___排空气法(氯气密度大于空气)
观察到集气瓶中充满_____色气体,则证明已集满。
烧杯中盛放的液体是__________。该液体的作用是______________________________。
吸收过量的氯气,防止污染环境
制取反应的化学方程式:______________________________________。
Cl2+2NaOH===NaCl+NaClO+H2O
(1)应用上述装置(如右图)能否收集到纯净干燥的氯气?如果不能,杂质是什么。
杂质HCl气体和水蒸气。
(2)如果要除去以上两种杂质,得到纯净干燥的氯气,需要选择何试剂?
Cl2(HCl、 H2O)
资料信息:已知Cl2能溶于水,常温常压下,在水中的溶解度约为1:2;某实验测得,在饱和食盐水中的溶解度约为1:1;HCl极易溶于水,常温常压下,在水(饱和食盐水)中的溶解度约为1:500。
不能。浓盐酸会挥发,且含有水蒸气。
Cl2 (HCl、H2O)
实验室制取纯净干燥的氯气
核心元素→类别、化合价变化→试剂选择
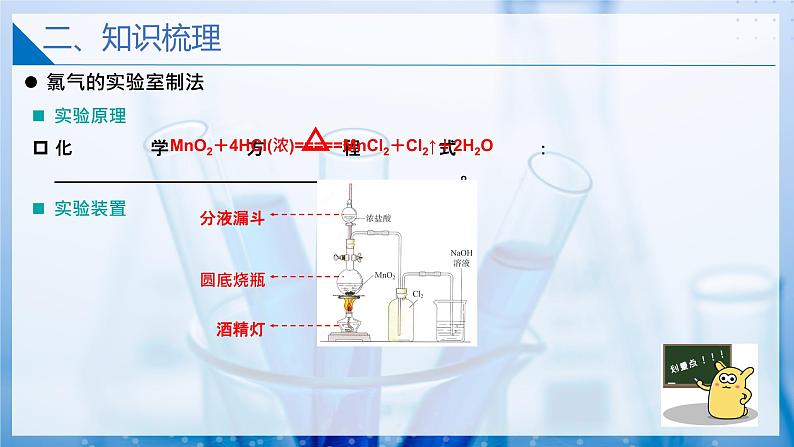
MnO2 + 4HCl(浓) MnCl2 + Cl2↑+ 2H2O
发生→除杂(如需要)→收集→尾气处理(如需要)
药品加入的顺序,化学反应条件的控制等
CaCO3 + 2HCl = CaCl2 + CO2↑+H2O
回顾初中所学的氧气、二氧化碳等气体的实验室制取方法,将相关内容填入下表。讨论氯气的制备装置和它们一样吗?如果一样,属于哪一种?如果不一样,请类比归纳氯气的制备装置。
(1)依据实验室O2与CO2制取、收集方法,请你观察这些装置有什么特点?
Zn与H2SO4反应制取H2
加热KMnO4制取O2
CaCO3与盐酸反应制取CO2
(2)根据上述装置图归纳氧气、二氧化碳是怎样收集的?依据是什么?
提示:氧气用了排水法收集,二氧化碳和氯气都用了向上排空气法收集。
小结: 依据气体的密度、气体在水中的溶解性,以及是否与水反应,选择收集装置。
结合O2、CO2等气体的实验室制取方法,讨论:设计实验室制取气体的装置时,应考虑哪些方面?
考虑 装置的选取依据 和 装置的连接顺序:
设计气体制备装置的基本思路
明确气体制备的原理,写出相应的化学方程式
根据药品状态、反应条件,选择合适的反应装置
分析气体是否含有杂质,根据气体和杂质性质的差异选择除杂、净化方法
根据气体性质,选择收集装置,分析是否需要尾气处理装置
气体制备装置的连接顺序
实验室制气体的制备思路
反应原理、反应物的状态、反应条件等。
实验室制备气体的净化装置的选择
装置Ⅰ(洗气瓶):盛液体除杂试剂,气流方向是长管进,短管出。
不减少被净化气体的量;不引入新杂质;操作简便,易于分离。
装置Ⅱ(干燥管):盛固体除杂试剂,气流方向是粗口进,细口出。
实验室制备气体的收集装置的选择
根据气体的密度、水溶性及是否与水或空气中的O2发生反应来确定气体的收集方法。
排水法:适用于难溶于水且不与水反应的气体,如O2、H2等。
向上排空气法:气体不与空气反应,且密度比空气大,如O2、CO2、Cl2等。
向下排空气法:气体不与空气反应,且密度比空气小,如H2等。
实验室制备气体的尾气处理装置的选择
根据气体的物理性质、化学性质,将气体转化成无毒物质或吸收。
①点燃法:如CO、H2、CH4等易燃性气体可用此法,必须先验纯,再点燃。
②吸收法:如Cl2、SO2、HCl、H2S等可用碱液吸收。
1.某化学兴趣小组利用MnO2和浓盐酸及如图装置制备Cl2。下列分析中不正确的是( )A.①中可用分液漏斗代替长颈漏斗B.①中缺少加热装置C.②中盛放的NaOH溶液可以净化氯气D.④中盛放的NaOH溶液可以吸收尾气
2.某小组使用下图装置制取并收集干燥、纯净的氯气,请回答问题:
(1)A装置中仪器a的名称是__________,KMnO4的作用是_________。
(2)C装置盛放的试剂是________,其作用是_______________________________。
(3)写出D装置中反应的离子方程式:______________________________。
干燥氯气(或除去氯气中的水蒸气)
Cl2+2OH-===Cl-+ClO-+H2O
相关课件
这是一份化学必修第一册分散系一等奖课件ppt,文件包含112分散系同步课件pptx、112分散系分层练习原卷版docx、112分散系分层练习解析版docx等3份课件配套教学资源,其中PPT共26页, 欢迎下载使用。
这是一份沪科技版(2020)必修第一册物质的分类优秀ppt课件,文件包含111物质的分类同步课件pptx、111物质的分类分层练习原卷版docx、111物质的分类分层练习解析版docx等3份课件配套教学资源,其中PPT共35页, 欢迎下载使用。
这是一份人教版 (2019)必修 第一册第三节 氧化还原反应试讲课课件ppt,共37页。PPT课件主要包含了物质失氧的反应,物质得氧的反应,C+O2CO2,氧化还原反应的概念,氧化还原反应,化合价规律,还记得,与四大反应的关系,一定不是氧化还原反应,氧化还原等内容,欢迎下载使用。










