











沪科技版(2020)必修第一册氧化剂和还原剂完整版ppt课件
展开理解氧化性和还原性及其强弱
了解氧化还原反应在实际中的应用
知道常见的氧化剂和还原剂
认识氧化剂、还原剂等概念
生活中常用ClO2、KMnO4、O3、H2O2物质能杀菌消毒,利用它们的什么性质?
在氧化还原反应中,有的元素的化合价升高,有的元素化合价降低,那么,含有这些元素的化合物又叫做什么呢?
失电子,化合价升高,被氧化,发生氧化反应
氧化剂 + 还原剂 = 还原产物 + 氧化产物
得电子,化合价降低,被还原,发生还原反应
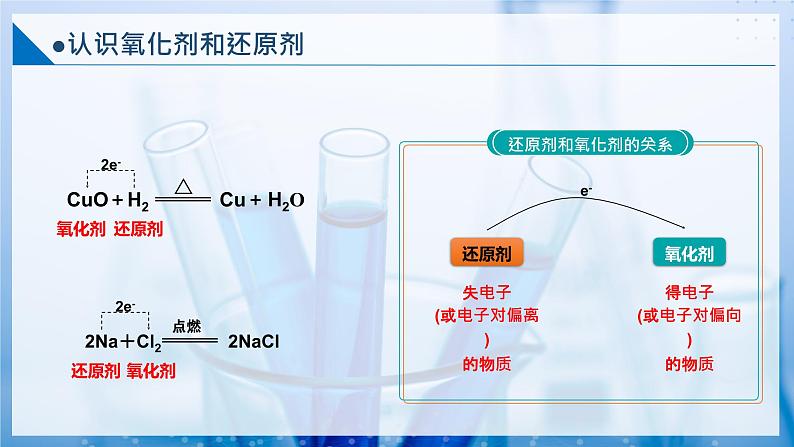
失电子(或电子对偏离)的物质
得电子(或电子对偏向)的物质
在氧化还原反应中,所含元素的化合价_____,即得到电子(或电子对偏向)的物质。
在氧化还原反应中,所含元素的化合价_____,即失去电子(或电子对偏离)的物质。
还原剂失去电子被_____的产物。
氧化剂得到电子被_____的产物。
得电子(或电子对偏向)而使化合价降低的性质(能力)。
失电子(或电子对偏离)而使化合价升高的性质(能力) 。
还(还原剂,具还原性) —升(价升高)—失(失电子)—氧(被氧化)
氧(氧化剂,具氧化性) —降(价降低)—得(得电子)—还(被还原)
①活泼性较强的非金属单质:如_____、O2等。②变价元素的高价态化合物:如_________、________、________等。③过氧化物:如________、_______等。④其他:如HClO、漂白粉[有效成分为Ca(ClO)2]、MnO2等。
①活泼性较强的金属单质:如Al、Fe、Zn等。②某些非金属单质:如________、_______、_______等。③含有较低价态元素的化合物:如________、________等。④其他:如浓盐酸、NH3等。
●常见的氧化剂和还原剂
氧化性还原性强弱主要取决于物质本身得失电子的难易程度,而不取决于得失电子数目的多少。
●氧化性和还原性及其强弱
不正确。如SO2中的硫元素处于中间价态,化合价既可升高又可降低,SO2既有还原性又有氧化性。
一种物质若具有还原性,则不具有氧化性,这种说法正确吗?说明理由。
反应中Fe是_____剂,Cu是_____产物。
例如:Fe+CuSO4===FeSO4+Cu
金属的还原性:Fe>Cu
反应中CuSO4是_____剂, FeSO4是_____产物。
离子的氧化性: CuSO4 > FeSO4
非金属单质的氧化性越强,对应阴离子的还原性越弱
金属单质的还原性越强,对应阳离子的氧化性越弱
有的反应是有益于人类活动的
有的反应对人类活动是有害的
红酒中添加二氧化硫的原因:
红酒的某些成分在储存的过程中会被氧气氧化,而使红酒的口感变差。所以我们应该在红酒中加入一些什么剂呢?
二氧化硫就是这种加入的还原剂,所以我们说二氧化硫应该具有还原性
焦亚硫酸钾是用来代替二氧化硫的一种抗氧化剂
1.下列反应中,属于氧化还原反应,但水既不作氧化剂又不作还原剂的是( )A.SO3+H2O===H2SO4B.3NO2+H2O===2HNO3+NOC.2F2+2H2O===4HF+O2D.2Na+2H2O===2NaOH+H2↑
2.某种飞船以N2H4和N2O4为动力源,发生反应:2N2H4+N2O4===3N2+4H2O,反应温度可高达2 700 ℃,对于该反应,下列说法中正确的是( )A.该反应属于置换反应B.N2H4是氧化剂DC.N2O4是还原剂D.N2既是氧化产物又是还原产物
4.已知X2、Y2、Z2、W2四种物质的氧化性由强到弱的顺序为W2>Z2>X2>Y2,下列氧化还原反应能发生的是( )A.2NaW+Z2===2NaZ+W2B.2NaX+Z2===2NaZ+X2C.2NaW+Y2===2NaY+W2D.2NaZ+X2===2NaX+Z2
3.根据反应的难易(反应条件)比较下列物质的氧化性强弱①2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O②MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O可判断氧化性:KMnO4____MnO2。(2)根据变价元素被氧化或被还原的程度比较下列物质的氧化性强弱①2Fe+3Cl2 2FeCl3②Fe+S FeS可判断氧化性:氯气____硫。
5.常温下,发生下列反应:①16H++10Cl-+ ===2Mn2++5Cl2↑+8H2O②2Fe2++Br2===2Fe3++2Br-③2Br-+Cl2===Br2+2Cl-根据上述反应,可得知相关微粒氧化性由强到弱的顺序是_______________________。
MnO4->Cl2>Br2>Fe3+
6.已知H2能与Cl2、Br2发生反应,前者反应的条件是点燃或光照,后者反应的条件是高温,Cl2和Br2的氧化性强弱关系是________。
Cl2>Br2。与同一还原剂反应时,反应越容易进行,则氧化剂的氧化性越强,故氧化性强弱关系为Cl2>Br2。
高中化学沪科技版(2020)必修第一册氯气的性质优质课件ppt: 这是一份高中化学沪科技版(2020)必修第一册<a href="/hx/tb_c4025822_t3/?tag_id=26" target="_blank">氯气的性质优质课件ppt</a>,文件包含212氯气的性质同步课件pptx、212氯气的性质分层练习原卷版docx、212氯气的性质分层练习解析版docx等3份课件配套教学资源,其中PPT共21页, 欢迎下载使用。
沪科技版(2020)必修第一册第1章 化学研究的天地化学中常用的实验方法物质的制备一等奖ppt课件: 这是一份沪科技版(2020)必修第一册<a href="/hx/tb_c4025812_t3/?tag_id=26" target="_blank">第1章 化学研究的天地化学中常用的实验方法物质的制备一等奖ppt课件</a>,文件包含131物质的制备同步课件pptx、131物质的制备docx等2份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
化学必修第一册分散系一等奖课件ppt: 这是一份化学必修第一册<a href="/hx/tb_c4025807_t3/?tag_id=26" target="_blank">分散系一等奖课件ppt</a>,文件包含112分散系同步课件pptx、112分散系分层练习原卷版docx、112分散系分层练习解析版docx等3份课件配套教学资源,其中PPT共26页, 欢迎下载使用。













