
2024年贵州省新高考化学试卷含答案(选择性)
展开1.(3分)历史文物见证了中华民族共同体在发展中的交往交流交融。下列贵州出土的文物中主要由天然高分子材料制成的是( )
A.AB.BC.CD.D
2.(3分)下列叙述正确的是( )
A.KBr的电子式:
B.聚乙炔的结构简式:
C.的空间结构:平面三角形
D.CH3CH2C(CH3)=CH2的名称:2﹣甲基﹣2﹣丁烯
3.(3分)厨房中处处有化学。下列说法错误的是( )
A.AB.BC.CD.D
4.(3分)贵州盛产灵芝等中药材。灵芝酸B是灵芝的主要活性成分之一,其结构简式如图。下列说法错误的是( )
A.分子中只有4种官能团
B.分子中仅含3个手性碳原子
C.分子中碳原子的杂化轨道类型是sp2和sp3
D.该物质可发生酯化反应、加成反应和氧化反应
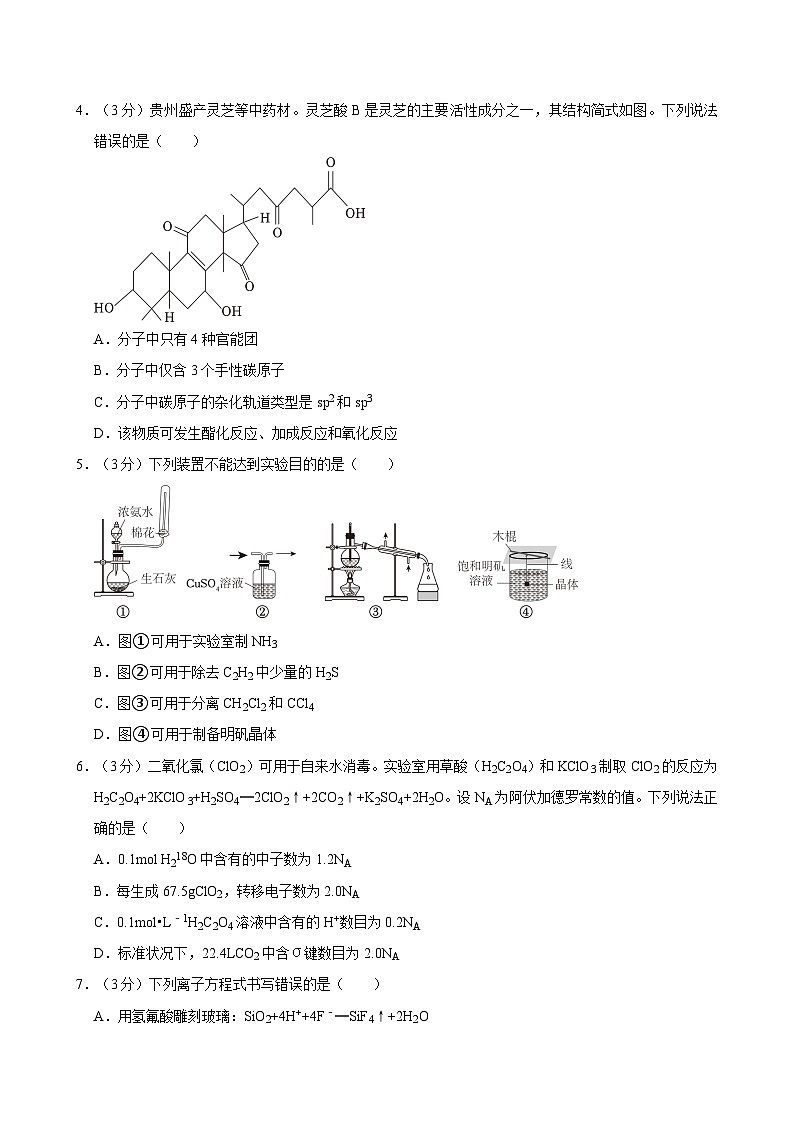
5.(3分)下列装置不能达到实验目的的是( )
A.图①可用于实验室制NH3
B.图②可用于除去C2H2中少量的H2S
C.图③可用于分离CH2Cl2和CCl4
D.图④可用于制备明矾晶体
6.(3分)二氧化氯(ClO2)可用于自来水消毒。实验室用草酸(H2C2O4)和KClO3制取ClO2的反应为H2C2O4+2KClO3+H2SO4═2ClO2↑+2CO2↑+K2SO4+2H2O。设NA为阿伏加德罗常数的值。下列说法正确的是( )
A.0.1ml H218O中含有的中子数为1.2NA
B.每生成67.5gClO2,转移电子数为2.0NA
C.0.1ml•L﹣1H2C2O4溶液中含有的H+数目为0.2NA
D.标准状况下,22.4LCO2中含σ键数目为2.0NA
7.(3分)下列离子方程式书写错误的是( )
A.用氢氟酸雕刻玻璃:SiO2+4H++4F﹣═SiF4↑+2H2O
B.用绿矾(FeSO4•7H2O)处理酸性废水中的Cr2:6Fe2++Cr2+14H+═6Fe3++2Cr3++7H2O
C.用泡沫灭火器灭火的原理:Al3++3═Al(OH)3↓+3CO2↑
D.工业电解饱和食盐水制烧碱和氯气:2Cl﹣+2H2O2OH﹣+H2↑+Cl2↑
8.(3分)我国科学家首次合成了化合物[K(2,2,2﹣crypt)]5[K@Au12Sb20]。其阴离子[K@Au12Sb20]5﹣为全金属富勒烯(结构如图),具有与富勒烯C60相似的高对称性。下列说法错误的是( )
A.富勒烯C60是分子晶体
B.图示中的K+位于Au形成的二十面体笼内
C.全金属富勒烯和富勒烯C60互为同素异形体
D.锑(Sb)位于第五周期第ⅤA族,则其基态原子价层电子排布式是5s25p3
9.(3分)某化合物由原子序数依次增大的短周期主族元素W、X、Y、Z、Q组成(结构如图)。X的最外层电子数等于内层电子数,Y是有机物分子骨架元素,Q和W能形成两种室温下常见的液态化合物。下列说法错误的是( )
A.第一电离能:Y<Z<Q
B.该化合物中Q和W之间可形成氢键
C.X与Al元素有相似的性质
D.W、Z、Q三种元素可形成离子化合物
10.(3分)根据下列实验操作及现象所推出的结论正确的是( )
A.AB.BC.CD.D
11.(3分)一种太阳能驱动环境处理的自循环光催化芬顿系统工作原理如图。光阳极发生反应:+H2O═+2H++2e﹣,+H2O═+H2O2。体系中H2O2与Mn(Ⅱ)/Mn(Ⅳ)发生反应产生的活性氧自由基可用于处理污水中的有机污染物。
下列说法错误的是( )
A.该芬顿系统能量转化形式为太阳能→电能→化学能
B.阴极反应式为O2+2H++2e﹣═H2O2
C.光阳极每消耗1ml H2O,体系中生成2ml H2O2
D.H2O2在Mn(Ⅱ)/Mn(Ⅳ)的循环反应中表现出氧化性和还原性
12.(3分)硼砂[Na2B4O5(OH)4•8H2O]水溶液常用于pH计的校准。硼砂水解生成等物质的量的B(OH)3(硼酸)和Na[B(OH)4](硼酸钠)。
已知:①25℃时,硼酸显酸性的原理
②。
下列说法正确的是( )
A.硼砂稀溶液中c(Na+)=c[B(OH)3]
B.硼酸水溶液中的H+主要来自水的电离
C.25℃时,0.01ml•L﹣1硼酸水溶液的pH≈6.38
D.等浓度等体积的B(OH)3和Na[B(OH)4]溶液混合后,溶液显酸性
13.(3分)贵州重晶石矿(主要成分BaSO4)储量占全国以上。某研究小组对重晶石矿进行“富矿精开”研究,开发了制备高纯纳米钛酸钡(BaTiO3)工艺。部分流程如图:
下列说法正确的是( )
A.“气体”主要成分是H2S,“溶液1”的主要溶质是Na2S
B.“系列操作”可为蒸发浓缩、冷却结晶、过滤、洗涤、干燥
C.“合成反应”中生成BaTiO3的反应是氧化还原反应
D.“洗涤”时可用稀H2SO4去除残留的碱,以提高纯度
14.(3分)AgCN与CH3CH2Br可发生取代反应,反应过程中CN﹣的C原子和N原子均可进攻CH3CH2Br,分别生成腈(CH3CH2CN)和异腈(CH3CH2NC)两种产物。通过量子化学计算得到的反应历程及能量变化如图(TS为过渡态,Ⅰ、Ⅱ为后续物)。
由图示信息,下列说法错误的是( )
A.从CH3CH2Br生成CH3CH2CN和CH3CH2NC的反应都是放热反应
B.过渡态TS1是由CN﹣的C原子进攻CH3CH2Br的α—C而形成的
C.Ⅰ中“N—Ag”之间的作用力比Ⅱ中“C—Ag”之间的作用力弱
D.生成CH3CH2CN放热更多,低温时CH3CH2CN是主要产物
二、非选择题:本题共4小题,共58分。
15.(14分)十二钨硅酸在催化方面有重要用途。某实验小组制备十二钨硅酸晶体,并测定其结晶水含量的方法如下(装置如图,夹持装置省略):
Ⅰ.将适量Na2WO4•2H2O、Na2SiO3•9H2O加入三颈烧瓶中,加适量水,加热,溶解。
Ⅱ.持续搅拌下加热混合物至近沸,缓慢滴加浓盐酸至pH为2,反应30分钟,冷却。
Ⅲ.将反应液转至萃取仪器中,加入乙醚,再分批次加入浓盐酸,萃取。
Ⅳ.静置后液体分上、中、下三层,下层是油状钨硅酸醚合物。
Ⅴ.将下层油状物转至蒸发皿中,加少量水,加热至混合液表面有晶膜形成,冷却结晶,抽滤,干燥,得到十二钨硅酸晶体(H4[SiW12O40]•nH2O)。
已知:
①制备过程中反应体系pH过低会产生钨的水合氧化物沉淀;
②乙醚易挥发、易燃,难溶于水且密度比水小;
③乙醚在高浓度盐酸中生成的与[SiW12O40]4﹣缔合成密度较大的油状钨硅酸醚合物。
回答下列问题:
(1)仪器a中的试剂是 (填名称),其作用是 。
(2)步骤Ⅱ中浓盐酸需缓慢滴加的原因是 。
(3)下列仪器中,用于“萃取、分液”操作的有 (填名称)。
(4)步骤Ⅳ中“静置”后液体中间层的溶质主要是 。
(5)步骤Ⅴ中“加热”操作 (选填“能”或“不能”)使用明火,原因是 。
(6)结晶水测定:称取mg十二铇硅酸晶体(H4[SiW12O40]•nH2O,相对分子质量为M),采用热重分析法测得失去全部结晶水时失重ω%,计算n= (用含ω、M的代数式表示)若样品未充分干燥,会导致n的值 (选填“偏大”“偏小”或“不变”)。
16.(15分)煤气化渣属于大宗固废,主要成分为Fe2O3、Al2O3、SiO2及少量MgO等。一种利用“酸浸—碱沉—充钠”工艺,制备钠基正极材料NaFePO4和回收Al2O3的流程如图:
已知:
①25℃时,Ksp[Fe(OH)3]=2.8×10﹣39,Ksp[Al(OH)3]=1.3×10﹣33,Ksp[Mg(OH)2]=5.6×10﹣12;
②2Na[Al(OH)4](aq)Al2O3•3H2O(s)+2NaOH(aq)。
回答下列问题:
(1)“滤渣”的主要成分为 (填化学式)。
(2)25℃时,“碱沉”控制溶液pH至3.0,此时溶液中c(Fe3+)= ml•L﹣1。
(3)“除杂”时需加入的试剂X是 。
(4)“水热合成”中,NH4H2PO4作为磷源,“滤液2”的作用是 ,水热合成NaFePO4的离子方程式为 。
(5)“煅烧”得到的物质也能合成钠基正极材料NaFeO2,其工艺如下:
①该工艺经碳热还原得到Fe3O4,“焙烧”生成NaFeO2的化学方程式为 。
②NaFeO2的晶胞结构示意图如甲所示。每个晶胞中含有NaFeO2的单元数有 个。
(3)若“焙烧”温度为700℃,n(Na2CO3):n(Fe3O4)=9:8时,生成纯相Na1﹣xFeO2,则x= ,其可能的结构示意图为 (选填“乙”或“丙”)。
17.(14分)在无氧环境下,CH4经催化脱氢芳构化可以直接转化为高附加值的芳烃产品。一定温度下,CH4芳构化时同时存在如下反应:
ⅰ.CH4(g)→C(s)+2H2(g)ΔH1=+74.6kJ•ml﹣1ΔS=+80.84J•ml﹣1•K﹣1
ⅱ.6CH4(g)→C6H6(l)+9H2(g)ΔH2
回答下列问题:
(1)反应ⅰ在1000K时 (选填“能”或“不能”)自发进行。
(2)已知25℃时有关物质的燃烧热数据如表,则反应ⅱ的ΔH2= kJ•ml﹣1(用含a、b、c的代数式表示)。
(3)受反应ⅰ影响,随着反应进行,单位时间内甲烷转化率和芳烃产率逐渐降低,原因是 。
(4)对催化剂在不同的pH条件下进行处理,能够改变催化剂的活性。将催化剂在5种不同pH条件下处理后分别用于催化CH4芳构化,相同反应时间内测定相关数据如下表,其中最佳pH为 ,理由是 。
(5)973K、100kPa下,在某密闭容器中按n(C6H6):n(CH4)=1:5充入气体,发生反应C6H6(g)+CH4(g)→C7H8(g)+H2(g),平衡时C6H6与C7H8的分压比为4:1,则C6H6的平衡转化率为 ,平衡常数Kp= (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数,列出计算式即可)。
(6)引入丙烷可促进甲烷芳构化制备苯和二甲苯,反应如下:
(两个反应可视为同级数的平行反应)
对于同级数的平行反应有,其中v、k分别为反应速率和反应速率常数,Ea为反应活化能,A1、A2为定值,R为常数,T为温度,同一温度下是定值。已知Ea,苯<Ea,二甲苯,若要提高苯的产率,可采取的措施有 。
18.(15分)氨磺必利是一种多巴胺拮抗剂。以下为其合成路线之一(部分试剂和条件已略去)。
回答下列问题:
(1)Ⅰ的结构简式是 。
(2)Ⅱ含有的官能团名称是磺酸基、酯基、 和 。
(3)Ⅲ→Ⅳ的反应类型是 ,Ⅵ→Ⅶ的反应中H2O2的作用是 。
(4)Ⅴ是常用的乙基化试剂。若用a表示Ⅴ中—CH3的碳氢键,b表示Ⅴ中—CH2﹣的碳氢键,则两种碳氢键的极性大小关系是a b(选填“>”“<”或“=”)。
(5)Ⅶ→Ⅷ分两步进行,第1)步反应的化学方程式是 。
(6)Ⅸ的结构简式是 。Ⅸ有多种同分异构体,其中一种含五元碳环结构,核磁共振氢谱有4组峰,且峰面积之比为1:1:1:1,其结构简式是 。
(7)化合物是合成药物艾瑞昔布的原料之一。参照上述合成路线,设计以为原料合成的路线 (无机试剂任选)。
参考答案
一、选择题:本题共14小题,每小题3分,共42分。在每小题给出的四个选项中,只有一项符合题目要求。
1.【答案】C
2.【答案】B
3.【答案】A
4.【答案】B
5.【答案】C
6.【答案】D
7.【答案】A
8.【答案】C
9.【答案】A
10.【答案】D
11.【答案】C
12.【答案】B
13.【答案】B
14.【答案】D
二、非选择题:本题共4小题,共58分。
15.【答案】(1)碱石灰或NaOH固体;吸收挥发的HCl;
(2)防止制备过程中局部pH过低而产生钨的水合氧化物沉淀;
(3)分液漏斗、烧杯;
(4)NaCl;
(5)乙醚易挥发,易燃,遇明火极易发生危险;
(6);偏大。
16.【答案】(1)SiO2;
(2)2.8×10﹣6;
(3)NaOH溶液;
(4)①4Fe3O4+6Na2CO3+O212NaFeO2+6CO2;
②3;
③乙。
17.【答案】(1)能;
(2)6a﹣b﹣9c;
(3)反应i生成固态碳,会覆盖在催化剂的表面,减小气体与催化剂的接触面积;
(4)10.0;pH=10.0时,甲烷的平均转化率最大、芳烃的平均产率最大、产物中积碳平均含量最小;
(5)20%;;
(6)适当降低温度、选择合适的催化剂。
18.【答案】(1);
(2)酰胺基;醚键;
(3)取代反应;作氧化剂;
(4)<;
(5);
(6);;
(7)。文物图示
选项
A.青陶罐
B.带盖铜托杯
C.鹭鸟纹蜡染百褶裙
D.九凤三龙嵌宝石金冠
选项
生活情境
涉及化学知识
A
清洗餐具时用洗洁精去除油污
洗洁精中的表面活性剂可使油污水解为水溶性物质
B
炒菜时不宜将油加热至冒烟
油脂在高温下容易生成对身体有害的稠环化合物
C
长期暴露在空气中的食盐变成了糊状
食盐中常含有容易潮解的MgCl2
D
久煮的鸡蛋蛋黄表面常呈灰绿色
蛋白中硫元素与蛋黄中铁元素生成的FeS和蛋黄混合呈灰绿色
选项
实验操作及现象
结论
A
将Zn和ZnSO4溶液与Cu和CuSO4溶液组成双液原电池,连通后铜片上有固体沉积
原电池中Zn作正极,Cu作负极
B
向洁净试管中加入新制银氨溶液,滴入几滴乙醛,振荡,水浴加热,试管壁上出现银镜
乙醛有氧化性
C
向苯酚浊液中加入足量Na2CO3溶液,溶液由浑浊变澄清
苯酚的酸性比H2CO3强
D
向BaCl2溶液中先通入适量SO2,无明显现象,再加入稀HNO3,有白色沉淀生成
稀HNO3有氧化性
物质
CH4(g)
C6H6(l)
H2(g)
ΔH/(kJ•ml﹣1)
a
b
c
pH
CH4平均转化率/%
芳烃平均产率/%
产物中积碳平均含量/%
2.4
9.60
5.35
40.75
4.0
9.80
4.60
45.85
7.0
9.25
4.05
46.80
10.0
10.45
6.45
33.10
12.0
9.95
4.10
49.45
安徽省示范高中培优联盟2023-2024学年高二下学期春季联赛化学试卷(Word版附解析): 这是一份安徽省示范高中培优联盟2023-2024学年高二下学期春季联赛化学试卷(Word版附解析),文件包含安徽省示范高中培优联盟2023-2024学年高二下学期春季联赛化学试题Word版含解析docx、安徽省示范高中培优联盟2023-2024学年高二下学期春季联赛化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共43页, 欢迎下载使用。
全国高中学生化学竞赛(决赛)理论试题14版: 这是一份全国高中学生化学竞赛(决赛)理论试题14版,共7页。
安徽省宣城市泾县重点中学2022-2023学年高一下学期竞赛选拔化学试题含解析: 这是一份安徽省宣城市泾县重点中学2022-2023学年高一下学期竞赛选拔化学试题含解析,共19页。试卷主要包含了单选题等内容,欢迎下载使用。