






所属成套资源:2024--2025年高考化学一轮复习全套知识课件(新教材,新一轮)
课件 高考化学一轮复习第八单元 化学反应速率与化学平衡 第32讲 化学反应的方向与调控
展开
这是一份课件 高考化学一轮复习第八单元 化学反应速率与化学平衡 第32讲 化学反应的方向与调控,共60页。PPT课件主要包含了夯实必备知识,自发反应,无需借助外力,熵和熵变,混乱程度,生成物,反应物,反应进行的方向,1判据,对点自测等内容,欢迎下载使用。
第32讲 化学反应的方向与调控
考点一 化学反应的方向考点二 反应条件的调控经典真题·明考向作业手册
夯实必备知识 | 提升关键能力
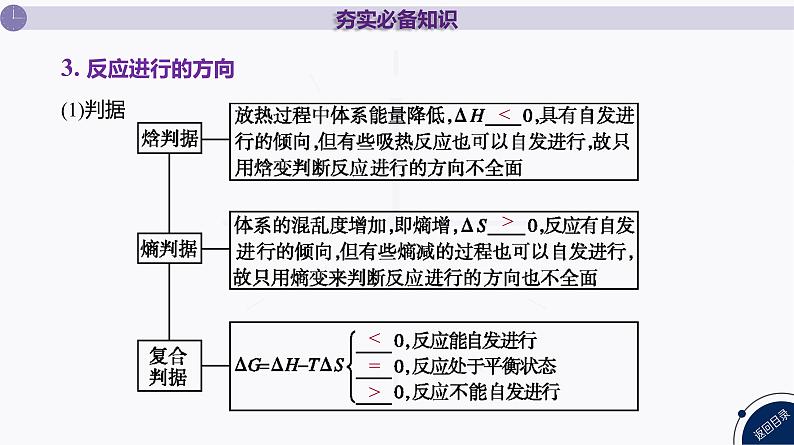
考点一 化学反应的方向
(1)含义在温度和压强一定的条件下 就能自发进行的反应称为自发反应。(2)特点①体系趋向于从 状态转变为 状态(体系对外部 或 热量)。 ②在密闭条件下,体系有从 自发地转变为 的倾向性(无序体系更加稳定)。
(1)熵是量度体系 的物理量,符号为S。 (2)影响熵大小的因素:①相同条件下,物质不同熵不同。②同一物质:S(g) S(l) S(s)。 (3)熵变(ΔS)= 的总熵- 的总熵。
(2)一般规律:①ΔH 0,ΔS 0的反应任何温度下都能自发进行; ②ΔH 0,ΔS 0的反应任何温度下都不能自发进行; ③ΔH和ΔS的作用相反,且相差不大时, 对反应的方向起决定性作用。当ΔH0时, 下反应能自发进行。 说明:对于一个特定的气相反应,熵变的大小取决于反应前后气体物质的化学计量数的大小。
1.判断正误(正确的打“√”,错误的打“×”)(1)能自发进行的反应,一定是放热反应( )(2)同种物质不同状态时熵值不同,气态时最大( )(3)在同一条件下不同物质有不同的熵值,其体系的混乱程度越大,熵值越大( )(4)熵增的反应一定能自发进行( )
[解析] (1)吸热反应也可能自发进行。
[解析] (4)反应的自发性由焓判据和熵判据共同决定。
(5)一个反应能否自发进行取决于该反应是放热还是吸热( )(6)用焓判据或熵判据判断同一反应进行的方向其结果相同( )
[解析] (5)反应能否自发进行与ΔH、ΔS有关。
[解析] (6)用焓判据或熵判据判断同一反应进行的方向其结果不一定相同。
2.25 ℃和1.01×105 Pa时,反应:2N2O5(g) = 4NO2(g)+O2(g) ΔH=+56.7 kJ·ml-1能自发进行,其原因是 。
[解析] 根据熵判据,该反应是熵增反应,能自发进行;根据焓判据,该反应是吸热反应,不能自发进行。事实上该反应能自发进行,说明熵增效应大于能量效应。
题组 化学反应进行的方向
1.下列说法正确的是( )A.非自发反应一定不能实现B.同种物质气态时熵值最小,固态时熵值最大C.反应NH3(g)+HCl(g) = NH4Cl(s)在室温下可自发进行,则该反应的ΔH液态>固态,B错误;
反应能自发进行说明:ΔH-TΔS
相关课件
这是一份2025届高考化学一轮总复习第8章化学反应速率与化学平衡第40讲化学平衡常数化学反应的方向与调控课件,共58页。PPT课件主要包含了答案48,答案01,答案2120,混乱程度,熵的变化,自发进行,增大反应物浓度,无影响等内容,欢迎下载使用。
这是一份新教材(广西专版)高考化学一轮复习第7章第3讲化学平衡常数化学反应的方向与调控课件,共60页。PPT课件主要包含了内容索引,强基础增分策略,增素能精准突破,研专项前沿命题,明考向真题演练,课程标准,2掌握四个公式,针对训练,陌生图像综合考查,第二步找数据等内容,欢迎下载使用。
这是一份备战2025届新高考化学一轮总复习第7章化学反应速率与化学平衡第37讲化学反应的方向与调控课件,共46页。PPT课件主要包含了课标指引,目录索引,素养发展进阶,必备知识•梳理,无需外界帮助,混乱度,熵的变化,自发进行,关键能力•提升,增大反应物浓度等内容,欢迎下载使用。








