










所属成套资源:沪科版化学选择性必修一课件+练习+素材
高中化学沪科技版(2020)选择性必修1第2章 化学反应的方向、限度和速率2.4工业合成氨一等奖课件ppt
展开
这是一份高中化学沪科技版(2020)选择性必修1第2章 化学反应的方向、限度和速率2.4工业合成氨一等奖课件ppt,文件包含24工业合成氨同步课件pptx、24工业合成氨分层练习原卷版docx、24工业合成氨分层练习解析版docx、合成氨技术的发展历程mp4等4份课件配套教学资源,其中PPT共22页, 欢迎下载使用。
1.理解合成氨生产条件的选择;2.知道合成氨工业生产的主要步骤;3.体会化学理论对化工生产实践的指导作用。
合成氨工业是关系我国国民经济的重要行业,是我国化肥工业的基础,也是传统煤化工的重要组成部分。氨是重要的化工原料,主要用于制造氮肥、硝酸、丁腈橡胶等;氨在冶金、机械加工、电子、造纸等行业用途广泛。
一、合成氨适宜生产条件的选择
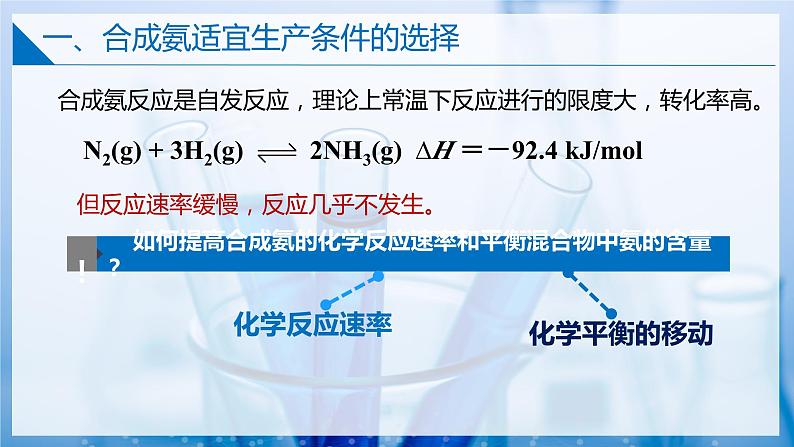
N2(g) + 3H2(g) 2NH3(g) ∆H =-92.4 kJ/ml
合成氨反应是自发反应,理论上常温下反应进行的限度大,转化率高。
但反应速率缓慢,反应几乎不发生。
合成氨反应为什么慢?
1. 从化学反应速率分析
如何增大合成氨的化学反应速率?
怎样降低反应的活化能?
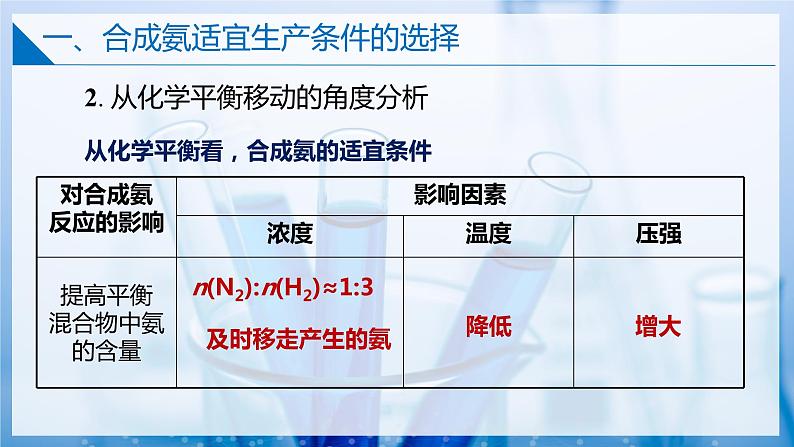
2. 从化学平衡移动的角度分析
n(N2):n(H2)≈1:3
从化学平衡看,合成氨的适宜条件
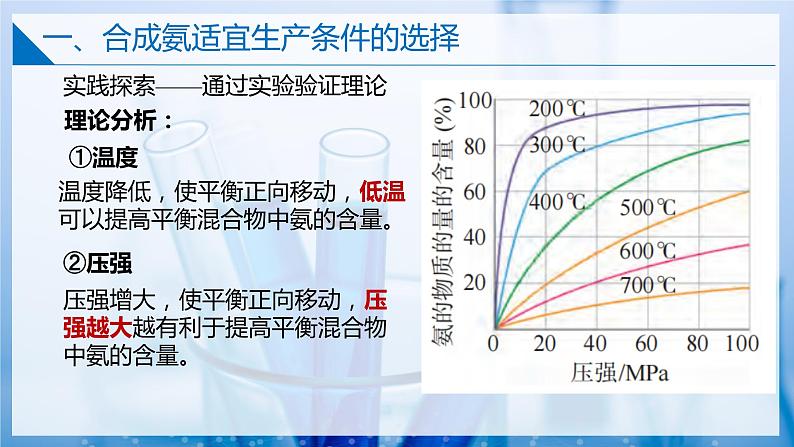
温度降低,使平衡正向移动,低温可以提高平衡混合物中氨的含量。
实践探索——通过实验验证理论
压强增大,使平衡正向移动,压强越大越有利于提高平衡混合物中氨的含量。
实现工业生产:综合考虑成本要低!
从化学反应速率与化学平衡考虑,都是压强越大越好。
综合动力、材料、设备等条件
20 MPa~50 MPa
合成氨工业要求催化剂具有活性强、机械强度高、不易中毒、容易制备、价格低廉等特点。
增大化学反应速率,不改变平衡混合物的组成。
目前公认的最适当的催化剂是以铁为主体的多成分催化剂。其活性最好的温度为500 ℃左右。
催化反应主要发生在催化剂的表面,因此,要提高催化效率、降低成本,增大催化剂的比表面积十分重要。
综合考虑,特别是考虑催化剂的活性。
一般选择在500 ℃左右
低温可以提高平衡混合物中氨的含量,但低温会减小化学反应速率。
所以实际生产中维持氢氮比为 2.8 ~ 2.9。
④反应物和生成物浓度
应将氨液化分离后的原料气循环使用,并及时补充氮气和氢气,使反应物保持一定的浓度,有利于合成氨反应。
从化学平衡角度讲,氢气和氮气的物质的量之比为 3:1 时,平衡混合物中氨的百分含量最大。
氮气在催化剂上的吸附活化是总反应中的控速步骤,适当提高氮气的浓度有利于合成氨反应的进行。
氢氮比为 2.8 ~ 2.9
工业合成氨常用的生产条件:
20 ~ 50 MPa
二、工业合成氨的生产流程
将空气液化、蒸发,分离出氮气
将空气中的O2跟碳作用生成CO2,再除去CO2
用水、煤、天然气、石油等为原料制得
在制取原料气的过程中,常混有一些杂质气体,其中如 H2S、CO 等杂质会使合成氨所用的催化剂中毒,所以必须除去。
加压后且达到催化剂的活性温度的 H2、N2
混合气体中氨含量为10% ~ 20%
合成氨反应为放热反应,可通过热交换器有效利用此反应热来预热反应前的 H2、N2,降低合成氨的成本。
例、在一定条件下,可逆反应N2(g)+3H2(g) 2NH3(g)(正反应是放热反应)达到平衡,当单独改变下列条件后,有关叙述错误的是( )A.加催化剂,v(正)、v(逆)都发生变化且变化的倍数相等B.加压,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数C.降温,v(正)、v(逆)都减小,且v(正)减小的倍数小于v(逆)减小的倍数D.等容条件下加入氩气,v(正)、v(逆)都增大,且v(正)增大的倍数大于v(逆)增大的倍数
一、合成氨适宜生产 条件的选择
压强温度催化剂反应物生成物浓度
1、有关合成氨工业的说法中,正确的是( )A.增大H2的浓度,可提高H2的转化率B.由于氨易液化,N2、H2在实际生产中会循环使用,所以总体来说氨的产率很高C.合成氨工业的反应温度控制在400~500 ℃,目的是使化学平衡向正反应方向移动D.合成氨厂采用的压强是10 MPa~30 MPa,因为该压强下铁触媒的活性最大
2、NH3是一种重要的工业原料。下列关于合成氨的说法中,不正确的是( )A.工艺涉及催化技术B.工艺涉及高温高压技术C.原料之一的氮气来自空气D.从合成塔出来的气体中,氨的体积分数为100%
相关课件
这是一份化学选择性必修1化学反应的方向精品ppt课件,文件包含21化学反应的方向同步课件pptx、21化学反应的方向分层练习原卷版docx、21化学反应的方向分层练习解析版docx等3份课件配套教学资源,其中PPT共25页, 欢迎下载使用。
这是一份高中化学沪科技版(2020)选择性必修1反应热的测量一等奖课件ppt,文件包含12反应热的测量和计算同步课件-pptx、12反应热的测量和计算分层练习-原卷版docx、12反应热的测量和计算分层练习-解析版docx、测定酸碱中和反应的热效应wmv等4份课件配套教学资源,其中PPT共34页, 欢迎下载使用。
这是一份高中鲁科版 (2019)第2章 化学反应的方向、 限度与速率第4节 化学反应条件的优化——工业合成氨说课ppt课件,共19页。PPT课件主要包含了合成氨反应的限度,合成氨反应的速率,使用铁作催化剂,铁催化剂,研究方向,合成氨的生产流程,练一练等内容,欢迎下载使用。










