






所属成套资源:高中化学人教版(2019)必修第一册精美课件多份
高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教学演示课件ppt
展开
这是一份高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教学演示课件ppt,共24页。PPT课件主要包含了思考与交流,如何配制,电子天平,怎么办到,容量瓶,①刻度线,②容积,③温度20℃,教材P54-55,使用注意事项等内容,欢迎下载使用。
【学习目标】1.掌握容量瓶的使用方法。2.掌握配制一定物质的量浓度溶液的方法及操作。3.掌握溶液配制中的误差分析。
1. 如何配制100克质量分数为20%的NaCl 溶液?
20g NaCl(s) + 80g 水,在烧杯中混合搅拌溶解就OK!
2.配制 100 mL 1.00 ml/L的NaCl 溶液,需要NaCl(s) 克?
需要称取5.85克NaCl(s) ,配成100ml的溶液
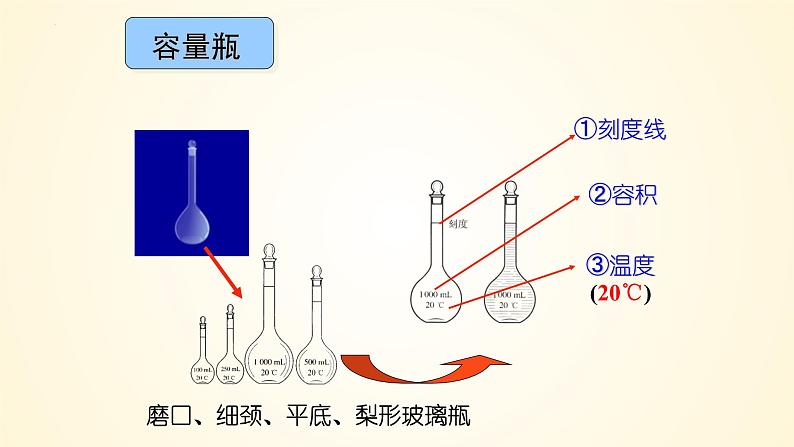
磨口、细颈、平底、梨形玻璃瓶
二. 一定物质的量浓度溶液的配制
2. 容量瓶上标有:温度(20℃)、容积、刻度线
a 选择与所配溶液体积相等或稍大的容量瓶。
c 使用前要检查是否漏水。
b 不能加热,不能久贮溶液,不能在瓶内溶解固体或稀释液体,不能用于化学反应。
常用有50ml、100 ml、200 ml、250 ml、500 ml、1000 ml等。
1. 用途:用于配制一定物质的量浓度的溶液
选用容量瓶一定要注明容积
不能加热、溶解、稀释、存放溶液、进行反应等
ml容量瓶
装水盖塞→倒立,观察→正立→玻璃塞旋转180°→倒立,再观察
3. 溶解,并冷却到室温
注意事项:(1)应在烧杯中溶解,不能在容量瓶中溶解(2)搅拌时用到了玻璃棒
[实验2-10] 配制 100 mL 1.00 ml/L的NaCl 溶液。
(一)用固体药品配制一定物质的量浓度的溶液
(为什么要恢复至室温?)
由于容量瓶瓶颈较细,为避免液体洒在外面,应用玻璃棒引流。
(100mL容量瓶、玻璃棒)
——溶液热胀冷缩,引起实验误差
且玻璃棒的着落点要在刻度线以下
:用少量蒸馏水洗涤烧杯和玻璃棒2~3次,洗涤液要全部转移到容量瓶中。
[P56 思考与讨论(1)]
(1)为什么要用蒸馏水洗涤烧杯内壁和玻璃棒2-3次,并将洗涤液也都注入容量瓶?
避免损失溶质,引起实验误差。
:向容量瓶中加入蒸馏水,在距离刻度线1~2cm时, 改用胶头滴管滴加蒸馏水至刻度线。
若凹液面超出刻度线,能否用胶头滴管将多出的溶液取出?
摇匀后发现液面低于刻度线,能否再滴加蒸馏水?
轻轻振荡,使溶液混合均匀
配制 100 mL 1.00 ml/L的NaCl 溶液
(玻璃棒引流,洗涤2-3次,转移)
(胶头滴管,平视凹液面)
下图是某同学用500 mL容量瓶配制0.10 ml·L-1 NaOH溶液的过程:
该同学的错误步骤有( ) A.1处 B.2处 C.3处 D.4处
第①步不能把NaOH放在纸上称量
第④步玻璃棒应接触容量瓶内壁刻度线以下的部分
第⑤步定容时应平视刻度线
2.实验中需要2 ml·L-1的Na2CO3溶液950 mL,配制时,你认为应该选用的容量瓶的规格和称取的碳酸钠质量分别是________、________。
1.将10.6 g Na2CO3·10H2O溶于水配成1 L溶液,物质的量浓度为0.1 ml/L,对吗?
Na2CO3·10H2O
3.若配制NaOH溶液,在称量时应注意什么?
注意:NaOH等吸湿性药品,必须放在小烧杯等玻璃器皿中称量。
称量时先称出空烧杯质量,再称烧杯与药品总质量。
4. 如何用密度为1.84g/ml、98%的浓硫酸配制0.5ml/L 480ml的稀硫酸?请简述步骤。
18.4 ml/L×Vml==0.5ml/L×500 ml
原理: 稀释前后溶质的量不变。
量取13.6ml 98%的浓硫酸
[要点:250ml烧杯;浓硫酸倒入水中]
[要点:500ml容量瓶;玻璃棒引流]
⑤洗涤(2-3次),洗涤液也转移到容量瓶;
轻轻振荡,使溶液混合均匀;
( 20ml量筒 胶头滴管)
问题:请按使用的先后顺序例举所用主要仪器
用浓溶液配制一定物质的量浓度的稀溶液
c(浓溶液)· V(浓溶液)= c(稀溶液)· V(稀溶液)
(3)稀释并冷却到室温
量筒、烧杯、玻璃棒、 ml容量瓶、胶头滴管
使用量筒时注意 (1) 读数时保留小数点后一位;
(2) 量取液体后量筒不用洗涤。
(5)洗涤(2-3次),洗涤液也转移到容量瓶;
并轻轻振荡,使溶液混合均匀
(若mB偏大,则CB偏大)
[若V(溶液)偏大,则CB偏小]
即,实验过程中造成溶质损失,则浓度偏小; 若引起V(溶液)增大,则浓度偏小
将NaOH(s)放在滤纸上称量
俯视或仰视刻度线对溶液浓度的影响
——仰小俯大(仅限定容时判断)
(2)定容时,往容量瓶中缓慢加蒸馏水,等液面离容量瓶刻度线1~2 mL时,改用胶头滴管滴加蒸馏水( )
1.正误判断,正确的划“√”,错误的划“×”(1)使用托盘天平称量药品,都不能直接放在托盘中,均应放两张相同的纸片( )
NaOH等腐蚀性药品放烧杯中称量
③配制NaOH溶液时,天平的两个托盘上放两张质量相等的纸片, 其他操作均正确_____。
②配制500 mL 0.1 ml/L的硫酸铜溶液,用托盘天平称取胆矾8.0 g____。
①配制450 mL 0.1 ml/L的NaOH溶液,用托盘天平称取NaOH固体1.8 g_____。
500 mL ×0.1 ml/L ×40g/ml
CuSO4·5H2O:
250g/ml×0.05ml=12.5g
解析: NaOH 会腐蚀性纸片,粘附在纸片上,造成损失
(1)从改变溶质的物质的量角度分析产生的误差(填“偏大”“偏小”或“无影响”)。
④配制一定物质的量浓度的NaOH溶液,需称量溶质4.4 g, 称量时物码放置颠倒______。
实际称量的NaOH固体质量为4 g-0.4 g=3.6 g。
⑤配制一定物质的量浓度的稀H2SO4溶液时,用量筒量取浓硫酸时,仰视读数:______。
结果:仰视时,容器内液面高于刻度线; 俯视时,容器内液面低于刻度线。
⑥定容时,加水超过刻度线,用胶头滴管吸取多余的液体至刻度线:______。
⑦配制一定物质的量浓度溶液时,烧杯及玻璃棒未洗涤:______。
相关课件
这是一份化学必修 第一册第三节 物质的量优秀ppt课件,共46页。PPT课件主要包含了实验误差分析等内容,欢迎下载使用。
这是一份人教版 (2019)第三节 物质的量授课课件ppt,共24页。PPT课件主要包含了思考与交流,如何配制,电子天平,怎么办到,容量瓶,①刻度线,②容积,③温度20℃,教材P54-55,使用注意事项等内容,欢迎下载使用。
这是一份人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯实验活动1 配制一定物质的量浓度的溶液课文内容ppt课件,共14页。PPT课件主要包含了玻璃棒,冷却至室温,~2cm,胶头滴管,洗涤液等内容,欢迎下载使用。










