




所属成套资源:人教版高一化学必修一同课件(含练习)
人教版 (2019)必修 第一册第一节 钠及其化合物课堂教学ppt课件
展开
这是一份人教版 (2019)必修 第一册第一节 钠及其化合物课堂教学ppt课件,文件包含第二章第一节微专题1Na2CO3与NaHCO3的相关计算pptx、第二章第一节微专题1Na2CO3与NaHCO3的相关计算教师版docx、第二章第一节微专题1Na2CO3与NaHCO3的相关计算学生版docx等3份课件配套教学资源,其中PPT共27页, 欢迎下载使用。
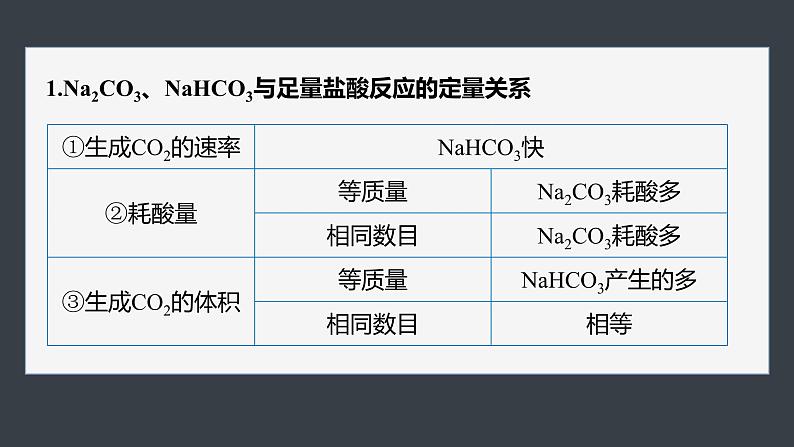
1.Na2CO3、NaHCO3与足量盐酸反应的定量关系
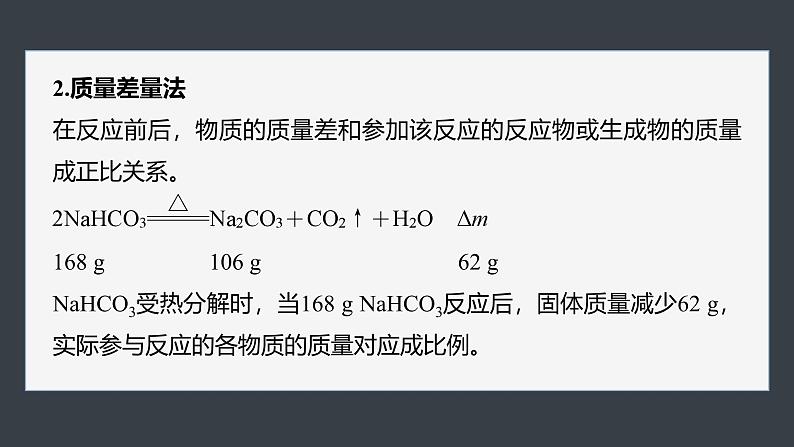
2.质量差量法在反应前后,物质的质量差和参加该反应的反应物或生成物的质量成正比关系。
168 g 106 g 62 gNaHCO3受热分解时,当168 g NaHCO3反应后,固体质量减少62 g,实际参与反应的各物质的质量对应成比例。
提示 根据化学方程式2NaHCO3 Na2CO3+CO2↑+H2O可知,168 g NaHCO3反应质量减少62 g,题中NaHCO3的质量减少3.1 g,因此NaHCO3分解8.4 g,所以NaHCO3分解百分率为 ×100%=50%。取反应后的固体少许加蒸馏水溶解,滴加氯化钡或氯化钙溶液,有白色沉淀产生,证明有碳酸钠固体生成。
【思考1】 如果将16.8 g NaHCO3加热一段时间,剩余固体为13.7 g,则NaHCO3的分解百分率为多少?如何检验有Na2CO3固体生成?
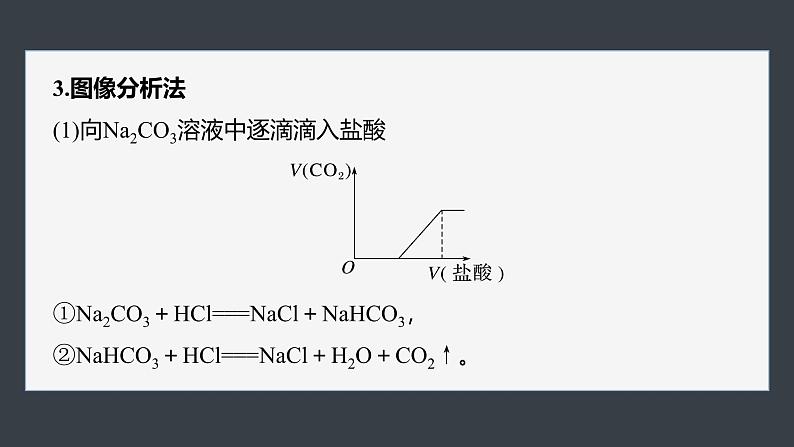
3.图像分析法(1)向Na2CO3溶液中逐滴滴入盐酸
①Na2CO3+HCl===NaCl+NaHCO3,②NaHCO3+HCl===NaCl+H2O+CO2↑。
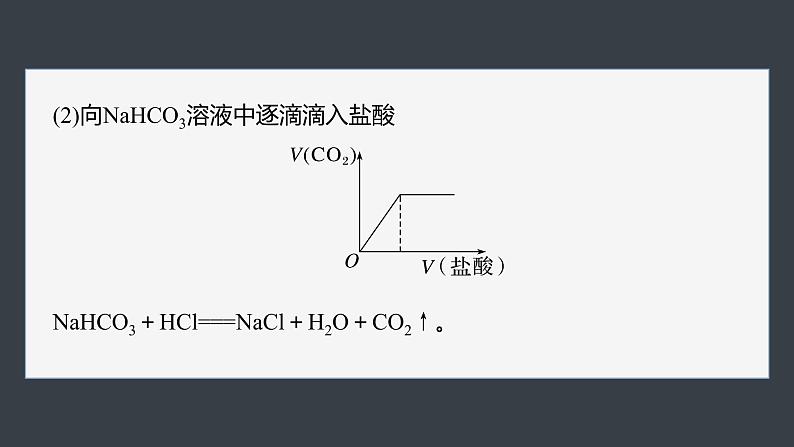
(2)向NaHCO3溶液中逐滴滴入盐酸
NaHCO3+HCl===NaCl+H2O+CO2↑。
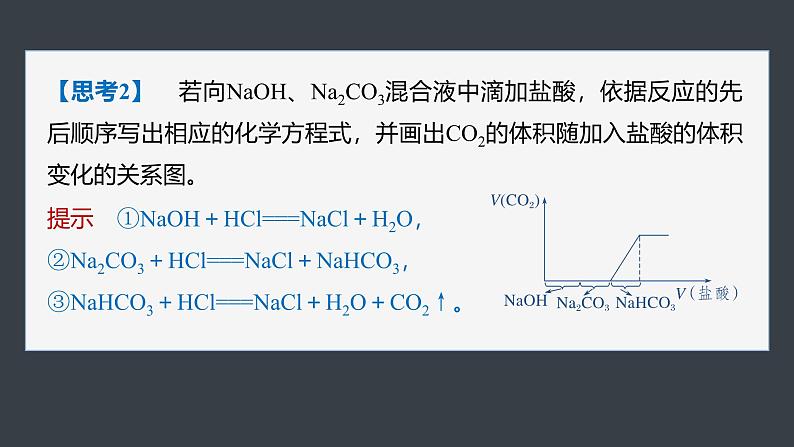
提示 ①NaOH+HCl===NaCl+H2O,②Na2CO3+HCl===NaCl+NaHCO3,③NaHCO3+HCl===NaCl+H2O+CO2↑。
【思考2】 若向NaOH、Na2CO3混合液中滴加盐酸,依据反应的先后顺序写出相应的化学方程式,并画出CO2的体积随加入盐酸的体积变化的关系图。
1.(2022·大同高一检测)把一定量的NaHCO3和Na2O2的混合物放在密闭容器中加热,关于混合物加热前后消耗的HCl的质量,下列判断正确的是A.加热前消耗的多B.加热后消耗的多C.加热前后消耗的一样多D.无法确定
2.加热5.00 g碳酸钠和碳酸氢钠的混合物,使碳酸氢钠完全分解,混合物质量减少了0.93 g,则原混合物中碳酸钠的质量为 g g g
3.有两份质量相同的NaHCO3,向第一份中加入盐酸使其充分反应;将第二份加热使其完全分解,冷却至原温度再加入相同浓度的盐酸,充分反应,则它们所耗用的盐酸的体积比为A.2∶1 B.1∶1C.1∶2 D.4∶1
4.把Na2CO3和NaHCO3的混合物27.4 g加热到质量不再变化时,得残留固体21.2 g。求原混合物中NaHCO3和Na2CO3的质量之比为A.53∶84 B.84∶53C.1∶1 D.42∶53
5.向NaOH和Na2CO3的混合溶液中滴加3.65 g·L-1的稀盐酸,生成的CO2的质量与加入盐酸的体积的关系如图所示。下列判断正确的是A.在O~a内,只发生酸碱中和反应B.ab段发生反应的离子方程式为 +2H+ ===H2O+CO2↑C.a=0.3D.原混合溶液中NaOH与Na2CO3的质量之比为1∶2
6.将一定体积的CO2通入一定浓度的NaOH溶液中,为了测定所得溶液的成分,向该溶液中逐滴加入盐酸,所加盐酸的体积与产生CO2的体积的关系如图所示:(1)所得溶液中的溶质为_______________。(2)OA段发生反应的离子方程式:____________________________________。AB段发生反应的离子方程式:_________________________。
NaOH、Na2CO3
7.有一含NaCl、Na2CO3·10H2O和NaHCO3的混合物,某同学设计如图所示的实验装置,通过测量反应产生的CO2和H2O的质量,来确定该混合物中各组分的质量分数。(1)实验步骤:①按图(夹持装置未画出)组装好实验装置后,首先进行的操作是________________。
②称取样品,并将其放入硬质玻璃管中;称量装浓硫酸的洗气瓶C的质量和装碱石灰的U形管D的质量。③打开弹簧夹K1、K2,关闭K3,缓缓鼓入空气数分钟,其目的是_______________________________。
④关闭弹簧夹K1、K2,打开K3,点燃酒精灯加热至不再产生气体。装置B中发生反应的化学方程式为______________________________________________________________________。
⑤打开弹簧夹K1,缓缓鼓入空气数分钟,然后拆下装置,再次称量洗气瓶C的质量和U形管D的质量。
(2)关于该实验方案,请回答下列问题。①若加热反应后不鼓入空气,对测定结果的影响是_____________________________________________________________________________。
Na2CO3·10H2O和NaHCO3的质量分数测定结果偏小,NaCl的质量分数测定结果偏大
②E处干燥管中盛放的药品是碱石灰,其作用是______________________________________________,如果实验中没有该装置,则会导致测得的NaHCO3的质量分数______(填“偏大”“偏小”或“无影响”)。
防止空气中的CO2和水
蒸气进入D中影响测定结果
③若样品质量为w g,反应后C、D装置增加的质量分别为m1 g、m2 g,则混合物中Na2CO3·10H2O的质量分数为____________________(用含w、m1、m2的代数式表示)。
相关课件
这是一份高中化学人教版 (2019)必修 第一册实验活动3 同周期、同主族元素性质的递变教学演示ppt课件,共13页。PPT课件主要包含了知识基础鉴别,答案C,答案B,NaHCO3,Na2CO3等内容,欢迎下载使用。
这是一份新高考化学一轮复习课件 第3章 第12讲 Na2CO3、NaHCO3 碱金属,共60页。PPT课件主要包含了高考化学一轮复习策略,归纳整合,专项突破,碱金属焰色试验,真题演练明确考向,课时精练等内容,欢迎下载使用。
这是一份高中化学苏教版 (2019)选择性必修1第二单元 化学能与电能的转化优秀课件ppt,共37页。PPT课件主要包含了常用解题步骤,阳极产物,阴极产物,原电池,电解池,+O2↑等内容,欢迎下载使用。









