









化学整理与提升集体备课课件ppt
展开一、氯气的性质及应用1.(2022·重庆南开中学高一月考)生活中难免会遇到一些突发事件,我们要善于利用学过的知识,采取科学、有效的方法保护自己。如果发生了氯气泄漏,以下自救得当的是A.用沾小苏打水的毛巾捂住口鼻撤退B.向地势低的地方撤离C.观察风向,顺风撤离D.在室内放一盆水
2.下列与氯气有关的说法正确的是A.氯气在化学反应中只能作氧化剂B.干燥的氯气不能使有色鲜花褪色C.氯气杀菌消毒时没有发生化学变化D.氯气没有漂白性,但通入品红溶液中,品红溶液褪色
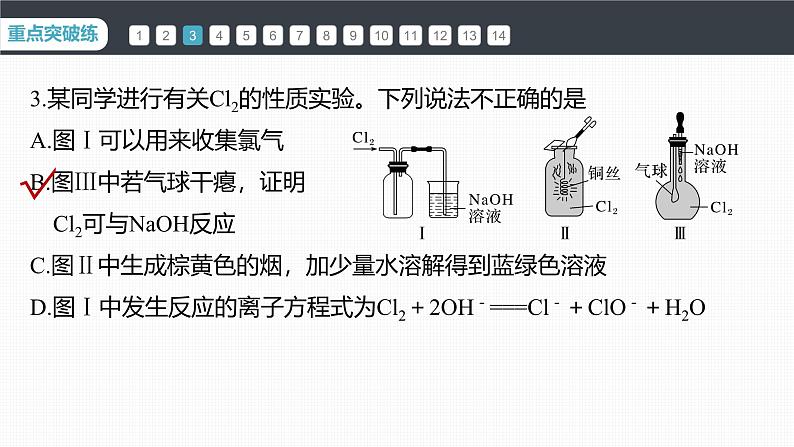
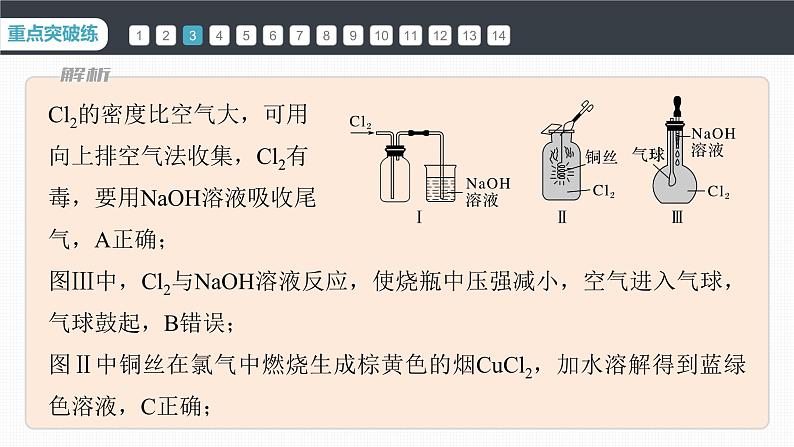
3.某同学进行有关Cl2的性质实验。下列说法不正确的是A.图Ⅰ可以用来收集氯气B.图Ⅲ中若气球干瘪,证明 Cl2可与NaOH反应C.图Ⅱ中生成棕黄色的烟,加少量水溶解得到蓝绿色溶液D.图Ⅰ中发生反应的离子方程式为Cl2+2OH-===Cl-+ClO-+H2O
4.无水三氯化铁(FeCl3)是一种重要的有机合成催化剂,利用如图装置可制备。已知:①FeCl3具有强烈的吸水性,能吸收空气中的水分而潮解;②FeCl3在100 ℃左右易升华。下列说法不正确的是A.A中浓硫酸的作用是干燥Cl2B.B中硬质玻璃管内发生反应的化学方程式为3Cl2+2Fe 2FeCl3C.实验时可观察到硬质玻璃管中产生蓝色的烟雾,铁粉逐渐减少D.C中冷水的作用是冷凝FeCl3
二、氯水和次氯酸的性质5.(2023·湖南株洲高一质检)现有盐酸、NaCl溶液、NaOH溶液和新制氯水,可用来区别它们的一种试剂是A.AgNO3溶液B.紫色石蕊溶液C.酚酞溶液D.饱和食盐水
6.“氯气对水一心一意,水偏弄成三分四离”其中“三分四离”指的是新制氯水中的七种微粒。下列实验现象和结论一致的是A.新制氯水使紫色石蕊溶液先变红后褪色,说明有氯气分子和H+存在B.向新制氯水中加入饱和NaHCO3溶液,有无色气体产生,说明有HClO 存在C.向新制氯水中加入饱和NaHCO3溶液,有无色气体产生,说明氯气和 水反应生成了HClD.向新制氯水中加入NaOH溶液,氯水黄绿色消失,说明氯水中的氯气 分子与氢氧化钠直接反应
7.光照装有氯水的广口瓶,测定氧气的体积分数随时间变化如图,下列关于氯水光照过程的说法正确的是A.H+的数目增大B.Cl-的数目减小C.颜色变深D.漂白性变强
三、氯气的实验室制法及相关应用8.实验室利用如图所示的装置制备干燥、纯净的氯气。下列有关叙述不正确的是A.本实验操作顺序为检验装置气 密性→添加固体药品→添加液 体药品→加热B.装置Ⅱ、Ⅲ中的试剂依次为饱和NaCl溶液、浓硫酸C.氯气密度比空气大,故装置Ⅳ中短导管进气,长导管出气D.装置Ⅴ中反应的离子方程式为Cl2+2OH-===Cl-+ClO-+H2O
9.(2022·成都高一月考)某化学兴趣小组模拟设计了如下的实验装置(夹持仪器已略去)。下列说法错误的是A.当三颈烧瓶中充满黄绿色气体时, 把d中的H2O加入三颈烧瓶,发现 红色布条颜色褪去B.干燥管c中无水CaCl2的作用是干燥氯气和除去挥发的HCl,可以用碱石灰代 替固体CaCl2C.拆除装置前,把f中NaOH溶液加入三颈烧瓶中可以消除余氯对环境的影响D.已知2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,该反应中浓 盐酸体现还原性和酸性的个数之比为5∶3
四、氯及其化合物的性质及综合应用10.已知反应Ca(ClO)2+4HCl===CaCl2+2Cl2↑+2H2O,下列说法错误的是A.Ca(ClO)2是漂白粉的有效成分B.HCl是还原剂C.生成1个Cl2分子转移2个电子D.Cl2既是氧化产物又是还原产物
11.(2022·广州期末)部分常见含氯物质的分类与相应化合价关系如图所示。下列反应路径不合理的是A.a+碱→b+cB.b+c+H+→aC.不存在a→c→e→d→b→a的循环转化关系D.d→b或e→c可通过复分解反应实现
12.用久置于空气中的生石灰[主要成分为CaO,还含有Ca(OH)2和CaCO3]制取KClO3的流程如图所示。下列有关说法不正确的是A.“打浆”的目的是为了提 高“氯化”时的反应速率B.“氯化”中主要发生的反 应为6Cl2+6Ca(OH)2 Ca(ClO3)2+5CaCl2+6H2OC.“过滤”后的滤渣中含有CaCO3D.“转化”时发生的化学反应Ca(ClO3)2+2KCl===CaCl2+2KClO3属于氧 化还原反应
13.漂白粉是一种常用杀菌、消毒剂,其有效成分为次氯酸钙。如图为制取漂白粉的工业流程简图。(1)流程Ⅱ的反应条件(2)是______。
(2)流程Ⅲ中发生两个反应,写出其中一个氧化还原反应的化学方程式:________________________________________。
2Cl2+2Ca(OH)2===Ca(ClO)2+CaCl2+2H2O
(3)流程Ⅳ中操作b是________(写名称)。
(4)用化学方程式说明较纯的次氯酸钙粉末必须密封保存的原因:___________________________________________________________。
14.某实验小组制取“84”消毒液(主要成分为NaClO)并探究其性质。[查阅资料]①常温下:16HCl(浓)+2KMnO4===2MnCl2+8H2O+2KCl+5Cl2↑;②苯为有机物,密度比水小且不溶于水;③氯、溴、碘的单质均易溶于有机溶剂。Ⅰ.制取NaClO的装置如图1所示(夹持装置略):
(1)仪器a的名称为__________。(2)装置B中发生反应的化学方程式为________________________________。
Cl2+2NaOH===NaCl+NaClO+H2O
(3)右述装置存在一个缺陷,会导致“84”消毒液的产率降低,改进的方法是___________________________________________。
在A、B之间安装一个装有
Ⅱ.探究“84”消毒液的性质:(4)为验证“84”消毒液的某些性质,实验小组设计图2实验方案。观察到试管1中溶液不褪色;试管2中溶液变蓝,短时间内无明显现象;试管3中溶液先变蓝,通入CO2后,溶液快速褪色。①试管1的作用是____________。
②由试管2、3的现象可得到的结论是______________________________________________________。
NaClO溶液呈碱性且能与酸反应,生成的HClO具有漂白性
③若将试管3中通入的CO2换成盐酸也可达到相同的效果,且速度更快,但有可能产生Cl2而带来不良的实验后果,试写出产生Cl2的化学方程式:_________________________________。
NaClO+2HCl===NaCl+Cl2↑+H2O
苏教版 (2019)必修 第二册专题9 金属与人类文明本单元综合与测试优质课件ppt: 这是一份苏教版 (2019)必修 第二册专题9 金属与人类文明本单元综合与测试优质课件ppt,共51页。PPT课件主要包含了节约金属资源,x=336t,氧化剂,或假设b成立,HCl,FeOH2,最后变为红褐色,ADECB,玻璃棒,溶液变成血红色等内容,欢迎下载使用。
苏教版 (2019)必修 第二册专题8 有机化合物的获得与应用本单元综合与测试一等奖ppt课件: 这是一份苏教版 (2019)必修 第二册专题8 有机化合物的获得与应用本单元综合与测试一等奖ppt课件,共53页。PPT课件主要包含了乙和丙,+CH3CH2OH,+H2O,+CH3OH,C6H12O6,新制的氢氧化铜悬浊液,银氨溶液或,溶液变蓝,高级脂肪酸,提高反应的产率等内容,欢迎下载使用。
苏教版 (2019)必修 第二册专题7 氮与社会可持续发展本单元综合与测试优质课件ppt: 这是一份苏教版 (2019)必修 第二册专题7 氮与社会可持续发展本单元综合与测试优质课件ppt,共53页。PPT课件主要包含了+2NH3↑,无色气体变成红棕色,+2H2O,将KI氧化为I2,NH3,+6H2O,酸性和氧化性等内容,欢迎下载使用。













