



人教版九上化学第四单元课时2化合价课件
展开
这是一份人教版九上化学第四单元课时2化合价课件,共31页。
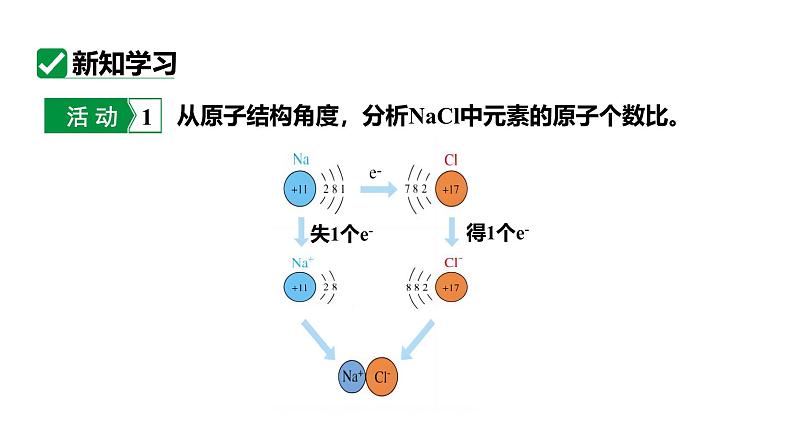
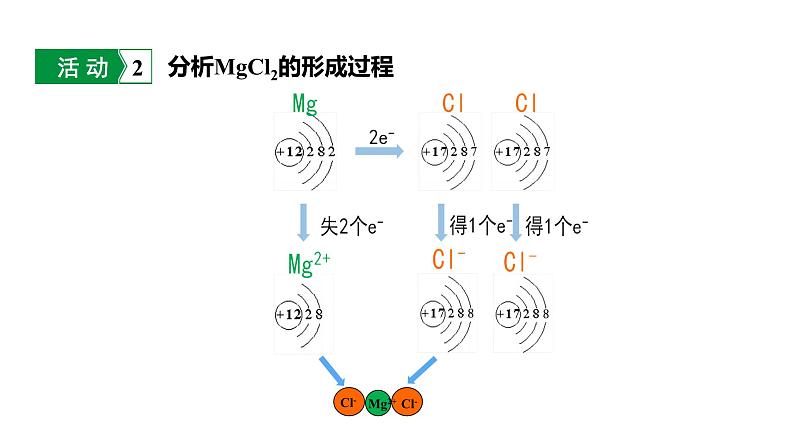
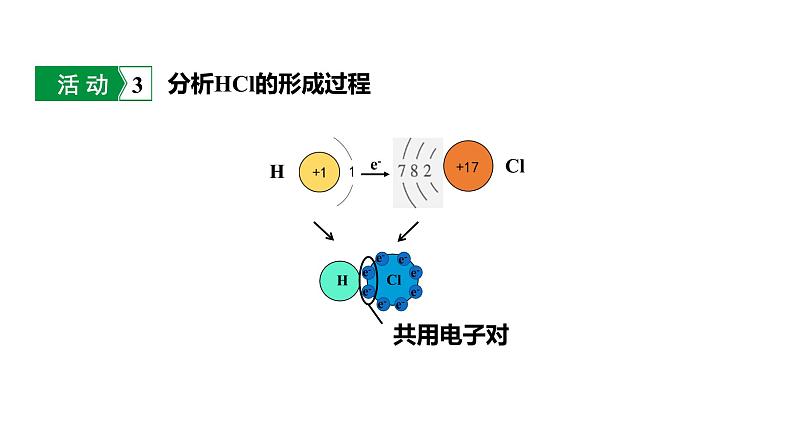
课时2 化合价九上 化学 人教版学习目标新课引入新知学习课堂小结1. 通过对氯化钠、氯化镁、氯化氢形成过程的认识,解释化合物中原子个数比不同的原因,了解化合价的本质,培养从微观视角来解释宏观事物的思想和方法2. 通过分析典型物质的化合价,了解化合价的表示方法,认识化合价的一般规律3. 通过典型试题练习,学会应用化合价解决化学问题观察下列物质中的原子个数比,你发现了什么?从原子结构角度,分析NaCl中元素的原子个数比。分析MgCl2的形成过程分析HCl的形成过程 不同原子最外层电子数不同,它达到稳定结构时得失电子(电子对偏移)的数目也不同,所以形成的化合物中,原子个数比不同。解释化合物中原子个数比不同的原因氯化钠中钠元素为+1价氯元素为-1价确定元素的化合价确定元素的化合价氯化镁中镁元素为+2价氯元素为-1价确定元素的化合价氯化氢中氢元素为+1价氯元素为-1价确定元素的化合价化合价的表示方法1. 写在元素符号的正上方。2. “+”、“-”符号在前,数值在后。3. “1”不能省略。例如:NaCl H2O+1-1+1-2化合价与离子符号的区别与联系 同种元素(或原子团)的化合价和离子所带的电荷,通常数值相等,正、负号相同,只是位置不同,正负号与数值的书写顺序不同,数值为“1”时,是否省略不同,即“两同三异”。常见元素的化合价根Ca(OH)2 CaCO3 Cu(NO3)2 BaSO4 Fe(OH)3 在这些化学式中有一些带电的原子团,如OH-、 、 、 ,它们也叫做根。带电的原子团常作为一个整体出现,根也有化合价。OH-OH-常见根的化合价常见元素的化合价口诀一价钾钠氯氢银,二价氧钙钡镁锌;三铝四硅五价磷,二三铁、二四碳;二四六硫都齐全,铜汞二价最常见;氢一氧二为标准,单质元素永为零。化合价的一般规律:1.化合价有正、有负。2.在化合物里,正负化合价的代数和为零。Na2CO3 BaCl2 ZnSO4 NaOH CuSO4+1+1-2-2-2+2+2+2-1-13.同种元素在不同物质中可显不同的化合价,在同一物质中也可能显不同的化合价。SO2 SO3 NH4NO3 -2-2+6+4-3+54.金属元素和非金属元素化合时,金属元素显正价,非金属元素显负价。5.在单质里,元素的化合价为0。6.在化合物里,氧元素通常显-2价,氢元素通常显+1价。NaCl CaCl2 AlCl3 KCl MgCl2 +1-1+1-1-1-1-1+2+2+3HCl H2S H2O +1+1-1-2+1-2化合价的一般规律: (1)已知磷的某种氧化物中,磷为+5价,氧为-2价,写出这种磷的氧化物的化学式。依据正负化合价代数和为0,求出各原子数目。十字交叉法:【思路】①先写元素符号(正前负后)②标出各元素的化合价(正上方)③把化合价数值化为最简整数比④把化简后的数字交叉写出⑤写出这种化合物的化学式【示例】Al OAl2O3 (2)写出氧化铝的化学式。(3)写出氢氧化钙的化学式。原子团数目不为1时,需用括号把原子团括起来。+2 -1例:求氯酸钾(KClO3)中氯元素的化合价。解:设氯元素的化合价为x,则(+1)+ x +(-2)×3 = 0 x = +5所以,在氯酸钾中,氯元素的化合价为+5。若求原子团中某元素的化合价,则代数和不为零。例:已知Na2FeO4中铁元素的化合价为+6,判断该化学式是否正确,具体步骤如下。①写出要判断的化学式,并标出元素(或原子团)的化合价: Na2FeO4+1 +6 -2②计算正负化合价代数和是否为零:(+1)×2+(+6)×1+(-2)×4=0③计算结果为0,则化学式书写正确(若计算结果不为0,则化学式书写错误)。判断未知元素化合价正、负号,数字原子最外层电子数不同 化合价表示规律元素应用得失电子共用电子对偏移书写化学式标在元素正上方正、负化合价代数和为零元素化合价有正价、负价……性质判断化学式的正误1.钼是组成眼睛虹膜的元素之一,虹膜可调节瞳孔大小,控制进入眼球内的光线。 Na2MoO4是 Mo元素的重要化合物,其中 Mo元素的化合价是( )A. +4 B. +5 C. +6 D. +7C(+1)×2 + x + (-2)×4 = 0 2. 某团队研究证明了 离子能够稳定存在(Pt是铂的元素符号),已知该离子中氧元素显 -2 价,则该离子中铂元素的化合价为( )A. +2 B. +4 C. +8 D. +10D x + (-2)×4 = +2 3. (2022济宁)下列四组物质中,同一种元素的化合价都相同的是( )A. NO2、 N2O4 B. Na2O、Na2O2C. Fe(OH)2、Fe(OH)3 D. KClO3、KClO44.厨房中的加碘盐含有KIO3,碘元素的化合价为________,该价态的碘元素形成的氧化物化学式为________。A+5I2O5+4 -2 +4 -2+1 -2 +1 -1+2 -2 +1 +3 -2 +1+1 +5 -2 +1 +7 -25. (2022山西)元素的化合价不同,组成的物质也多种多样。在下列纯净物中,化学式书写及元素的化合价标注均正确的是( )A. N2 B. CaCl2 C. KHO D. P5O20+1+1-2A对应巩固练习见《基础题与中考新考法》






