






化学必修 第一册第一节 钠及其化合物评课ppt课件
展开【研究目的】纯碱是一种重要的化工原料,具有广泛的用途。通过查阅资料,了解纯碱的生产历史,感受化学工业发展过程中技术进步的重要性,以及建设生态文明的意义。
(2)制取方法评价路布兰制取纯碱,主要生产过程在固相中进行,难以连续生产,又需硫酸做原料,设备腐蚀严重,产品质量不纯,原料利用不充分,价格较贵,所以在20世纪20年代被淘汰。
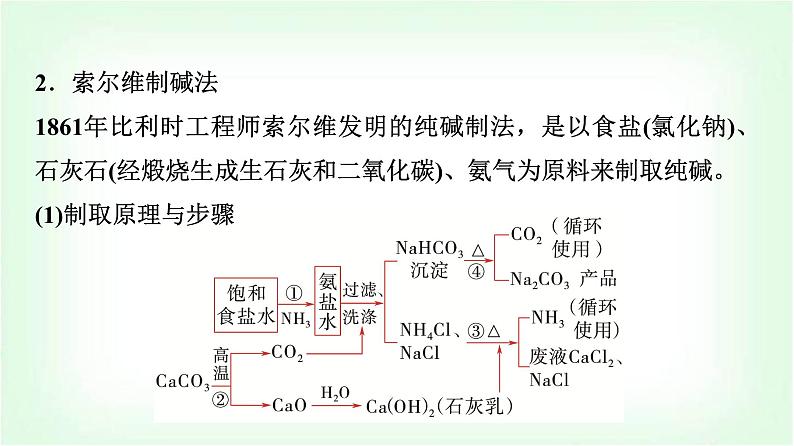
2.索尔维制碱法1861年比利时工程师索尔维发明的纯碱制法,是以食盐(氯化钠)、石灰石(经煅烧生成生石灰和二氧化碳)、氨气为原料来制取纯碱。(1)制取原理与步骤
(2)制取方法评价此法食盐利用率比路布兰制碱法高,产品较纯净,成本低。缺点:原料中一半成分未能转化为产品。
3.侯氏制碱法1943年我国化学工业科学家侯德榜发明创建了联合制碱法,即将氨碱法(又称索尔维制碱法)和合成氨法两种工艺联合起来,同时生产纯碱和氯化铵两种产品的方法。原料是食盐、氨和二氧化碳,二氧化碳为合成氨厂用水煤气制取氢气时的废气。(1)制取原理与步骤
(2)制取方法评价①符合现在提倡的“绿色化学的要求”,提高了原料(NaCl)的利用率,不产生无用的CaCl2。②利用了大规模联合生产的优越性,利用一个厂的废料,作为另一个厂的主要原料。如合成氨厂的废料CO2可以作为碱厂的主要原料;碱厂无用的Cl-可以代替价格比较昂贵的硫酸用来固定氨,制成氮肥,降低了成本,提高了综合经济效益。
【结果与讨论】1.根据以上研究分析后一种制碱法与前一种制碱法相比所具有的优势是什么?
提示:索尔维制碱法相比于路布兰制碱法的优点是原料(食盐和石灰石)便宜;产品纯碱的纯度高;副产品氨和二氧化碳都可以回收循环使用;制造步骤简单,适合于大规模生产。侯氏制碱法与索尔维制碱法相比较,其优点是食盐的利用率大大提高,用等量的食盐可生产更多的纯碱,同时得到氮肥氯化铵,不再产生废渣氯化钙,减少了对环境的污染,并且大大降低了纯碱和氮肥的成本,充分体现了大规模联合生产的优越性。
2.从生态文明建设的角度,思考侯氏制碱法的意义。
提示:减少了对环境的污染,有助于环境保护和生态文明建设,原料利用率高,产率高,降低了成本,减少了资源的浪费和能源的消耗。
【实践训练】1.实验室模拟侯氏制碱法制备少量纯碱,下列实验装置和操作能达到实验目的的是( )A.用甲装置制取CO2B.用乙装置先通CO2,再通NH3制备NaHCO3C.用丙装置过滤并洗涤NaHCO3D.用丁装置加热NaHCO3制备Na2CO3
C [稀硫酸和碳酸钙反应会生成硫酸钙,而硫酸钙微溶于水,会附着在碳酸钙表面,阻止反应的继续进行,无法得到足够的二氧化碳,反应会逐渐停止,A错误;由于CO2 在水中的溶解度小,而氨气极易溶于水,因此先通入氨气使溶液呈碱性,然后再通入CO2 ,B错误;NaHCO3在冷水中的溶解度较小,可以用冷的蒸馏水洗涤NaHCO3,C正确;加热NaHCO3制备Na2CO3应该在坩埚中进行,D错误。]
2.我国化学家侯德榜创立了著名的“侯氏制碱法”(流程简图如图所示),促进了世界制碱技术的发展。下列有关说法不正确的是( )A.操作a是过滤B.图中X可能是氨气C.母液的主要成分是NH4Cl,可用于化肥工业D.通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收,更多地析出沉淀
3.“索尔维制碱法”工艺流程如图所示,请回答下列问题:
(1)向饱和氯化钠溶液中先通入________,效果更好。反应制得NaHCO3沉淀和NH4Cl溶液的化学方程式为______________________________________________________。
NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl
(2)索尔维制碱法除了得到纯碱外,还会产生一种废渣________。侯氏制碱法在此工艺上改进,不再使用碳酸钙制备CO2,而是在制备NH3的过程中制得CO2,则侯氏制碱法在得到纯碱的同时还制得了________,此物质在农业上的用途是________。
[解析] (1)由于氨气极易溶于水,所以向饱和NaCl溶液中先通入氨气,效果更好。反应制得NaHCO3沉淀和NH4Cl溶液的化学方程式为NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl。(2)根据原子守恒可知反应过程中还有氯化钙生成。根据化学方程式NaCl+NH3+CO2+H2O===NaHCO3↓+NH4Cl可知,侯氏制碱法在得到纯碱的同时还制得氯化铵,铵盐在农业上可作氮肥。
4.我国化学家侯德榜发明的“联合制碱法”为世界制碱工业做出了巨大贡献。Ⅰ.如图为联合制碱法的主要过程(部分物质已略去):
(1)①~③的涉及的操作方法中,包含过滤的是________(填序号)。(2)根据上述流程图,将化学方程式补充完整。NH3+CO2+________+________===NaHCO3+NH4Cl。(3)煅烧NaHCO3固体的化学方程式是______________________________________________。(4)上述联合制碱法流程可以循环使用的中一种物质是________(填化学式)。
Ⅱ.某小组利用下列装置对Na2CO3和NaHCO3的性质进行探究,(夹持装置已略去,气密性已检查)。
(5)方框中为洗气装置,请将该装置图补充完整________。(6)试剂a为饱和NaHCO3溶液,其作用是______________________________________________________________。(7)实验持续一段时间后,观察到饱和Na2CO3溶液中有细小晶体析出,用化学方程式表示产生细小晶体的原因_______________________________________________________________________。
+H2O===2NaHCO3↓
[解析] Ⅰ.向饱和食盐水依次通入氨气、二氧化碳气体发生反应生成碳酸氢钠晶体和氯化铵,过滤得到的碳酸氢钠固体加热分解生成碳酸钠,溶液A中加入氯化钠析出氯化铵晶体,过滤得到氯化铵晶体和溶液B(主要为氯化钠、氯化铵等)。(1)过滤是分离固体和液体的操作,分析可知①~③所涉及的操作方法中,包含过滤的是①③。
(2)氨化的饱和食盐水中通入二氧化碳生成碳酸氢钠和氯化铵,反应的化学方程式:NH3+CO2+NaCl+H2O===NaHCO3↓+NH4Cl。(3)碳酸氢钠受热分解生成碳酸钠、二氧化碳和水。(4)开始通入二氧化碳参加反应,最后碳酸氢钠受热分解生成的CO2可循环使用。
人教版 (2019)必修 第一册第一节 钠及其化合物授课ppt课件: 这是一份人教版 (2019)必修 第一册<a href="/hx/tb_c161979_t3/?tag_id=26" target="_blank">第一节 钠及其化合物授课ppt课件</a>,文件包含第二章第一节研究与实践1了解纯碱的生产历史pptx、第二章第一节研究与实践1了解纯碱的生产历史教师版docx、第二章第一节研究与实践1了解纯碱的生产历史学生版docx等3份课件配套教学资源,其中PPT共28页, 欢迎下载使用。
人教版高中化学必修第一册研究与实践导学案+课件: 这是一份人教版高中化学必修第一册研究与实践导学案+课件,文件包含研究与实践1了解纯碱的生产历史pptx、研究与实践3认识元素周期表pptx、研究与实践2检验食品中的铁元素pptx、研究与实践1了解纯碱的生产历史DOCX、研究与实践3认识元素周期表docx、研究与实践2检验食品中的铁元素docx等6份课件配套教学资源,其中PPT共49页, 欢迎下载使用。
人教版 (2019)必修 第二册第七章 有机化合物实验活动8 搭建球棍模型认识有机化合物分子结构的特点多媒体教学课件ppt: 这是一份人教版 (2019)必修 第二册第七章 有机化合物实验活动8 搭建球棍模型认识有机化合物分子结构的特点多媒体教学课件ppt,共16页。













