






所属成套资源:【核心素养目标】人教版 化学选择性必修一授课课件
选择性必修1第一节 电离平衡试讲课课件ppt
展开
这是一份选择性必修1第一节 电离平衡试讲课课件ppt,共20页。PPT课件主要包含了学习目标,素养目标,情境引入,教学过程,电离平衡常数,表达式,1一元弱酸酸碱,2多元弱酸酸碱,影响因素,电离度等内容,欢迎下载使用。
1.了解电离平衡常数的含义。2.掌握电离平衡常数的有关应用和计算。
1.通过对电离平衡常数的理解,培养学生“变化观念与平衡思想”的学科素养。2.通过电离平衡常数的计算,培养学生“证据推理与和模型认知”的学科素养。
甲酸(HCOOH)又称蚁酸,酸性很强,有腐蚀性,能刺激皮肤出现红肿。甲酸存在手某些蚁类和毛虫的分泌物中。
从电离平衡的角度分析皮肤被蚂蚁、毛虫叮咬后出现红肿的原因。
已知人体血液中存在如下平衡:
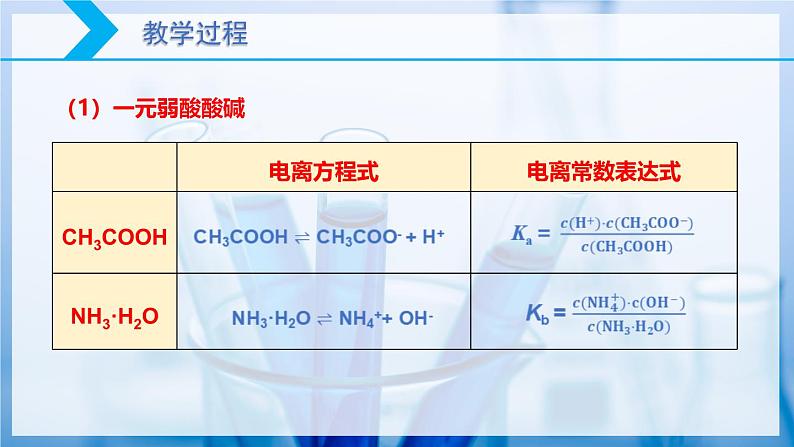
1.概念:在一定条件下,当弱电解质的电离达到平衡时,溶液中弱电解质电离所生成的各种离子浓度的乘积,与溶液中未电离分子的浓度之比是一个常数,这个常数叫做电离平衡常数,简称电离常数,用 K 表示。
一般多元弱酸各步电离常数的大小为Ka1≫Ka2≫Ka3,因此,多元弱酸的酸性主要由第一步电离决定。 由于多元弱碱为难溶碱,所以一般不用电离平衡常数,而用以后要学到的难溶物的溶度积常数。
电离平衡常数表示弱电解质的电离能力。一定温度下,K值越大,弱电解质的电离程度越大,酸性(或碱性)越强。
酸性:HCOOH > HNO2>HF > CH3COOH> HClO > HCN
(1)内因:弱电解质本身的性质。(2)外因:电离平衡常数只跟温度有关,温度升高,电离平衡常数增大。
电离是吸热的,升高温度,平衡正向移动,电离常数 K 增大。
(1)判断弱酸(或弱碱)的相对强弱,电离平衡常数越大,酸性(或碱性)越强。 (2)判断复分解反应能否发生,一般符合“强酸制弱酸”规律。 (3)判断溶液中微粒浓度比值的变化。如加水稀释醋酸溶液,由 不变,稀释后c(CH3COO-)减小,则(c(H+)/c(CH3COOH)增大。
应用:判断复分解反应能否发生,一般符合“强酸制弱酸”规律
实验:向盛有2 mL 1 ml/L 醋酸的试管中滴加1 ml/L Na2CO3溶液,观察现象。你能否由此推测Ka(CH3COOH)与Ka1(H2CO3)的大小关系?
CH3COOH > H2CO3
Ka(CH3COOH) > Ka1(H2CO3)
1. 概念:弱电解质达电离平衡时,已电离的电解质分子数占原来总分子数(包括已电离的和未电离的)的百分数。2. 影响因素①内因:弱电解质本身的性质②外因:温度及浓度3. 意义:表示不同弱电解质在水溶液中的电离程度,在相等条件下可用电离度比较弱电解质的相对强弱。
三、电离常数的计算1. 列出“三段式”计算2. 由于弱电解质的电离程度比较小,最终计算时,一般弱电解质的平衡浓度≈起始浓度(即忽略弱电解质电离的部分)。
电离平衡常数计算题思维模型
某温度下,氨水的浓度为 2.0 ml·L–1 , 达到电离平衡时,已电离的NH3·H2O 为1.7×10-3 ml·L–1 。计算该温度下的电离平衡常数。
【答案】A【解析】电离平衡常数K是温度的函数,所以B错。只要温度一定,不同浓度的同一弱电解质电离平衡常数K相同,所以C错。多元弱酸各步电离平衡常数相互关系应为K1>K2>K3,所以D错。
下列关于电离平衡常数(K)的说法中正确的是( )A.组成相似时电离平衡常数(K)越小,表示弱电解质电离能力越弱B.电离平衡常数(K)与温度无关C.不同浓度的同一弱电解质,其电离平衡常数(K)不同D.多元弱酸各步电离平衡常数相互关系为K1HCN,由此可判断:Ka(HF)>Ka(HNO2)>Ka(HCN),其对应数据依次为Ka(HF)=6.3×10-4、Ka(HNO2)=5.6×10-4、Ka(HCN)=6.2×10-10。
已知下面三个数据:6.3×10-4、5.6×10-4、6.2×10-10分别是下列有关的三种酸的电离常数,若已知下列反应可以发生:NaCN+HNO2=HCN+NaNO2;NaNO2+HF=HNO2+NaF。由此可判断下列叙述不正确的是( )A.Ka(HF)=6.3×10-4B.Ka(HNO2)=6.2×10-10C.三种酸的强弱顺序为HF>HNO2>HCND.Ka(HCN)NaHCO3C.向Na2CO3溶液中加入足量HX,反应的离子方程式:HX+CO32-=HCO3-+X-D.HX溶液中c(H+)一定比HY溶液的大
【答案】C【解析】B项,Ka越小,酸越弱,水解程度越大,碱性越强,即NaY>Na2CO3>NaX>NaHCO3,错误;D项,没有指明溶液浓度,无法比较c(H+),错误。
相关课件
这是一份人教版 (2019)选择性必修1第二节 水的电离和溶液的pH试讲课课件ppt,共18页。PPT课件主要包含了学习目标,素养目标,情境引入,教学过程,总结归纳,课堂练习,课堂小结等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第一节 电离平衡获奖ppt课件,共22页。PPT课件主要包含了学习目标,素养目标,情境引入,教学过程,实验探究,实验操作,实验视频,小pH1,大pH≈3,实验现象及结论等内容,欢迎下载使用。
这是一份化学选择性必修1第二节 化学平衡完整版ppt课件,共20页。PPT课件主要包含了学习目标,素养目标,情境引入,化学平衡常数,教学过程,课堂练习,K22,K12K2,浓度熵等内容,欢迎下载使用。










