










所属成套资源:苏教版化学必修一课件+分层练习+实验视频
苏教版 (2019)必修 第一册第一单元 氯气及氯的化合物课前预习ppt课件
展开
这是一份苏教版 (2019)必修 第一册第一单元 氯气及氯的化合物课前预习ppt课件,文件包含311氯气的发现与制备同步课件pptx、311氯气的发现与制备分层练习原卷版docx、311氯气的发现与制备分层练习解析版docx、02-氯化钠溶液的电解mp4、1-舍勒发现氯气的电影片段-480P清晰-AVCmp4、氯气的实验室制取wmv等6份课件配套教学资源,其中PPT共29页, 欢迎下载使用。
1.了解氯气的发现史,掌握实验室制取氯气的方法,通过分析、推理,设计并完成实验。2.初步认识工业上电解饱和食盐水制取氯气的反应原理,培养科学探究与创新意识的化学核心素养。
氯气主要用于生产塑料(如PVP)、合成纤维、染料、农药、消毒剂、漂白剂溶剂以及各种氯化物。 迪嘉特气的高纯氯气主要用于电子工业干刻、光导纤维、晶体生长和热氧化。
MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O
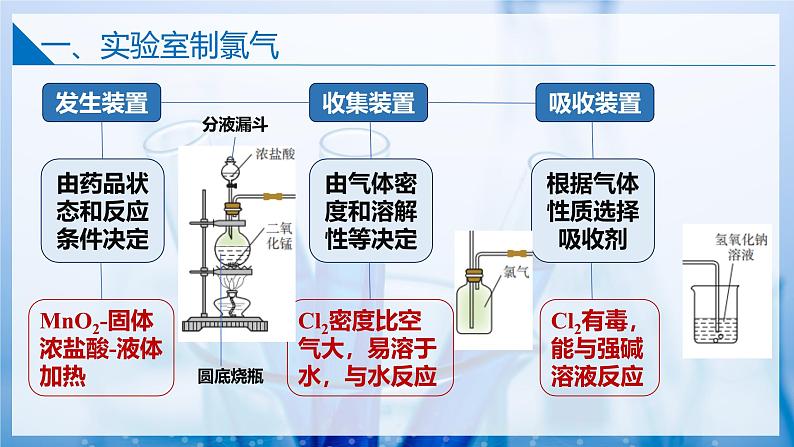
由药品状态和反应条件决定
MnO2-固体浓盐酸-液体加热
由气体密度和溶解性等决定
Cl2密度比空气大,易溶于水,与水反应
根据气体性质选择吸收剂
Cl2有毒,能与强碱溶液反应
氯气与空气不反应且密度比空气的大
吸收过量的氯气,防止污染环境
2NaOH+Cl2===NaCl+NaClO+H2O
先验密,后实验;先固体,后液体;先撤管,后熄灯。
这样收集到的氯气纯净吗?装置还有哪些可改进的?
Cl2能溶于水,难溶于饱和食盐水, HCl易溶于饱和食盐水
恒压装置既保障浓盐酸顺利滴下,又避免浓盐酸浪费和污染环境
用分液漏斗装浓盐酸,让浓盐酸缓慢地注入,不能一次将浓盐酸注入烧瓶里。
用分液漏斗可以控制液体的用量,避免生成的氯气过多。缓慢注入可提高浓盐酸利用率。
用浓盐酸和二氧化锰制取氯气时,要缓缓加热,不能强热。
浓盐酸有很强的挥发性,强热时能挥发出大量的氯化氢气体和水蒸气,而使制得的氯气中含有大量的杂质;另一方面,又降低了HCl的利用率。
实验结束后,先熄灭酒精灯使反应停止并排出残留的Cl2后,再拆卸装置,避免污染空气。
尾气吸收时,应选用NaOH溶液,不能选用澄清石灰水,因为澄清石灰水中含Ca(OH)2的量少,吸收不完全。
1、浓硫酸能否换成碱石灰?能换成什么干燥剂?
碱石灰能与氯气反应,不能用碱石灰;可换成无水氯化钙。
2、若MnO2过量,待充分反应后,溶液中仍有盐酸剩余,为什么?
随着反应的进行,浓盐酸的浓度逐渐减小,小到一定浓度将不再与MnO2反应。
如果将过量的二氧化锰与20 mL 12 ml·L-1的盐酸混合加热,充分反应后生成的氯气明显少于0.06 ml。其主要的原因有①______________________________________________________;②___________________________。
反应中随着HCl的消耗,盐酸变稀,稀盐酸不能与MnO2反应
加热时有部分HCl挥发而损失
使用浓盐酸与足量的MnO2共热制Cl2,实际产生的Cl2总比理论值低。
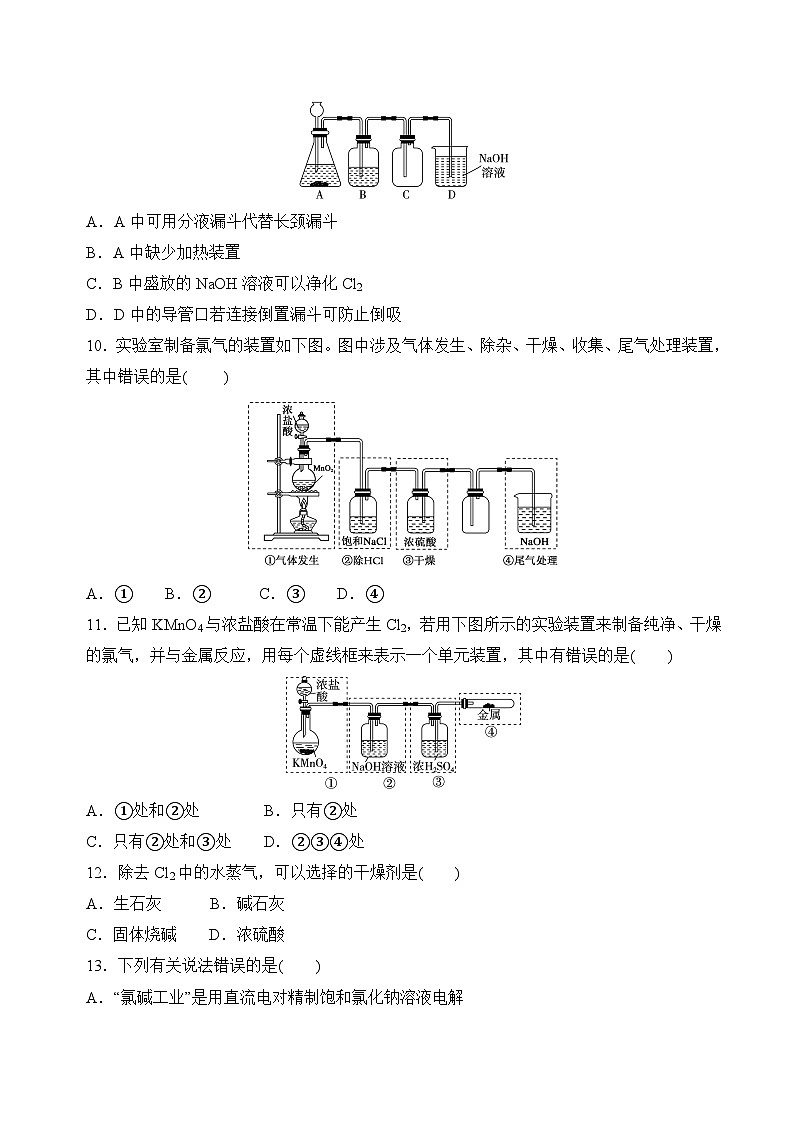
例1 下列描述正确的是( )A.将Cl2与HCl混合气体通过饱和食盐水可得到纯净干燥的Cl2B.将浓盐酸与MnO2共热产生的气体先通过浓H2SO4,后通过饱和食盐水来制备纯净干燥Cl2C.过量浓盐酸与一定量二氧化锰反应,MnO2能完全反应D.除去氯气中的HCl气体,装置如图
工业上对氯气的需求量很大。大量生产氯气不仅要求原料易得,而且价格也是必须考虑的重要因素。
海水中蕴含丰富的氯元素,它主要以氯化钠、氯化镁等氯化物的形式存在。
氯气性质活泼,氯元素在自然界没有游离态,只以化合态形式存在。
无色气体,靠近火焰有爆鸣声
黄绿色气体,能使湿润的淀粉碘化钾试纸变蓝
Cl2+2KI===I2+2KCl
工业制取氯气的反应原理:
2NaCl+2H2O 2NaOH+Cl2↑+H2↑
氯碱工业:以电解饱和食盐水为基础制取氯气等产品的工业。
例2.下列关于电解氯化钠水溶液的说法不正确的是( )A.电解产物为氯气和钠B.电解过程中能产生黄绿色气体C.电解一段时间后,将全部电解液转移到烧杯中,然后滴加石蕊溶液,溶液呈蓝色D.用排水法可以收集到较纯净的氢气
1.下图是某研究性学习小组设计制取氯气并以氯气为反应物进行特定反应的装置。
(1)A中反应的化学方程式: 。
(2)要将C装置接入B和D之间,正确的接法是a→ → →d。
(3)实验开始先点燃A处的酒精灯,打开弹簧夹K,让Cl2充满整个装置,再点燃D处的酒精灯。Cl2通过C装置后进入D,D装置内盛有炭粉,发生氧化还原反应,生成CO2和HCl(g),发生反应的化学方程式为 。 。为了使C装置发挥更好的作用,可向烧杯中加入浓硫酸,加入浓硫酸的作用是 。(4)D处反应完毕后,关闭弹簧夹K,移去两个酒精灯,由于余热的作用,A处仍有少量Cl2产生,此时B中的现象是 。
浓硫酸稀释时放热,促进水蒸气产生
瓶内气体黄绿色加深,瓶中液面下降,长颈漏斗内液面上升
相关课件
这是一份高中化学苏教版 (2019)必修 第一册第二单元 金属钠及钠的化合物备课ppt课件,文件包含321金属钠及钠的化合物钠的性质与制备同步课件pptx、321金属钠及钠的化合物钠的性质与制备分层练习-原卷版docx、321金属钠及钠的化合物钠的性质与制备分层练习-解析版docx、06钠的性质切割燃烧与水反应wmv、美丽化学之元素燃烧00_00_22-00_00_55mp4、钠与水反应mp4等6份课件配套教学资源,其中PPT共35页, 欢迎下载使用。
这是一份高中苏教版 (2019)第一单元 含硫化合物的性质集体备课课件ppt,文件包含412含硫化合物的性质硫酸的工业制备和性质同步课件pptx、412含硫化合物的性质硫酸的工业制备和性质分层练习--原卷版docx、412含硫化合物的性质硫酸的工业制备和性质分层练习--解析版docx、1-化工史话硫酸工业1-硫酸的发现及早期制备情况mp4、11-铜与浓硫酸mp4、浓硫酸的脱水性蔗糖mp4、铁与浓硫酸mp4、铝与浓硫酸mp4等8份课件配套教学资源,其中PPT共35页, 欢迎下载使用。
这是一份高中化学苏教版 (2019)必修 第一册专题3 从海水中获得的化学物质第一单元 氯气及氯的化合物精品ppt课件,共24页。PPT课件主要包含了含量g,海水中都有什么呢,学习目标,化学式Cl2,氯气的生产原理,一氯气的工业制法,电解饱和食盐水,实验原理,两极均产生气泡,有氢气生成等内容,欢迎下载使用。










