



化学人教版 (2019)第二章 海水中的重要元素——钠和氯第三节 物质的量学案
展开02
预习导学
自主梳理
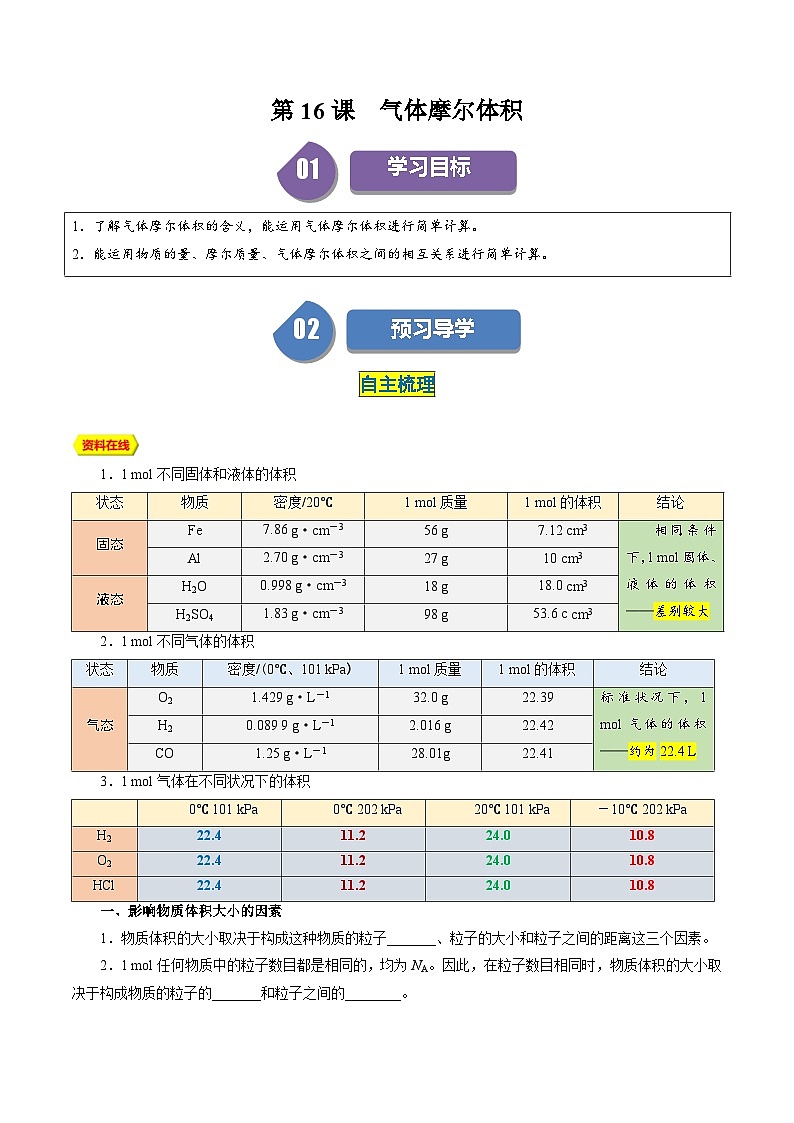
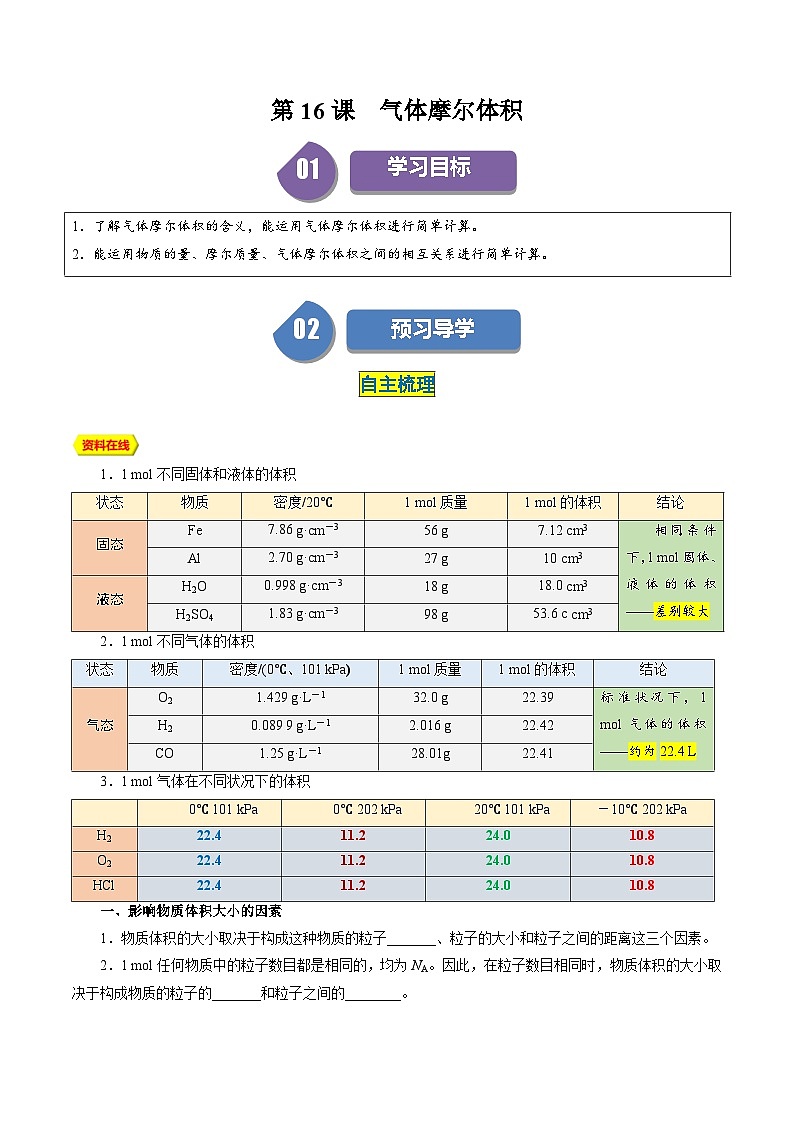
1.1 ml不同固体和液体的体积
2.1 ml不同气体的体积
3.1 ml气体在不同状况下的体积
一、影响物质体积大小的因素
1.物质体积的大小取决于构成这种物质的粒子_______、粒子的大小和粒子之间的距离这三个因素。
2.1 ml任何物质中的粒子数目都是相同的,均为NA。因此,在粒子数目相同时,物质体积的大小取决于构成物质的粒子的_______和粒子之间的________。
3.对于气体来说,粒子之间的距离远远大于粒子本身的直径。当粒子数目相同时,气体的体积主要取决于气体_______________________。
4.气体的体积取决于分子的数目和分子的间距,分子的间距与温度、压强有关:
压强一定,升高温度,分子之间的距离_______,气体体积_______;反之,气体体积_______。温度一定,增大压强,粒子之间的距离_______,气体体积_______;反之,气体体积增大。
二、气体摩尔体积和阿伏加德罗定律
1.单位物质的量的气体所占的________叫做气体摩尔体积,用符号Vm表示。气体摩尔体积的数值不是固定不变的,它取决于气体所处的_______和_______。
2.在相同温度和压强下,任何气体分子之间距离可看成是_________的,因此,在相同的温度和_______下,分子数相同的任何气体都具有相同的________。
预习检测
1.(2022年湖北省期中)下列物质的体积约为22.4 L的是
A.标准状况下,1 ml H2OB.20℃、101kPa时,36.5 g HCl
C.常温常压下,16 g CH4D.标准状况下,1 ml O2
2.(2023年江苏省海门中学期中)在标准状况下,1升某气体的质量为1.25 g,则该气体可能是
A.H2B.CO2C.CH4D.CO
3.(2023年江苏省沛县上学期第一次学情调研)在标准状况下,将1 g H2、11 g CO2和4 g O2混合,该混合气体的体积约为
A.16.8 LB.14 LC.19.6 LD.8.4 L
4.(2022年河北省唐山市遵化市期中)下列说法正确的是
A.气体摩尔体积就是22.4 L
B.任何状况下,1 ml任何气体的体积一定是22.4 L
C.标准状况下,22.4 L水含有6.02×1023个分子
D.1 ml H2和O2的混合气体在标准状况下的体积约22.4 L
5.(2022年四川省成都区期中)下列关于气体摩尔体积的几种说法正确的是
A.22.4 L任何气体的物质的量均为1 ml
B.非标准状况下,1 ml气体的体积不可能是22.4 L
C.0.1 ml H2、0.2 ml O2、0.3 ml N2和0.4 ml CO2组成的混合气体在标准状况下的体积约为22.4 L
D.在同温同压下,相同体积的任何气体单质所含分子数和原子数都相同
6.(2023年福建省宁德市上学期期中)同温、同压下,同体积的甲烷(CH4)和二氧化碳气体中,相同的是
A.物质的量B.原子总数C.密度D.质量
►环节一 气体摩尔体积
情境材料
教室标准尺寸国家标准
中小学教室标准尺寸长9米,宽6米,高3米。而普通中小学教室的标准是面积要求是50到60平方米。
问题探究
若教室的长9米,宽6米,高3米,则这间教室里空气的质量为多少?(已知空气的平均摩尔质量为29 g·ml-1)。
要点归纳
一、气体摩尔体积
1.决定物质体积的因素
①对于固体或液体,粒子之间的距离很小(几乎相等),其体积取决于粒子数目及大小;当粒子数目相同时(如各为1 ml),其体积与粒子大小(不同物质的粒子大小不相同)有关,所以1 ml不同的固体或液体的体积往往不相同。
②对气体来说,粒子之间的距离要比粒子本身的直径大很多倍,气体的体积与分子的大小无关,只取决于气体分子数目及间距(相同条件下,分子间距相同),所以1 ml不同的气体的体积几乎相同。
2.气体摩尔体积
(1)使用气体摩尔体积四注意
(2)用“22.4 L·ml-1”要“二看”
一看——物质状态,必有是气体,如标准状况下水、酒精、四氯化碳等为非气体物质。
二看——外界条件,必须为标准状况。非标准状况下,1 ml气体的体积不一定是22.4 L。
(3)气体摩尔体积的适用范围
气体摩尔体积的适用范围是气体,可以是单一气体,也可以是混合气体。需要注意的是混合气体中气体之间不能发生化学反应。
典例精讲
【例1】(2022年北京市丰台区期中)现有下列四种因素:①温度和压强、②所含微粒数、③微粒本身大小、④微粒间的距离,其中对气体物质体积有显著影响的是
A.②③④B.①②④C.①③④D.①②③④
【例2】(2022年福建厦门期末)标准状况下,下列物质所占体积最大的是
A.36 g H2OB.1.5 ml H2
C.48 g O3D.3.01×1023个N2
【例3】(2022年四川南充期末)下列各组物质中,所含分子数相同的是
A.10 gH2和10 gO2
B.5.6LN2(标准状况)和11 g CO2
C.18 g H2O和0.5 ml Br2
D.224 mLH2和0.01 mlN2
►环节二 阿伏加德罗定律
情境材料
2+1=2
190多年前,德国的数学家高斯和意大利科学家阿伏加德罗进行了一场激烈的辩论,核心是化学究竟是不是一门真正的科学。阿伏加德罗做一实验:将2 L氢气放在1 L氧气中燃烧得到2 L水蒸气,他十分自豪地对高斯说:“请看吧!只要化学愿意,它能使2加1等于2,数学能做到这一点吗?遗憾的是我们对化学知道的太少了!”。后来为解释气体体积反应定律——当温度和压强不变时,参加反应的气体与生成的气体体积间成简单的整数比。他提出了阿伏加德罗假说,后来被科学家证明为阿伏加德罗定律。
问题探究
1.实验时的温度必须超过_____℃。
2.阿伏加德罗定律在历史上曾经用来求气体的分子式。若在一定的温度和压强下,4体积某气态化合物完全分解后产生1体积气体A4和6体积气体B2,由此可推断该气态化合物化学式为_______;这是根据____________定律和__________定律推断出来的。
要点归纳
二、阿伏加德罗定律
1.概念:在相同的温度和压强下,相同体积的任何气体都含有相同数目的粒子。
2.推论
(1)阿伏加德罗定律既适用于单一气体,也适用于混合气体,但对于固体和液体则不适用。
(2)同温、同压、同体积和同分子数,共同存在,相互制约,只要“三同”成立,“第四同”必定成立。
典例精讲
【例4】(2022年江苏省扬州市扬州中学期中)在体积相同的两个密闭容器中分别充满C2H4、C3H6气体,当这两个容器内温度和气体密度相等时,下列说法正确的是
A.两种气体的压强是P(C2H4)<P(C3H6)B.C2H4比C3H6的质量小
C.两种气体的分子数目相等D.两种气体的氢原子数目相等
【例5】(2022·安徽宿州十三所重点中学期中)如图所示,气缸的总体积一定,内部被活塞隔成I、II两部分,活塞可以自由移动,也可以固定。25℃时向I中充入8 g SO2,II中充入8 g O2,则下列说法正确的是
A.当活塞不再移动时,I、II两部分体积比为1∶2
B.当活塞不再移动时,I、II两部分密度比为1∶1
C.当活塞固定在气缸中间,I、II两部分压强比为1∶1
D.当活塞固定在气缸中间,I、II两部分压强比为2∶1
04
课堂总结
决定物质体积大小的因素
气体摩尔体积
阿伏加德罗定律
在相同的温度和压强下,相同体积的任何气体都含有相同数目的分子。
0503
强化训练
1.(2022年山东省泰安肥城市期中)一定温度和压强下,用m g的CH4、CO2、O2、SO2四种气体分别吹出四个体积大小不同的气球,下列说法中正确的是
A.气球②中装的是O2
B.气球①和气球③中气体分子数相等
C.气球①和气球④中气体物质的量之比为4∶1
D.气球③和气球④中气体密度之比为2∶1
2.(2023年江苏省沛县上学期第一次学情调研)同温同压下,两种气体的体积如果不相同,其主要原因是
A.气体的分子大小不同B.气体分子间的平均距离不同
C.气体的性质不同D.气体的分子数不同
3.(2023年江苏省沛县上学期第一次学情调研)雾霾天气对环境造成了严重影响,部分城市开展PM2.5和臭氧的监测。下列有关说法正确的是
A.臭氧的摩尔质量是48 g
B.同温同压条件下,等质量的氧气和臭氧体积比为2∶3
C.16 g臭氧中含有6.02×1023个原子
D.通常状况下,1 ml氧气和臭氧混合气体的体积约为22.4 L
4.(2023年江苏省海门中学期中)1811年,阿伏加德罗在大量实验基础上得出结论:同温同压下,相同体积的任何气体都含有相同数目的分子。根据这个结论,下列叙述不正确的是
A.同温同压下,等质量的氮气和一氧化碳体积相同
B.同温同压下,等体积的两种气体原子数不一定相等
C.同温同压下,气体的体积与分子数成正比
D.两种分子数和体积都相等的气体,所处的温度和压强一定相同
5.(2022年江苏省宿迁市沭阳县期中)下列说法正确的是
A.2 g H2含有的氢原子物质的量为1 ml
B.常温常压下,22.4 LO2含有的分子物质的量为1 ml
C.65 g Zn与足量盐酸反应失去的电子物质的量为2 ml
D.标准状况下,22.4 L的H2O含有的分子物质的量为1 ml
6.(2023年江苏省海门中学期中)实验室用镁带和稀硫酸反应产生氢气,来测定氢气的气体摩尔体积,所涉及到的步骤有①读数;②冷却至室温;③调节使水准管和量气管液面相平。正确的顺序是
A.①②③B.①③②C.③①②D.②③①
7.(2023年北京丰台区期中)等物质的量的SO2和SO3相比较,下列结论不正确的是
A.分子数目之比为1∶1B.氧原子数目之比为2∶3
C.质量之比为1∶1D.同温同压下体积之比为1∶1
8.(2023年江苏省海安中学期中)在两个密闭容器中,分别充有质量相等的甲乙两种气体。若两容器的温度和压强均相等,且甲的密度大于乙的密度,则下列说法正确的是
A.甲的分子数比乙的分子数多B.甲的物质的量比乙的物质的量少
C.甲的摩尔体积比乙的摩尔体积小D.甲的相对分子质量比乙的相对分子质量小
9.(2023年江苏省常州高级中学第一次调研)下列说法正确的是
A.同温同压下质量相同的O2和O3为的原子数之比是2∶3
B.5.6 g CO和22.4 L CO2含有的碳原子数一定相等
C.20℃,1×1015Pa时,相同体积的O2和CO2具有相同的分子数
D.当气态物质的体积为22.4 L时,该气体一定处于标准状况
10.(2022年河北省石家庄市第二十八中学期中)已知NA为阿伏加德罗常数的值。回答下列问题:
(1)质量相同的H2、NH3、SO2、O3四种气体中,含有分子数目最少的是________(填化学式,下同),在相同温度和相同压强条件下,体积最大的是_______。
(2)73.0 g HCl气体中含有的分子数为_____________,标准状况下的体积为_________L。
(3)18.6 g Na2R含0.6 ml Na+,则Na2R的摩尔质量为________,R的相对原子质量为________。
(4)已知CO、CO2的混合气体质量共16.0 g,标准状况下体积为8.96 L,则该混合气体中CO与CO2的体积比为_________。1.了解气体摩尔体积的含义,能运用气体摩尔体积进行简单计算。
2.能运用物质的量、摩尔质量、气体摩尔体积之间的相互关系进行简单计算。
状态
物质
密度/20℃
1 ml质量
1 ml的体积
结论
固态
Fe
7.86 g·cm-3
56 g
7.12 cm3
相同条件下,1 ml固体、液体的体积——差别较大
Al
2.70 g·cm-3
27 g
10 cm3
液态
H2O
0.998 g·cm-3
18 g
18.0 cm3
H2SO4
1.83 g·cm-3
98 g
53.6 c cm3
状态
物质
密度/(0℃、101 kPa)
1 ml质量
1 ml的体积
结论
气态
O2
1.429 g·L-1
32.0 g
22.39
标准状况下,1 ml气体的体积——约为22.4 L
H2
0.089 9 g·L-1
2.016 g
22.42
CO
1.25 g·L-1
28.01g
22.41
0℃ 101 kPa
0℃ 202 kPa
20℃ 101 kPa
-10℃ 202 kPa
H2
22.4
11.2
24.0
10.8
O2
22.4
11.2
24.0
10.8
HCl
22.4
11.2
24.0
10.8
定义
单位物质的量的气体所占的体积
符号
Vm
单位
L·ml-1(或L/ml)
特例
标准状况下(即0 ℃和101 kPa),气体摩尔体积约为22.4 L·ml-1
相同条件
结论
公式
语言叙述
同温同压
eq \f(V1,V2)=eq \f(n1,n2)=eq \f(N1,N2)
同温同压下,体积之比等于物质的量之比,等于分子数之比
同温同体积
eq \f(p1,p2)=eq \f(n1,n2)=eq \f(N1,N2)
同温同体积下,压强之比等于物质的量之比,等于分子数之比
同温同压
eq \f(ρ1,ρ2)=eq \f(M1,M2)
同温同压下,密度之比等于摩尔质量之比
同温同压同体积
eq \f(m1,m2)=eq \f(M1,M2)
同温同压下,体积相同的气体,其质量与摩尔质量成正比
化学必修 第一册第三节 化学键导学案及答案: 这是一份化学必修 第一册<a href="/hx/tb_c162000_t4/?tag_id=42" target="_blank">第三节 化学键导学案及答案</a>,文件包含第30讲48共价键教师版-2024年高中化学同步精品讲义必修一docx、第30讲48共价键学生版-2024年高中化学同步精品讲义必修一docx等2份学案配套教学资源,其中学案共26页, 欢迎下载使用。
人教版 (2019)必修 第一册第二节 元素周期律学案: 这是一份人教版 (2019)必修 第一册<a href="/hx/tb_c161998_t4/?tag_id=42" target="_blank">第二节 元素周期律学案</a>,文件包含第25讲43核素教师版-2024年高中化学同步精品讲义必修一docx、第25讲43核素学生版-2024年高中化学同步精品讲义必修一docx等2份学案配套教学资源,其中学案共19页, 欢迎下载使用。
人教版 (2019)必修 第一册第一节 物质的分类及转化导学案: 这是一份人教版 (2019)必修 第一册<a href="/hx/tb_c161971_t4/?tag_id=42" target="_blank">第一节 物质的分类及转化导学案</a>,文件包含第02讲12物质的转化教师版-2024年高中化学同步精品讲义必修一docx、第02讲12物质的转化学生版-2024年高中化学同步精品讲义必修一docx等2份学案配套教学资源,其中学案共20页, 欢迎下载使用。













