




专题 1 物质的分类及转化-高中化学学业水平考试学考复习专题(广东专用)
展开知识点一 物质分类
1.元素与物质的关系
(1)元素是物质的基本组成成分,物质都是由元素组成的。
(2)每一种元素都能自身组成单质,有的单质有多种形态,如碳元素形成的单质有金刚石、石墨和C60等,像这样由同一种元素形成的几种性质不同的单质,叫做这种元素的同素异形体。
【易错警示】
①同素异形体之间的转换是化学变化;
②同素异形体之间由于结构不同,物理性质有差异,但由于同种元素组成,化学性质相似或略有差异;
③由一种元素组成的物质不一定是纯净物。如氧气和臭氧。
2.物质与微粒的关系
物质都是由微粒构成的,构成物质的微粒有分子、原子和离子,如水和酒精是由分子构成的,铜、金刚石和石墨是由原子构成的,氯化钠、硫酸铜是由离子构成的。
3.分类方法
常用的两种分类法是交叉分类法和树状分类法。
(1)含义:根据不同的分类标准,对同一事物进行多种分类的一种分类方法。即对事物以不同的标准进行分类。
(2)举例:试从不同的角度对下列各组物质进行分类,将其类别名称分别填在相应的空格内。
(2)树状分类法。
①酸的分类:酸可依据电离出氢离子的个数,将酸分为一元酸、二元酸、多元酸。也可按照酸分子中是否含氧元素,将酸分为含氧酸和无氧酸。
一元酸:HCl、HNO3、CH3COOH等 含氧酸:HNO3、H2CO3、H2SO4等
酸 二元酸:H2CO3、H2SO4等 酸
多元酸:H3PO4 无氧酸:HCl、H2S等
②碱的分类:可依据电离出OH-的个数,将碱分为一元碱、二元碱、多元碱。 也可按照溶解性,将碱分为可溶性碱、难溶性碱。
一元碱:NaOH、NH3·H2O 可溶性碱:NaOH、Ba(OH)2等
碱 二元碱:Mg(OH)2、Cu(OH)2 碱 难溶性碱:Mg(OH)2、Cu(OH)2 等
多元碱:Fe(OH)3、Al(OH)3
③盐的分类
正盐:既不能电离出H+,也不能电离出OH-的盐,如Na2CO3、CuSO4
盐 酸式盐:酸根能电离出H+的盐,如NaHCO3、NaHSO4
碱式盐:能电离出OH-的盐,如Cu2(OH)2CO3
④氧化物的分类:依据氧化物的性质,可将氧化物分为酸性氧化物、碱性氧化物、两性氧化物及不成盐氧化物。
酸性氧化物:与碱反应只生成盐和水。如CO2、SO2、SiO2等
氧化物 碱性氧化物:与碱反应只生成盐和水。如Fe2O3、CaO等
两性氧化物:既能与酸反应又能与碱反应。如Al2O3
不成盐氧化物:既不与酸反应也不与碱反应。如NO、CO等
【易错警示】
NO2不属于酸性氧化物;
Na2O2、Fe3O4不属于碱性氧化物。Na2O2属于过氧化物,Fe3O4属于复杂氧化物。
【巩固练习】
1.2020年12月4日,“嫦娥5号”完成对月球钻岩取样工作。月岩中共有大约55种矿物,玄武岩最多,其中富含硅、氧、铁、钛、铝和钙等元素。下列叙述错误的是( )
A.Fe2O3属于碱性氧化物 B.CaO属于碱性氧化物
C.Al2O3属于碱性氧化物 D.SiO2属于酸性氧化物
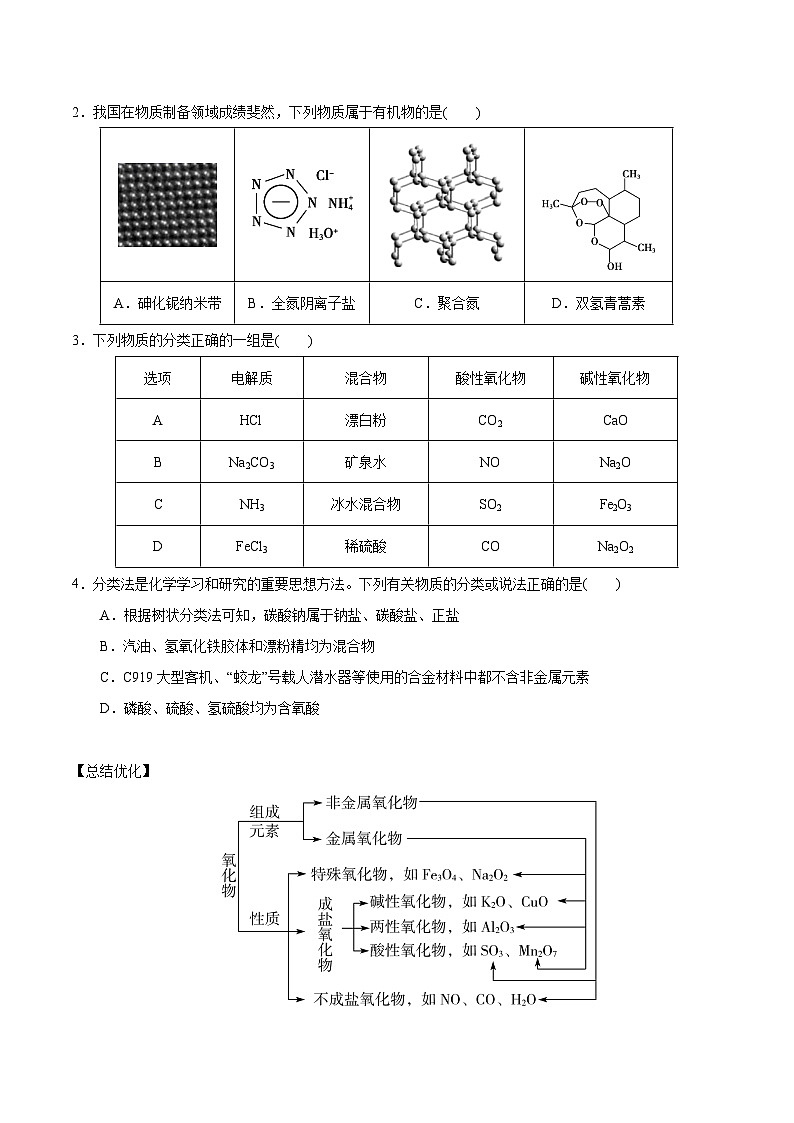
2.我国在物质制备领域成绩斐然,下列物质属于有机物的是( )
3.下列物质的分类正确的一组是( )
4.分类法是化学学习和研究的重要思想方法。下列有关物质的分类或说法正确的是( )
A.根据树状分类法可知,碳酸钠属于钠盐、碳酸盐、正盐
B.汽油、氢氧化铁胶体和漂粉精均为混合物
C.C919大型客机、“蛟龙”号载人潜水器等使用的合金材料中都不含非金属元素
D.磷酸、硫酸、氢硫酸均为含氧酸
【总结优化】
知识点二 分散系及其分类
1.分散系
(1)分散系
(2)分类:按照分散质粒子的大小
2.胶体
(1)胶体的分类:按照分散剂的状态不同可分为三类
常见胶体:牛奶、豆浆、空气、血液、墨水、土壤、蛋白质溶液、淀粉溶液等。
(2)Fe(OH)3胶体的配制
试剂:蒸馏水、饱和FeCl3溶液
过程:向沸水中逐滴滴加饱和FeCl3溶液,加热直到溶液变为红褐色时,停止加热,即得到Fe(OH)3胶体。
化学方程式:FeCl3 + 3H2Oeq \(=====,\s\up7(△))Fe(OH)3(胶体)+3HCl。
【易错警示】不可用自来水配制,不能加热时间过长,防止胶体变成沉淀。
(3)胶体的性质及应用
丁达尔效应:可见光束通过胶体时,在入射光的侧面可看见胶体中有一条光亮的“通路”,这种现象称为丁达尔效应。这是由胶体粒子对光线散射而形成的。
应用:可用于鉴别溶液和胶体。
实例:放电影、光线透过树叶间的缝隙射入密林等。
【巩固练习】
1.新型冠状病毒可通过气溶胶传播,气溶胶属于胶体的一种。下列有关胶体的叙述正确的是( )
A.雾是气溶胶,在阳光下可观察到丁达尔效应
B.将Fe(OH)3胶体过滤,在滤纸上能得到分散质
C.向有污染的水中加入胶体,具有杀菌消毒的作用
D.在饱和氯化铁溶液中逐滴加入NaOH溶液,产生红褐色的Fe(OH)3胶体
2.分散系是混合分散体系的简称,下列关于分散系的说法正确的是( )
A.根据体系的稳定性,可将分散系分为溶液、胶体和浊液
B.一种分散系的分散质可以是固态、液态或气态,但只能是纯净物
C.利用丁达尔效应可以区分溶液和胶体,它利用了光的折射原理
D.用光束照射牛奶会出现丁达尔效应
3.分类法在化学发展中起到了非常重要的作用,下列说法正确的是( )
A.NaHCO3溶液为碱性,故NaHCO3属于碱式盐
B.纳米级CaCO3微粒大小在50 nm左右,故纳米级CaCO3属于胶体
C.SO3溶于水可以导电,故SO3属于电解质
D.SiO2可以与NaOH反应生成Na2SiO3和水,故SiO2属于酸性氧化物
4.分类是学习和研究化学的一种常用的科学方法。下列分类合理的是( )
A.金属氧化物一定是碱性氧化物
B.根据酸分子中H原子个数分为一元酸、二元酸等
C.根据丁达尔现象将分散系分为胶体、溶液和浊液
D.根据SiO2是酸性氧化物,判断其可与NaOH溶液反应
5.下列有关物质分类的叙述正确的是( )
A.CaCl2、NaOH、HCl、O2四种物质都属于化合物
B.溶液、浊液、胶体都属于混合物
C.硫酸、纯碱、硝酸钠和生石灰分别属于酸、碱、盐和碱性氧化物
D.CO2、CO等非金属氧化物均属于酸性氧化物
6.下列有关物质的分类或归纳的说法正确的是( )
A.PM 2.5(微粒直径约为 2.5×10-6 m)分散在空气中形成气溶胶,能产生丁达尔效应
B.乙烯、油脂、纤维素、光导纤维都属于高分子化合物
C.漂白粉、水玻璃、福尔马林都是混合物
D.纯碱、氨水、蔗糖分别属于强电解质、弱电解质和非电解质
【总结优化】
知识点三 物质的转化
1.酸、碱、盐的主要化学性质
同类事物往往具有相似的性质。
(1)酸的主要化学性质(以H2SO4为例)
(2)碱的主要化学性质(以NaOH为例)
(3)盐的主要化学性质(以CuSO4为例)
2.不同酸或碱或盐性质相似的微观解释
从微观角度来看,不同的酸溶液都含有H+,不同碱溶液都含有OH-,所以不同的酸或碱性质相似;不同的碳酸盐溶液都含有CO32-,所以不同的碳酸盐也有相似的化学性质。
3.酸、碱、盐的反应类型
从反应类型看,我们初中学过的酸与金属、盐与金属的反应都属于置换反应,酸与碱、盐与酸、盐与碱、盐与盐之间的反应都属于复分解反应。
4.物质的转化
【易错警示】在认识一类物质的共性的同时,还要注意某种物质的特性,如大多数酸和金属活动顺序表中氢前面的金属反应时都能发生置换反应生成氢气,但硝酸不能发生该类反应。
【巩固练习】
1.“古诗文经典已融入中华民族的血脉”。下列诗文中隐含化学变化的是( )
A.月落乌啼霜满天,江枫渔火对愁眠B.掬月水在手,弄花香满衣
C.飞流直下三千尺,疑是银河落九天D.举头望明月,低头思故乡
2.下列属于置换反应的是( )
A.2FeCl3+Cu===CuCl2+2FeCl2 B.4HNO3(浓) eq \(=====,\s\up7(△))4NO2↑+O2↑+2H2O
C.CuO +Ceq \(=====,\s\up7(△))Cu+CO2 D.2Mg +CO2eq \(=====,\s\up7(点燃))2MgO+C
3.近年来我国大力弘扬中华优秀传统文化体现了中华民族的文化自信。下列有关说法不正确的是( )
A.成语“百炼成钢”水滴石穿”中均涉及了氧化还原反应
B.“忽如一夜春风来,千树万树梨花开”的场景描述主要是物理变化
C.《梦溪笔谈》中“又石穴中水,所滴者皆为钟乳……”不涉及氧化还原反应
D.《荷塘月色》中“薄薄的青雾浮起在荷塘里”中的“青雾”属于胶体
4.在一定条件下,下列物质跟酸、碱、盐都能发生反应的是( )
A.CaO B.Na2CO3 C.CaCO3 D.CO2
【总结优化】
【效果验证】
1.牙膏常用碳酸钙(CaCO3)作摩擦剂。碳酸钙属于( )
A.氧化物 B.酸 C.碱 D.盐
2.下列物质中,属于氧化物的是( )
A.H3PO4 B.KOH C.MgO D.AgNO3
3.下列物质中属于纯净物、化合物、无机化合物、盐、钙盐的是( )
A.石灰石 B.Ca(OH)2 C.CaCO3 D.CH4
4.下列物质既属于钠盐,又属于含氧酸盐的是( )
A.Na2SO4 B.NaCl C.K2SO4 D.NaOH
5.下列厨房中的常见物质溶于相应溶剂后,不能形成胶体的是( )
A.淀粉溶于水中 B.鸡蛋清溶于水中
C.豆浆加入水中 D.食醋溶于水中
6.“纳米材料”是当今材料科学研究的前沿,其研究成果广泛应用于催化及军事领域。所谓“纳米材料”是指研究开发出的直径从几纳米至几十纳米的材料。将纳米材料分散到空气中形成胶体,该胶体属于( )
A.固溶胶 B.液溶胶
C.气溶胶 D.悬浊液
7.根据中央电视台报道,近年来,我国的一些沿江或沿海城市多次出现大雾天气,致使高速公路关闭,航班停飞,雾属于下列分散系中的( )
A.溶液 B.悬浊液
C.乳浊液 D.胶体
8.FeCl3溶液和Fe(OH)3胶体具有的共同性质是( )
A.都能透过滤纸 B.都呈红褐色
C.具有相同的颗粒直径D.都存在布朗运动
9.下列物质所属类别不正确的一组是( )
A.混合物:空气、碱石灰
B.化合物:氢氧化钙、石灰石
C.碱性氧化物:氧化钠、氧化钙
D.盐:碳酸钠、碳酸氢钠
10.下列关于物质分类的叙述不正确的是( )
A.硫酸属于酸 B.液氨属于纯净物
C.碳酸钠属于碱 D.氧化钠属于氧化物
11.下列变化过程中不涉及化学反应的是( )
A.陶瓷的烧制 B.活字印刷排版术
C.鞭炮和烟火的燃放D.铜塑像表面出现铜绿
12.KOH是我国古代纺织业常用于漂洗的洗涤剂。古代制取KOH的流程如下。图中流程中没有涉及的化学反应类型是( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
13.下列反应方程式中有一个与其他三个在分类上不同,该反应是( )
A.3Fe+2O2eq \(=====,\s\up15(点燃))Fe3O4 B.CO2+Ceq \(=====,\s\up15(高温))2CO
C.NH4HSeq \(=====,\s\up15(△))NH3↑+H2S↑ D.Na2CO3+CO2+H2O===2NaHCO3
14.盐是一类常见的物质,下列物质通过一步反应可直接形成盐的是( )
①金属单质 ②碱性氧化物 ③碱 ④非金属单质 ⑤酸性氧化物 ⑥酸
A.①②③ B.①④⑥
C.②⑤⑥ D.全部
15.用下图表示的一些物质或概念之间的从属或包含关系中错误的是( )
16.《天工开物·杀青》中关于竹纸和皮纸的记载中有以下步骤,其中涉及化学变化的是( )
A.煮徨足火 B.舂臼取泥
C.荡料入帘 D.覆帘压纸
17.合成新物质是研究化学的主要目的之一。意大利科学家最近合成了一种新型的氧分子O4。下列关于O4的说法正确的是( )
A.O4是一种新型的化合物
B.1个O4分子由两个O2分子构成
C.O4和O2互为同素异形体
D.O4和O2可通过氧化还原反应实现转化
18.下列物质在给定条件下的转化均能一步实现的是( )
A.Fe3O4eq \(――→,\s\up15(CO))Feeq \(――→,\s\up15(HCl))FeCl3
B.H2O2eq \(――→,\s\up15(HCl))H2eq \(――→,\s\up15(O2))H2O
C.CaCl2溶液eq \(――→,\s\up15(CO2))CaCO3eq \(――→,\s\up15(HCl))CO2
D.CuSO4溶液eq \(――→,\s\up15(HCl))Cueq \(――→,\s\up15(O2))CuO
19.下表所列各组物质中,物质之间按箭头方向不能通过一步反应实现如图所示转化关系的是( )
20.某化学课外活动小组制备氢氧化铁胶体并检验其性质:
(1)把饱和FeCl3溶液逐滴滴入沸水中,能形成胶体,其反应的化学方程式为____________(填字母,下同)。
a.FeCl3+3H2Oeq \(=====,\s\up7(△))Fe(OH)3↓+3HCl
b.FeCl3+3H2Oeq \(=====,\s\up7(△))Fe(OH)3(胶体)+3HCl
(2)为验证制得的分散系是胶体,下列方法中最简单的是________。
a.用一束可见光照射该分散系,观察是否产生丁达尔效应
b.向分散系中加入氯化钠,观察是否聚沉
c.在分散系中插入石墨电极,接通直流电源,观察与直流电源负极相连的一极颜色是否变深
(3)取少量的氢氧化铁胶体于试管中,逐滴加入稀硫酸,其现象是________。
a.出现红褐色沉淀
b.红褐色溶液变为棕黄色
c.先出现红褐色沉淀,然后沉淀逐渐溶解
(4)氢氧化铁胶体能稳定存在的原因是____________。
A.胶体的分散质微粒直径小于1 nm
B.胶体的分散质微粒均带正电荷
C.胶体的分散质微粒能透过滤纸
21.同学们吃的零食的包装袋中经常有一个小纸袋,上面写着“干燥剂”,其主要成分是生石灰(CaO)。
(1)生石灰属于________(填字母,下同)。
A.酸 B.碱 C.盐 D.纯净物 E.化合物
F.金属氧化物 G.非金属氧化物 H.碱性氧化物
I.酸性氧化物
(2)某同学将浓硫酸、NaOH固体、生石灰等物质划分为一类。该同学的分类依据为________。
A.酸类 B.碱类
C.氧化物 D.干燥剂
(3)生石灰可作干燥剂的理由是___________________________ (用化学方程式表示)。
(4)生石灰还可以跟哪些类别的物质发生化学反应?请列举两例并填表。
(5)小纸袋中的物质能否长期持续地作干燥剂?____________。
【强化提升】
1.油条的做法是将矾、碱、盐按比例加入温水中,再加入面粉搅拌成面团;放置,使面团产生气体,形成孔洞。放置过程发生反应:2KAl(SO4)2·12H2O+3Na2CO3===2Al(OH)3↓+3Na2SO4+K2SO4+3CO2↑+21H2O。下列判断正确的是( )
A.从物质的分类角度来看,油条配方中的“矾、碱、盐”主要成分均为盐
B.放置过程发生的反应为氧化还原反应
C.放置过程发生的反应中,反应物和生成物均为电解质
D.反应的离子方程式为2Al3++3 CO32-===2Al(OH)3↓+3CO2↑
2.工业上利用矿物资源的流程图如下,下列说法正确的是( )
A.转化产物中FeO为碱性氧化物,金属氧化物均为碱性氧化物
B.制备玻璃过程中,石灰石的主要成分属于盐类,纯碱属于碱类,二者均能与盐酸反应
C.在制备纯硅过程SiCl4+2H2eq \(=====,\s\up7(高温))Si+4HCl为复分解反应
D.黄铜矿(主要成分为CuFeS2)与O2反应是氧化还原反应A.砷化铌纳米带
B.全氮阴离子盐
C.聚合氮
D.双氢青蒿素
选项
电解质
混合物
酸性氧化物
碱性氧化物
A
HCl
漂白粉
CO2
CaO
B
Na2CO3
矿泉水
NO
Na2O
C
NH3
冰水混合物
SO2
Fe2O3
D
FeCl3
稀硫酸
CO
Na2O2
分散系
溶液
胶体
浊液
分散质粒子直径
<1nm
1-100nm
>100nm
外观
均一、透明
较均一、透明或半透明
不均一、不透明
稳定性
稳定
介稳定
不稳定
能否透过滤纸
能
能
不能
实例
NaCl溶液
Fe(OH)3胶体
泥水
分散剂状态
液体
气体
固体
胶体类别
液溶胶
气溶胶
固溶胶
举例
Fe(OH)3胶体
烟、云、雾
有色玻璃
分散系
溶液
胶体
浊液
分散质粒子直径
小于1 nm
1~100 nm
大于100 nm
性质
外观
均一、透明
均一
不均一、不透明
稳定性
稳定
较稳定
不稳定
能否透过滤纸
能
能
不能
能否透过半透膜
能
不能
不能
鉴别
无丁达尔效应
有丁达尔效应
静置分层或沉淀
酸的主要化学性质
反应实例(写出化学方程式)
酸与活泼金属反应
H2SO4+Zn==ZnSO4+H2↑
酸与碱性氧化物的反应
H2SO4+CuO==CuSO4+H2O
酸与碱反应
H2SO4+2NaOH==Na2SO4+2H2O
酸与某些盐反应
H2SO4+BaCl2== BaSO4↓+2HCl
碱的主要化学性质
反应实例(写出化学方程式)
碱与某些酸性氧化物的反应
2NaOH+CO2==Na2CO3+H2O
碱与酸反应
2NaOH+H2SO4==Na2SO4+2H2O
碱与某些盐反应
2NaOH+CuSO4== Cu(OH)2↓+Na2SO4
盐的主要化学性质
反应实例(写出化学方程式)
盐与活泼金属反应
Zn+CuSO4==ZnSO4+Cu
盐与碱反应
CuSO4+2NaOH ==Cu(OH)2↓+Na2SO4
盐与某些盐反应
CuSO4+BaCl2== BaSO4↓+CuCl2
选项
X
Y
Z
A
氧化物
化合物
纯净物
B
溶液
分散系
混合物
C
强电解质
电解质
化合物
D
置换反应
氧化还原反应
离子反应
选项
物质
甲
乙
丙
A
CuO
CO2
H2O
B
C
CO
CO2
C
CaCO3
CaO
Ca(OH)2
D
H2SO4
H2O
H2
物质类别
化学方程式
专题2 离子反应-高中化学学业水平考试学考复习专题(广东专用): 这是一份专题2 离子反应-高中化学学业水平考试学考复习专题(广东专用),文件包含02离子反应解析版docx、02离子反应学生版docx等2份试卷配套教学资源,其中试卷共21页, 欢迎下载使用。
专题3 氧化还原反应-高中化学学业水平考试学考复习专题(广东专用): 这是一份专题3 氧化还原反应-高中化学学业水平考试学考复习专题(广东专用),文件包含03氧化还原反应解析版docx、03氧化还原反应学生版docx等2份试卷配套教学资源,其中试卷共20页, 欢迎下载使用。
【学考复习】2024年高中化学学业水平考试(新教材专用)第06讲 物质的量-复习讲义: 这是一份【学考复习】2024年高中化学学业水平考试(新教材专用)第06讲 物质的量-复习讲义,文件包含知识梳理2024年高中化学学业水平考试新教材专用第06讲物质的量-讲义原卷版docx、知识梳理2024年高中化学学业水平考试新教材专用第06讲物质的量-讲义解析版docx等2份试卷配套教学资源,其中试卷共33页, 欢迎下载使用。












