






所属成套资源:2025届高中化学全程复习构想课件
2025届高中化学全程复习构想课件全套28化学键
展开
这是一份2025届高中化学全程复习构想课件全套28化学键,共26页。PPT课件主要包含了考点一,考点二,阳离子,非金属之间,不同种,最外层电子,⑥⑦⑧,⑤⑥⑦⑧,答案A,极性键等内容,欢迎下载使用。
1.了解化学键的定义,了解离子键、共价键的形成。2.了解共价键的类型及键参数。
1.化学键(1)定义:相邻原子之间强烈的相互作用。(2)化学反应的本质:反应物的旧化学键断裂与生成物的新化学键形成。
2.离子键和共价键的比较
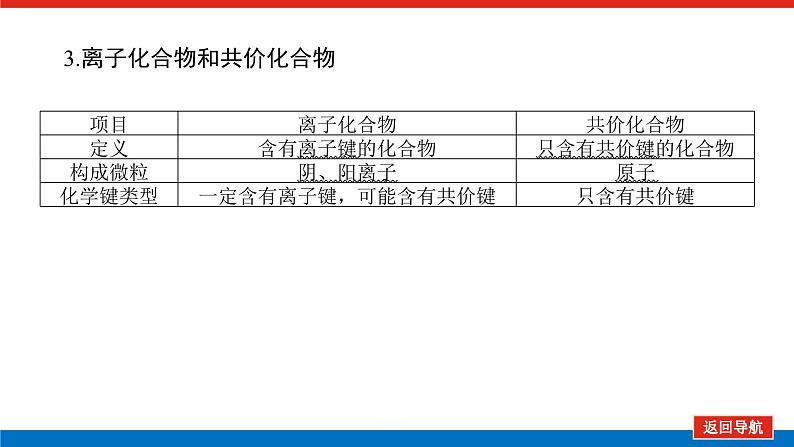
3.离子化合物和共价化合物
4.化学键的表示方法——电子式(1)概念:在元素符号周围用“·”或“×”来表示原子的____________的式子。(2)用电子式表示化合物的形成过程①离子化合物:如NaCl_______________________。②共价化合物:如HCl________________________。
【教考衔接】典例1 正误判断,正确的打“√”,错误的打“×”。(1)[2023·湖南卷,2A]HClO的电子式: ( )(2)[2023·辽宁卷,2B]P4中的共价键类型:非极性键( )
【师说·延伸】 化学键与物质类别之间的关系
【对点演练】考向一 化学键与离子化合物、共价化合物的判断1.一定条件下,氨与氟气发生反应:4NH3+3F2===NF3+3NH4F,其中NF3的空间结构与NH3相似。下列有关说法错误的是( )A.除F2单质外,反应物和生成物均为共价化合物B.NF3中各原子均满足8电子稳定结构C.NF3中只含极性共价键D.NH4F中既含有离子键又含有共价键
解析:NF3为共价化合物,NH4F为离子化合物。
考向二 电子式的规范书写2.判断下列电子式书写是否正确。
3.写出下列微粒的电子式。(1)—OH________________,H3O+________________。(2)H2S________________,N2H4________________。(3)NaH________________,NaBH4________________。
1.共价键的特征:共价键具有方向性和饱和性。2.分类
(2)键参数对分子性质的影响①键能越大,键长越________,分子越稳定。 ②
【易错诊断】 判断正误,错误的说明理由。1.σ键能单独形成,而π键一定不能单独形成:___________________________________________________________。2.σ键可以绕键轴旋转,π键一定不能绕键轴旋转:___________________________________________________________。3.在任何情况下,都是σ键比π键强度大:___________________________________________________________。4.分子的稳定性与分子间作用力的大小无关:___________________________________________________________。
错误。有的π键强度比σ键强度大。
【教考衔接】典例1 [2023·山东卷,5]石墨与F2在450 ℃反应,石墨层间插入F得到层状结构化合物(CF)x,该物质仍具润滑性,其单层局部结构如图所示。下列关于该化合物的说法正确的是( )A.与石墨相比,(CF)x导电性增强B.与石墨相比,(CF)x抗氧化性增强C.(CF)x中C—C的键长比C—F短D.1 ml (CF)x中含有2x ml共价单键
解析:石墨导电的原因是石墨层间有自由移动的电子,石墨层间插入F得到层状结构化合物(CF)x后,可自由移动的电子减少,导电性减弱,A错误;石墨层间插入F后形成的C—F键极短,键能极大,分子结构稳定性增强,抗氧化性增强,B正确;随原子序数递增,同周期主族元素的原子半径逐渐减小,因此(CF)x中C—C的键长比C—F长,C错误;由题图知,(CF)x中每个碳原子形成3个C—C键、1个C—F键,其中每个C—C键被2个碳原子共用,则1 ml (CF)x中含有2.5x ml共价单键,D错误。
典例2 (1)[2022·全国甲卷节选]聚四氟乙烯的化学稳定性高于聚乙烯,从化学键的角度解释原因___________________________________________________________。(2)[2022·全国乙卷节选]一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、一氯乙炔(C2HCl)分子中,C—Cl键长的顺序是______________________,理由:(ⅰ)C的杂化轨道中s成分越多,形成的C—Cl键越强;(ⅱ)________________________________________。
C—F键的键能大于聚乙烯中C—H的键能,键能越大,化学性质越稳定
一氯乙烷>一氯乙烯>一氯乙炔
Cl参与形成的大π键越多,形成的C—Cl键的键长越短
【对点演练】考向一 共价键的类型及数目判断1.(1)CH4中的化学键从形成过程来看,属于______(填“σ”或“π”)键,从其极性来看属于______键。(2)已知CN-与N2结构相似,推算HCN分子中σ键与π键数目之比为________。(3)C60分子中每个碳原子只跟相邻的3个碳原子形成共价键,且每个碳原子最外层都满足8电子稳定结构,则一个C60分子中π键的数目为________。
考向二 对共价键参数的理解与应用2.N≡N键的键能为946 kJ·ml-1,N—N键的键能为193 kJ·ml-1,则一个π键的平均键能为__________,说明N2分子中________键比________键稳定(填“σ”或“π”)。3.Ge与C是同族元素,C原子之间可以形成双键、三键,但Ge原子之间难以形成双键或三键。从原子结构角度分析,原因是___________________________________________________________。
376.5 kJ/ml
Ge原子半径大,原子间形成的σ单键较长,p-p轨道肩并肩重叠程度很小或几乎不能重叠,难以形成π键,不易形成双键或三键
4.结合事实判断CO和N2相对活泼的是________,试用下表中的键能数据解释其相对活泼的原因:___________________________________________________________。
断开CO分子的第一个化学键所需要的能量(273.0 kJ·ml-1)比断开N2分子的第一个化学键所需要的能量(523.3 kJ·ml-1)小
相关课件
这是一份2025届高中化学全程复习构想课件全套20硫酸 含硫物质的转化,共47页。PPT课件主要包含了考点一,考点二,吸水性,脱水性,强氧化性,答案B,答案A,答案C,NH42S,H2O等内容,欢迎下载使用。
这是一份2025届高中化学全程复习构想课件全套03离子共存、离子检验与推断,共47页。PPT课件主要包含了考点一,考点二,①②③⑥,FeSCN3,答案B,不溶解,蓝色沉淀,蓝色钴玻璃,常见阴离子的检验,BaCl2溶液等内容,欢迎下载使用。
这是一份2025届高中化学全程复习构想课件全套37电解池 金属的腐蚀与防护,共60页。PPT课件主要包含了考点一,考点二,考点三,答案D,答案C,通入HCl,加CuO,NH3,电镀铜,待镀金属制品等内容,欢迎下载使用。









