
所属成套资源:湖北省重点高中智学联盟2025届高三上学期8月联考各学科试卷及答案
湖北省重点高中智学联盟2025届高三上学期8月联考化学试卷(Word版附答案)
展开
这是一份湖北省重点高中智学联盟2025届高三上学期8月联考化学试卷(Word版附答案),共12页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 S-32 Ga-70
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.我国饮食注重营养均衡,讲究“色香味形”。下列说法不正确的是
A.烹饪糖醋排骨用蔗糖炒出焦糖色,蔗糖属于寡糖
B.新鲜榨得的花生油具有独特油香,花生油的主要成分为不饱和高级脂肪酸
C.凉拌黄瓜加醋使其具有可口酸味,食醋中含有极性分子
D.端午时节用棕叶将糯米包裹成形,糯米中的淀粉属于有机高分子
2.根据材料的组成和结构变化可推测其性能变化,下列推测不合理的是
3.下列关于物质的检验、分离、提纯方法正确的是
A.用溴水鉴别苯酚和苯甲醛
B.用酸性溶液除去乙炔中硫化氢气体
C.用溶液检验溶液是否变质
D.在提纯(混有少量)晶体过程中,可采取蒸发结晶的方法
4.下列化学用语或图示表达正确的是
A.砷原子的简化电子排布式为:
B.用电子式表示的形成过程:
C.分子中键的电子云轮廓图:
D.的化学名称:—二甲基甲酰胺
5.下列方程式书写正确的是
A.向溶液中通入少量的离子方程式为:
B.向的溶液中滴加等体积等浓度的的溶液的离子方程式:
C.溶液与足量的溶液反应:
D.溶液和过量的新制溶液混合加热反应:
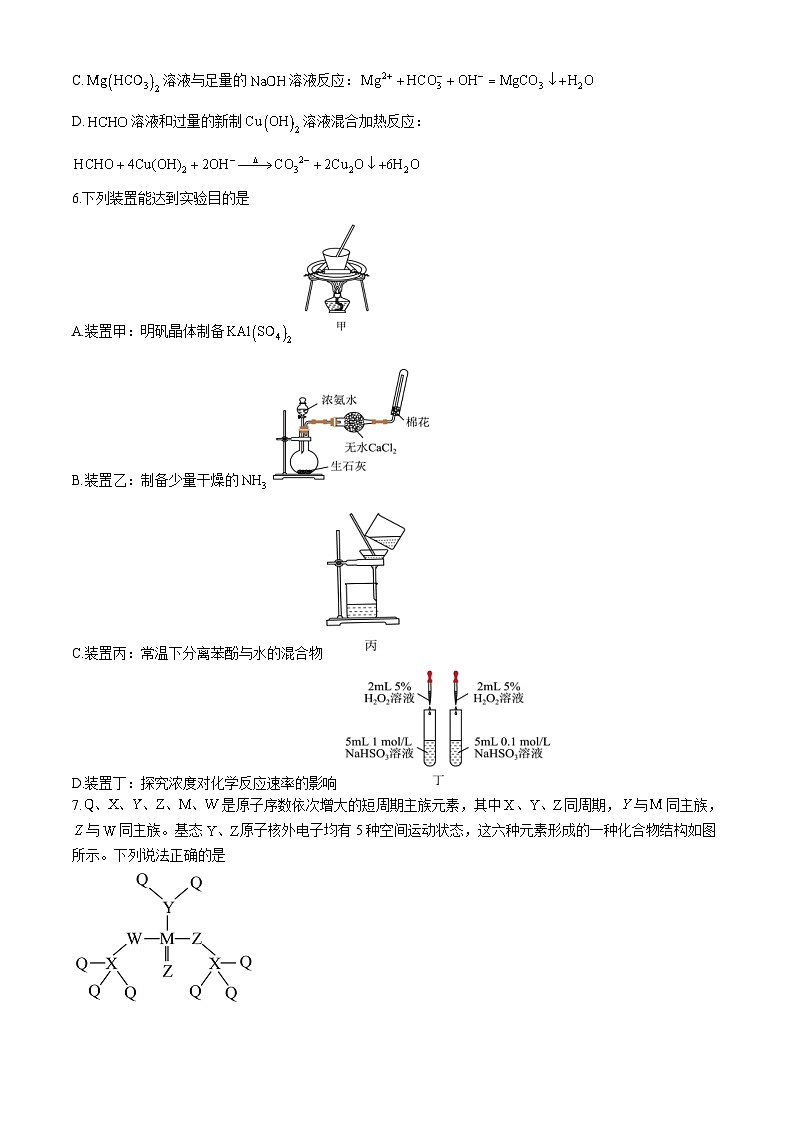
6.下列装置能达到实验目的是
A.装置甲:明矾晶体制备
B.装置乙:制备少量干燥的
C.装置丙:常温下分离苯酚与水的混合物
D.装置丁:探究浓度对化学反应速率的影响
7.是原子序数依次增大的短周期主族元素,其中同周期,与同主族,与同主族。基态原子核外电子均有5种空间运动状态,这六种元素形成的一种化合物结构如图所示。下列说法正确的是
A.电负性:
B.第一电离能:
C.和的简单氢化物的键角:
D.三种元素组成的化合物既可能呈酸性,也可能呈碱性
8.设为阿伏伽德罗常数的值,下列说法正确的是
A.的盐酸和的醋酸溶液等体积混合后,溶液中的数目仍为
B.硫酸氢钠晶体含有阳离子
C.常温下,和混合气体中含有极性键数目为
D.足量的铜与浓硝酸充分反应,转移的电子数目为
9.异靛蓝及其衍生物是一类具有生理活性的燃料,目前在有机半导体材料中有重要的应用。其部分合成路线如下:
下列说法错误的是
A.物质与足量加成后,产物分子有个3手性碳
B.向中加入足量溶液,最多与反应
C.物质中含3种官能团
D.物质核磁共振氢谱有4组峰
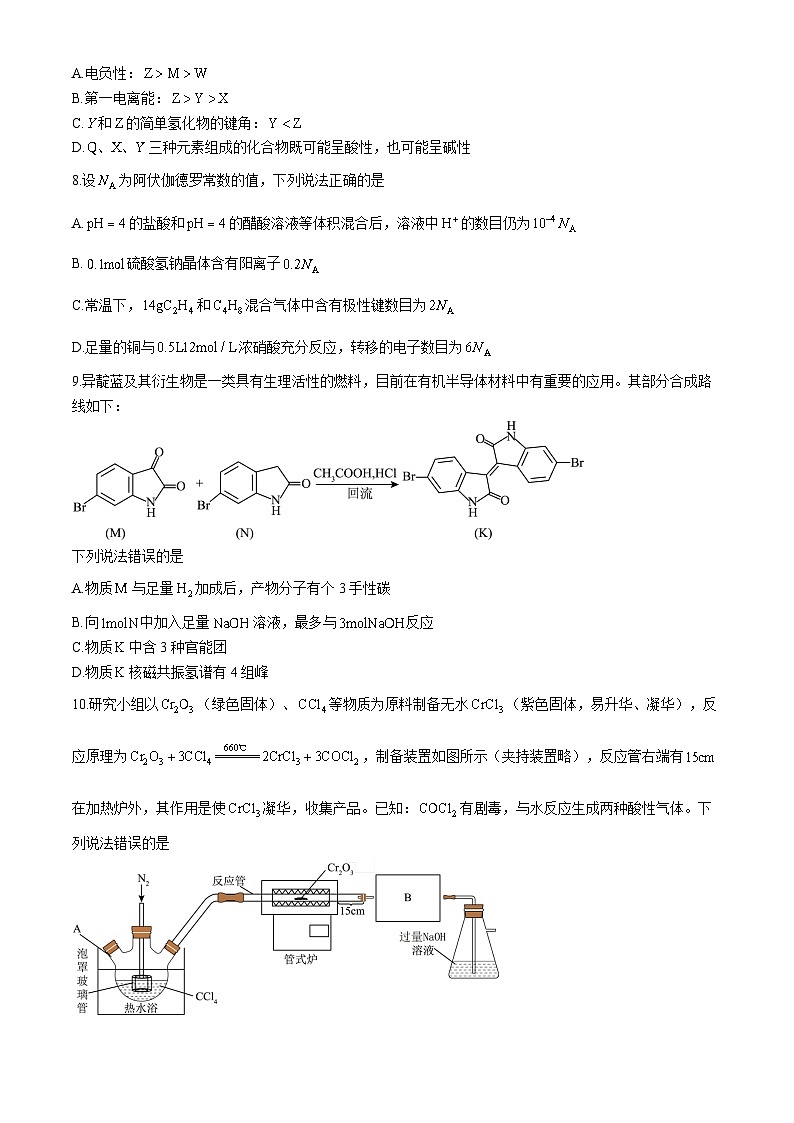
10.研究小组以(绿色固体)、等物质为原料制备无水(紫色固体,易升华、凝华),反应原理为,制备装置如图所示(夹持装置略),反应管右端有在加热炉外,其作用是使凝华,收集产品。已知:有剧毒,与水反应生成两种酸性气体。下列说法错误的是
A.实验中需持续通入,其目的为排除装置中的空气,将四氯化碳吹入反应管
B.装置处应增加一个装有浓硫酸的形管,防止锥形瓶内水蒸气进入
C.装置中锥形瓶内溶液吸收尾气后可以得到两种盐
D.当反应管中固体消失时,停止加热,待装置冷却后,停止通入
11.冠醚能与碱金属离子结合(如下图所示),是有机反应很好的催化剂,例如能加快酸性溶液与环己烯的反应速率。
用结合常数表示冠醚与碱金属离子的结合能力,结合常数越大,两者结合能力越强。
下列说法正确的是
A.冠醚通过与结合将携带进入有机相,从而加快反应速率
B.结合常数的大小与碱金属离子直径有关,与冠醚空腔直径无关
C.如图所示的实验中:①>②>③
D.为加快酸性溶液与环己烯的反应速率,选择冠醚比冠醚更合适
12.物质结构决定性质。下列有关物质性质的解释错误的是
13.采用了氮化镓元件的充电器体积小、质量轻,在发热量、效率转换上相比普通充电器也有更大的优势,被称为“快充黑科技”,下图是氮化镓的三种晶体结构(表示阿伏加德罗常数的值)。下列有关说法错误的是
A.氮化镓晶体属于共价晶体
B.图晶体结构中含有6个、6个
C.三种晶体结构中原子的配位数之比为
D.图晶体结构中若和的距离为,则晶体的密度为
14.有机电化学合成是一种环境友好的合成方法,由对硝基苯甲酸制取对氨基苯甲酸的电解装置如图所示,其中双极膜能将解离成和。
下列说法错误的是
A.端电势低于端电势
B.电解后阴极区溶液降低
C.每产生就有发生解离
D.的电极反应方程式可表示为:
15.某氨基酸衍生物(简称)的,。常温下构建体系,其中,,体系中含物种分布系数与关系如图所示,下列说法正确的是
A.
B.时
C.时,存在
D.后继续增大,溶液中的一定继续增大
二、非选择题:本题共4小题,共55分。
16.(12分)钨酸是一种重要的化工原料,用作媒染剂催化剂,制造防火材料等。一种以黑钨矿(主要成分是和,还含有等元素的杂质)为原料制备钨酸的工业流程如下图所示。
已知:①滤渣1的成分是和。
②“水浸”后滤液中主要阴离子为和。
③。
回答下列问题:
(1)基态的价电子排布式为__________。
(2)在“焙烧”时,发生反应的化学方程式为_____________________。
(3)滤渣2的主要成分的化学式是__________,加入盐酸“调节”要在加热煮沸条件下进行,煮沸的目的是______________________________。
(4)“除磷、砷”过程中元素以和形式沉淀,则“氧化”过程中加入溶液的目的是____________________。
(5)当“滤液1”中时,此时__________(填“是”或“否”)沉淀完全。
17.(14分)既是重要的清洁能源也是一种重要的化工原料。以为原料合成涉及的主要反应如下:I:
II:
已知:①常温常压下,和的燃烧热分别为和;
② 。
(1)_________。
(2)下列不能说明在恒温恒容的密闭容器中发生反应I和反应II达到平衡状态的是_______。
A.混合气体气体密度不再变化B.混合气体的平均摩尔质量不再变化
C.容器内的压强不再变化D.的体积分数不再变化
(3)在密闭容器中通入和,分别在压强为和下进行反应。实验中对平衡体系中的三种物质进行分析,其中和的平衡体积分数受温度的影响如图所示。
①时,表示和平衡体积分数随温度变化关系的曲线分别是________和________。点平衡体积分数高于点的原因是_________________________。
②图中当和平衡体积分数均为时,若容器的体积为,则该温度下反应I的平衡常数的值为________________。(保留三位有效数字)。
(3)利用超干重整是减少温室气体的一种有效方式,其催化转化原理如图所示:
①与超干重整总反应的化学方程式为________________________。
②有关转化过程,下列说法正确的是________(填序号)。
A.过程I中未参与反应
B.过程II实现了含碳物质与含氢物质的分离
C.转化②中消耗过程中的,有利于反应正向进行
D.转化③中与反应的物质的量之比为
18.(15分)是常见的化学试剂,某小组利用废铜屑“湿法”制备并开展相关探究。
已知:氯化铜在不同温度下结晶形成的结晶水合物
回答下列问题:
(1)仪器的名称为_________。
(2)上述方法制备的离子方程式为___________________________。
(3)为得到纯净的晶体,反应完全后要进行的操作是:除去其他可能的金属离子后,过滤,向滤液中持续通入气体,加热蒸发浓缩,__________________,过滤,洗涤,低温干燥。持续通入气体的目的是___________________________。
(4)实验中,的实际用量要大于理论用量,可能因素为:原因1:__________________;原因2:生成的催化了的分解。
(5)该小组对“原因2”进行拓展探究。为验证对分解的催化作用,该小组向5支盛有的试管中滴加不同溶液,实验记录如下表(忽略溶液体积的微小变化:已知一定条件下,还原产物的浓度越小,氧化剂的氧化性越强):
①实验IV过程中观察到有白色沉淀(经检验为)生成,反应的机理表示为:
第一步:;
第二步:__________________________________(写离子方程式)。
②已知化学反应速率第一步
相关试卷
这是一份湖北省重点高中智学联盟2023-2024学年高一化学上学期10月联考试题(Word版附解析),共3页。试卷主要包含了 下列说法中正确的有, 关于物质分类的正确组合是等内容,欢迎下载使用。
这是一份2024湖北省重点高中智学联盟高三上学期10月联考化学试题含答案,共12页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
这是一份2024湖北省重点高中智学联盟高三上学期10月联考化学试题含答案,共12页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。









