






还剩15页未读,
继续阅读
成套系列资料,整套一键下载
高中化学第一节 物质的分类优质ppt课件
展开
这是一份高中化学第一节 物质的分类优质ppt课件,共23页。PPT课件主要包含了你认识他们吗,组织建设,思考与交流,纯净物,金属单质,非金属单质,化合物,氧化物,混合物,稀有气体单质等内容,欢迎下载使用。
图书馆里有许许多多的书籍,为什么你很快就能找到你需要的书呢?
分类是学习和研究化学物质及其变化的一种常用的科学方法。
第一节 物质的分类(第1课时 简单分类法及其应用)
第二章 化学物质及其变化
一、简单分类法及其应用
1.分类:把某些特征相似的事物归类到一起的方法
试想想:没有分类的世界的模样会怎样?
分类的目的和意义:能够提高人们工作、学习的效率,使人们更快更便捷的达到目的。
1、请回顾初中学过哪些有关物质类别的概念?
混合物、纯净物、单质、化合物、金属单质、非金属单质、稀有气体单质、酸、碱、盐、氧化物
2、请大家用已有知识对上述概念进行分类,并用图示把这些概念的相互关系表示出来?
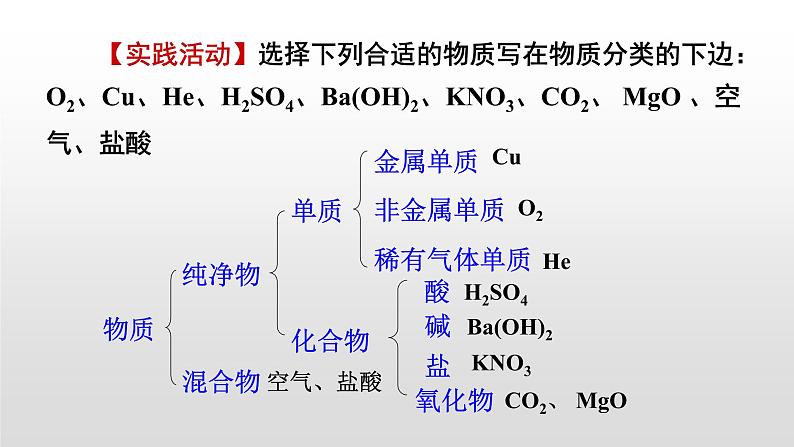
【实践活动】选择下列合适的物质写在物质分类的下边:O2、Cu、He、H2SO4、Ba(OH)2、KNO3、CO2、 MgO 、空气、盐酸
(1)树状分类法 对同类事物按同一标准进行再分类的方法。
树状分类法的分类原则:同一层次的物质类别间一般是相互独立,没有交叉的。(同层次间为并列关系,不同层次之间为从属关系)
树状分类法
树状分类法特征:把大范围的事物进行细分, 对事物认识更加深刻。
例.用交叉分类法对下列物质进行分类
(2)交叉分类法 根据不同的分类标准,对同一事物进行多种分类的一种方法
交叉分类法的特征:同时可依照多种标准对号入座进行分类,对事物认识较全面,弥补单一分类方法的不足。
【小试牛刀】请大家用交叉分类法对下列物质分类Na2SO4 钠盐NaNO3 钾盐Na2CO3 硝酸盐K2SO4 碳酸盐K2CO3 硫酸盐KCl 盐酸盐NaCl
1.定义:电离时生成的阳离子全部是氢离子(H+)的化合物叫做酸
HCl、HBr、HNO3、CH3COOH
H2SO4、H2CO3、H2C2O4
H2SO4、 HNO3 、H3PO4 、 H2CO3
HCl、HBr、HI、HF、H2S
HNO3、HCl、HF、HBr、HI、H2S
H2SO4、H3PO4
HCl、HBr、HNO3、H2SO4 、HI、HClO4
H2SO3、H3PO4、H2C2O4
H2CO3、CH3COOH、HF
KOH、、NaOH、、Ba(OH)2、、NH3·H2O
Cu(OH)2、Fe(OH)3、、Mg(OH)2
1.定义:电离时生成的阴离子全部是氢氧根离子的化合物
NaOH(烧碱)、KOH、Ba(OH)2
Fe(OH)3、NH3·H2O
NaOH、 NH3·H2O、KOH
Ba(OH)2、Ca(OH)2
K+、Na+ 、NH4+、Cu2+、Ca2+
NO3-、SO42-、、Cl-、、CO32-、、PO43-
K+、、Na+、NH4+、NO3-、SO42-、Cl-
CO32-、PO43-、AgCl、BaSO4
组成中是否有可电离的H、OH
既不含能电离的氢离子,又不含氢氧根离子的盐:Na2CO3、KCl、Ba(NO3)2
电离时生成的阳离子除金属离子(或NH4+)外还有氢原子,阴离子为酸根离子的盐。NaHCO3、Ca(HCO3)2
1.定义:阳离子由金属离子或NH4+、阴离子由酸根离子组成的化合物
电离时生成的阴离子除酸根外,还有氢氧原子团,阴离子为金属离子(或NH4+)离子的盐。Cu2(OH)2CO3
金属氧化物:非金属氧化物:
CuO MgO CaO
1.定义:元素与氧化合生成的化合物。有且只有两种元素组成
能与酸反应只生成盐和水的氧化物
能与碱起反应只生成盐和水的氧化物
Na2O、CaO、Fe2O3
既能与酸又能与碱起反应,且均只生成盐和水的氧化物
1.下列化合物中依次属于氧化物、碱、盐的一组是( ) A. Na2CO3、KOH、CaO B. CO、NaOH、KCl C. H2O、H2SO4、NaCl D.CuO、Cu2(OH)2CO3、CaCO3
2.按照物质的树状分类和交叉分类,HNO3应属于( ) ①酸;②氢化物;③氧化物;④含氧酸;⑤难挥发性酸;⑥一元酸;⑦化合物 A.①②③④⑤⑥⑦ B.①④⑥⑦ C.①⑧ D.①④⑤⑥⑦
图书馆里有许许多多的书籍,为什么你很快就能找到你需要的书呢?
分类是学习和研究化学物质及其变化的一种常用的科学方法。
第一节 物质的分类(第1课时 简单分类法及其应用)
第二章 化学物质及其变化
一、简单分类法及其应用
1.分类:把某些特征相似的事物归类到一起的方法
试想想:没有分类的世界的模样会怎样?
分类的目的和意义:能够提高人们工作、学习的效率,使人们更快更便捷的达到目的。
1、请回顾初中学过哪些有关物质类别的概念?
混合物、纯净物、单质、化合物、金属单质、非金属单质、稀有气体单质、酸、碱、盐、氧化物
2、请大家用已有知识对上述概念进行分类,并用图示把这些概念的相互关系表示出来?
【实践活动】选择下列合适的物质写在物质分类的下边:O2、Cu、He、H2SO4、Ba(OH)2、KNO3、CO2、 MgO 、空气、盐酸
(1)树状分类法 对同类事物按同一标准进行再分类的方法。
树状分类法的分类原则:同一层次的物质类别间一般是相互独立,没有交叉的。(同层次间为并列关系,不同层次之间为从属关系)
树状分类法
树状分类法特征:把大范围的事物进行细分, 对事物认识更加深刻。
例.用交叉分类法对下列物质进行分类
(2)交叉分类法 根据不同的分类标准,对同一事物进行多种分类的一种方法
交叉分类法的特征:同时可依照多种标准对号入座进行分类,对事物认识较全面,弥补单一分类方法的不足。
【小试牛刀】请大家用交叉分类法对下列物质分类Na2SO4 钠盐NaNO3 钾盐Na2CO3 硝酸盐K2SO4 碳酸盐K2CO3 硫酸盐KCl 盐酸盐NaCl
1.定义:电离时生成的阳离子全部是氢离子(H+)的化合物叫做酸
HCl、HBr、HNO3、CH3COOH
H2SO4、H2CO3、H2C2O4
H2SO4、 HNO3 、H3PO4 、 H2CO3
HCl、HBr、HI、HF、H2S
HNO3、HCl、HF、HBr、HI、H2S
H2SO4、H3PO4
HCl、HBr、HNO3、H2SO4 、HI、HClO4
H2SO3、H3PO4、H2C2O4
H2CO3、CH3COOH、HF
KOH、、NaOH、、Ba(OH)2、、NH3·H2O
Cu(OH)2、Fe(OH)3、、Mg(OH)2
1.定义:电离时生成的阴离子全部是氢氧根离子的化合物
NaOH(烧碱)、KOH、Ba(OH)2
Fe(OH)3、NH3·H2O
NaOH、 NH3·H2O、KOH
Ba(OH)2、Ca(OH)2
K+、Na+ 、NH4+、Cu2+、Ca2+
NO3-、SO42-、、Cl-、、CO32-、、PO43-
K+、、Na+、NH4+、NO3-、SO42-、Cl-
CO32-、PO43-、AgCl、BaSO4
组成中是否有可电离的H、OH
既不含能电离的氢离子,又不含氢氧根离子的盐:Na2CO3、KCl、Ba(NO3)2
电离时生成的阳离子除金属离子(或NH4+)外还有氢原子,阴离子为酸根离子的盐。NaHCO3、Ca(HCO3)2
1.定义:阳离子由金属离子或NH4+、阴离子由酸根离子组成的化合物
电离时生成的阴离子除酸根外,还有氢氧原子团,阴离子为金属离子(或NH4+)离子的盐。Cu2(OH)2CO3
金属氧化物:非金属氧化物:
CuO MgO CaO
1.定义:元素与氧化合生成的化合物。有且只有两种元素组成
能与酸反应只生成盐和水的氧化物
能与碱起反应只生成盐和水的氧化物
Na2O、CaO、Fe2O3
既能与酸又能与碱起反应,且均只生成盐和水的氧化物
1.下列化合物中依次属于氧化物、碱、盐的一组是( ) A. Na2CO3、KOH、CaO B. CO、NaOH、KCl C. H2O、H2SO4、NaCl D.CuO、Cu2(OH)2CO3、CaCO3
2.按照物质的树状分类和交叉分类,HNO3应属于( ) ①酸;②氢化物;③氧化物;④含氧酸;⑤难挥发性酸;⑥一元酸;⑦化合物 A.①②③④⑤⑥⑦ B.①④⑥⑦ C.①⑧ D.①④⑤⑥⑦














