





高中化学人教版 (新课标)必修1第三章 金属及其化合物第一节 金属的化学性质精品课件ppt
展开位于金属活动性顺序表中氢(H)之前的金属都能与酸发生化学反应,金属越活泼越容易与酸反应。
Fe+2HCl=FeCl2+H2↑
2Al+6HCl=2AlCl3+3H2 ↑
2Na+2HCl=2NaCl+H2 ↑
Mg+2HCl=MgCl2+H2 ↑
【注意】钠与酸反应时,如酸过量则钠只与酸反应,如酸不足则钠先与酸反应再与水反应。
【小试牛刀】将11.5 g钠、28 g铁分别投入200 mL 1 ml·L-1的盐酸中,结果正确的是( ) A.钠与盐酸反应最剧烈,产生的气体最多 B.铁与盐酸反应最剧烈 C.铁与盐酸反应产生的气体比钠多 D.反应结束时产生的气体一样多
活泼金属可将不活泼金属从它的盐溶液中置换出来
四、金属与盐溶液的反应
金属与盐溶液的反应一般遵循强置弱,前置后的规律
将Na投入CuSO4稀溶液中可能发生什么反应?将会看到什么现象?
浮在水面、熔成小球、四处游动、有蓝色沉淀产生。
思考: 钠为什么不能置换CuSO4溶液中的铜,却产生蓝色沉淀?由此推测,钠和CuSO4溶液发生了哪些反应?请写出反应的离子方程式。
【小试牛刀】将适量金属钠投入下列溶液中,有气体放出,但无沉淀生成的是( ) A.盐酸 B.饱和氢氧化钠溶液 C.FeCl3溶液 D.CuSO4溶液
【再来一刀】能正确表示下列反应的离子方程式的是( ) A.钠与水反应:Na+2H2O=Na++2OH-+H2↑ B.钠与CuSO4溶液反应:2Na+Cu2+=Cu+2Na+ C.钠与盐酸反应:Na+2H+=Na++H2↑ D.钠与氯化钾溶液反应:2Na+2H2O=2Na++2OH-+H2↑
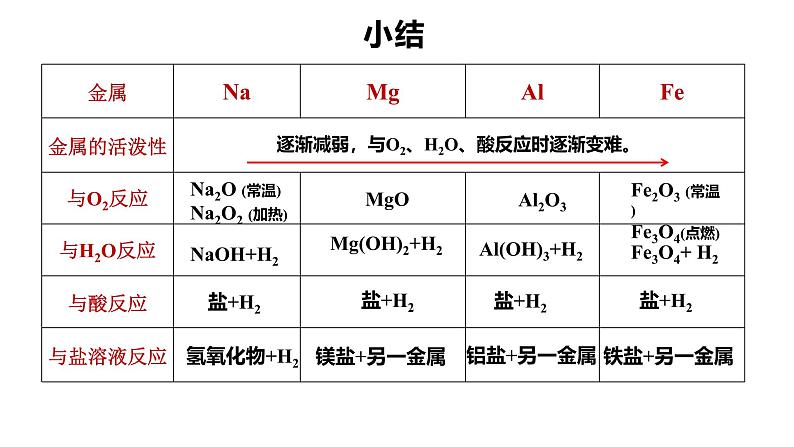
Na2O (常温)Na2O2 (加热)
Fe2O3 (常温)Fe3O4(点燃)
五、铝与氢氧化钠溶液的反应
铝片放入盐酸、NaOH溶液中都有气泡产生
为什么铝与盐酸、氢氧化钠溶液的反应开始时气体产生的速度较慢,而后越来越快?
因为开始时是铝表面的氧化膜先发生作用,氧化膜反应完全以后才有H2产生,且随着反应的进行,温度升高,反应速度也加快。
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
铝的特殊性:既能跟酸反应产生H2,又能跟强碱溶液反应产生H2。
【例题1】5.4 g Al与足量的NaOH溶液反应,求生成的气体在标况下的体积?若是足量的盐酸呢?
2Al~2NaOH~3H2↑
2Al~6HCl~3H2↑
5.4 g (即0.2ml)Al
~H2(0.3ml),标况下6.72L。
2Al+2NaOH+2H2O=2NaAlO2+3H2↑
【例题2】Mg、Al组成的混合物与足量盐酸反应,产生标准状况下的氢气4.48 L,下列推断中不正确的是( ) A.参加反应的Mg、Al共0.2 ml B.参加反应的HCl为0.4 ml C.Mg、Al在反应中共失去0.4 ml电子 D.若与足量的稀硫酸反应能产生0.2 ml H2
【小试牛刀】2Al+2NaOH+2H2O=2NaAlO2+3H2↑可用来疏通下水管道。下列说法错误的是( ) A.Al是还原剂,发生氧化反应 B.每生成1mlH2,转移2ml电子 C.可用NaOH溶液除去镁粉中混有的少量Al粉 D.等量的铝与足量NaOH溶液反应生成的H2比与足量盐酸的多
【再来一刀】等量的铝与等量的盐酸和NaOH溶液反应产生氢气体积比为4:5,则反应可能情况为( ) A.恰好反应 B.酸过量 C.碱过量 D.酸碱均过量
六、物质的量在化学方程式计算中的应用
【口诀】上下单位对齐、左右单位相当
2个 2个 2个 2个 3个
2NA 2NA 2NA 2NA 3NA
2ml 2ml 2ml 2ml 3ml
54g 80g 36g 164g 6g
【小试牛刀】将0.46 g金属钠投入足量的水中,充分反应后配制成体积为0.1 L的溶液,所得溶液中溶质的物质的量浓度为( ) A.0.1 ml/L B.0.2 ml/L C.0.8 ml/L D.0.4 ml/L
【再来一刀】完全沉淀等物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl-,消耗等物质的量浓度的AgNO3溶液的体积比为3∶2∶1,则上述溶液的体积比为( ) A.1∶1∶1 B.3∶2∶1 C.6∶3∶2 D.9∶3∶1
1.等质量的甲、乙、丙三种金属,分别与足量的溶质质量分数相同的稀硫酸完全反应都生成+2价的硫酸盐,其产生氢气的体积与反应时间的关系如图所示,则下列说法正确的是( )
A.三种金属的活动性顺序为甲>乙>丙B.反应时消耗硫酸的质量一定相同C.三种金属的相对原子质量大小顺序是甲>乙>丙D.甲先反应完,乙最后反应完
高中化学人教版 (新课标)必修1第一节 金属的化学性质获奖ppt课件: 这是一份高中化学人教版 (新课标)必修1<a href="/hx/tb_c21521_t3/?tag_id=26" target="_blank">第一节 金属的化学性质获奖ppt课件</a>,共23页。PPT课件主要包含了组织建设,含量特征,存在形式,物理通性,金属的颜色光泽,延展性,金属的通性,思考与交流,化学通性,一钠与氧气的反应等内容,欢迎下载使用。
高中化学人教版 (新课标)必修1第三节 氧化还原反应优秀课件ppt: 这是一份高中化学人教版 (新课标)必修1<a href="/hx/tb_c21518_t3/?tag_id=26" target="_blank">第三节 氧化还原反应优秀课件ppt</a>,共19页。PPT课件主要包含了从得失氧的角度,氧化反应,物质得到氧的反应,还原反应,物质失去氧的反应,氧化还原反应,NaCl的形成过程,Na+,HCl的形成过程,从电子转移的角度等内容,欢迎下载使用。
人教版 (2019)选择性必修1第三章 水溶液中的离子反应与平衡第三节 盐类的水解评课ppt课件: 这是一份人教版 (2019)选择性必修1第三章 水溶液中的离子反应与平衡第三节 盐类的水解评课ppt课件,共24页。PPT课件主要包含了课程目标,基础•初探,☂名师点拨,课堂•专练,2实质,盐类水解的规律等内容,欢迎下载使用。













