




- 浙教版科学九上科学1.1物质的变化学案 学案 1 次下载
- 浙教版科学九上科学1.2物质的酸碱性学案 学案 1 次下载
- 浙教版科学九上科学1.4常见的碱第一课时学案 学案 1 次下载
- 浙教版科学九上科学1.4常见的碱第二课时学案 学案 1 次下载
- 浙教版科学九上科学1.5酸碱之间的反应学案 学案 1 次下载
科学九年级上册第3节 常见的酸第一课时导学案
展开一.酸的通性教育网
1.酸能使紫色石蕊试液变 ,无色酚酞试液 ;
2.将锌、铁等金属放入酸中,有气泡产生。经检验,该气体能燃烧,并发出淡蓝色的火焰,气体是 。这说明酸能和某些金属反应生成氢气。
写出锌、铁与硫酸,铝、镁和盐酸反应的化学方程式:
、 ;
、 ;
应用:制取氢气。
3.将生锈的铁钉放入硫酸中,铁锈会消失,并生成 色溶液,一段时间后会有气泡产生。
这说明酸能和金属氧化物反应生成盐和水。请写出生锈的铁钉与硫酸反应的化学方程式: 、 氧化铜、氧化镁等也能与酸反应,请写出与盐酸反应的方程式: 、 应用:金属除锈。
4.在蓝色的氢氧化铜沉淀中加入盐酸,沉淀会溶解,变为蓝色溶液。
这说明酸能和碱反应产生盐和水。请写出氢氧化铜和盐酸,氢氧化铁和硫酸反应的方程式: 、 ;
应用:除去酸性或碱性物质。 如胃酸过多,需服用胃舒平A1(OH)3 ,写出方程式: ;
5. 在石灰石、大理石上滴加盐酸,有气泡产生,该气体能使燃烧的木条熄灭,该气体是 。
这说明酸能和某些盐反应。写出石灰石和盐酸反应的方程式: 。
此外,盐酸还能和硝酸银反应;硫酸还能和氯化钡反应,写出方程式: 、 ;
应用:制取二氧化碳(实验室一般只用石灰石或大理石和稀盐酸反应制取,不用浓盐酸是因为 ;不用稀硫酸是因为 )由上述反应可总结出酸的通性酸的通性:
(1)能使酸碱指示剂变色,能使紫色石蕊试液变 ,无色酚酞 。
(2)金属 + 酸 = + ;
(3)金属氧化物 + 酸 = 盐 + ;
(4) + 酸 = 盐 + 水。
(5)盐 + 酸 = 新盐 + 。
特别提醒:酸之所以有共性,是因为它们都能电离出共同的 。
二.特殊酸的个性
(一)盐酸的物理性质
(1)组成:是氯化氢的水溶液(混合物) 。
(2)纯盐酸是无色透明的液体,工业盐酸因含杂质,而显黄色(铁离子存在)。
(3)浓盐酸是无色,有刺激性气味和酸味的液体,具有挥发性和腐蚀性。跟空气中的水蒸气重新结合成盐酸的小液滴(即白雾),挥发后质量和浓度均变小。
特别提醒: 闻溶液气味的方法是:用手在瓶口轻轻扇动,使少许气体飘进鼻孔,千万不要直接凑近鼻子闻,因为这样做很危险!
(二)硫酸和硝酸
1、硫酸的物理性质
纯硫酸是一种无色油状液体。常用的浓硫酸中H2SO4的质量分数为98.3%,其密度为1.84g·cm-3。硫酸是一种高沸点难挥发的强酸,易溶于水,能以任意比与水混溶。浓硫酸溶解时放出大量的热,因此浓硫酸稀释时应该把浓硫酸沿着器壁(或玻璃棒)慢慢地注入水里,并不断搅拌。若将水倒入浓硫酸中,温度可达到173℃,导致酸液飞溅。
浓硫酸具有吸水性,因此将一瓶浓硫酸敞口放置在空气中,其质量将变大,密度将减小,浓度变小,体积增大,这是因为浓硫酸具有吸水性。
特别提醒:(1)就硫酸而言,吸水性是浓硫酸的性质,而不是稀硫酸的性质。
(2)浓硫酸吸水的过程是物理变化的过程,吸水性是浓硫酸的物理性质。
(3)浓硫酸不仅能吸收一般的游离态水(如空气中的水),而且还能吸收某些结晶水合物(如CuSO4· 5H2O、Na2CO3·10H2O)中的水。
2、硫酸的化学性质
浓硫酸具有脱水性,吸水性和腐蚀性。
(1)脱水性
= 1 \* GB3 \* MERGEFORMAT ①就硫酸而言,脱水性是浓硫酸的性质,而非稀硫酸的性质,即浓硫酸有脱水性且脱水性很强。
= 2 \* GB3 \* MERGEFORMAT ②物质被浓硫酸脱水的过程是 变化的过程,反应时,浓硫酸按水分子中氢氧原子数的比(2∶1)夺取被脱水物中的氢原子和氧原子。
= 3 \* GB3 \* MERGEFORMAT ③可被浓硫酸脱水的物质一般为含氢、氧元素的有机物,其中蔗糖、木屑、纸屑和棉花等物质中的有机物,被脱水后生成了黑色的炭(碳化)。 如C12H22O11————>12C + 11H2O .
(2)腐蚀性:如果浓硫酸不小心滴到手上,应马上用干抹布抹去,然后用大量的水(或小苏打水)冲洗
二、课堂练习
考点1.酸的通性掌握(与指示剂,金属氧化物,碱)
例1.盐酸(HCl)是实验室的重要物质,能与许多物质反应。关于如图所示的概念图,下列描述中正确的是( )
A.X不可能是H2O
B.Y可能是硫酸钡
C.若W呈红色,则指示剂可能是无色酚酞试液
D.碱可以是可溶性碱,也可以是难溶性碱
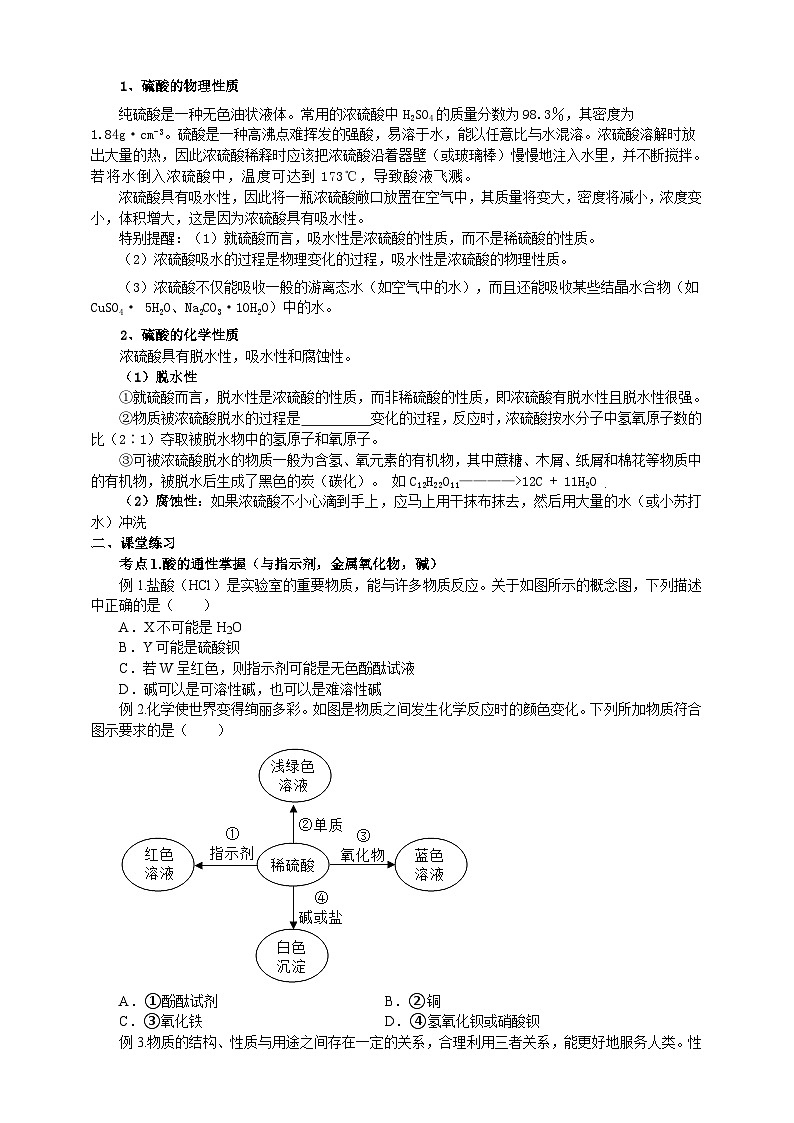
例2.化学使世界变得绚丽多彩。如图是物质之间发生化学反应时的颜色变化。下列所加物质符合图示要求的是( )
A.①酚酞试剂B.②铜
C.③氧化铁D.④氢氧化钡或硝酸钡
例3.物质的结构、性质与用途之间存在一定的关系,合理利用三者关系,能更好地服务人类。性质一用途:稀硫酸能去除钢铁表面的铁锈(氧化铁),这是利用其化学性质中( )
A.能与某些碱反应
B.能与某些金属反应
C.能与某些盐反应
D.能与某些金属氧化物反应
例4.构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的知识网络图:“﹣”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
A.CO2、Ba(OH)2、CuSO4B.Ba(OH)2、HNO3、K2CO3
C.KOH、FeCl3、CaCO3D.NaOH、BaCl2、H2SO4
变式训练1.向稀盐酸中加入Z物质,其pH变化情况如图所示,则Z物质是( )
A.H2OB.AgNO3固体C.浓盐酸D.KOH固体
变式训练2.如图是小科以稀硫酸为主题绘制的“多彩酸世界”思维导图,下列说法正确的是( )
A.实验①中酚酞试液滴入稀硫酸中可使溶液变成红色
B.实验②中稀硫酸与CuCl2溶液反应可得到蓝色溶液
C.实验③中稀硫酸与铁钉反应还可观察到有气泡生成
D.实验⑤中稀硫酸与Na2CO3溶液反应可产生白色沉淀
变式训练3.探索稀盐酸的性质时,向一定量的氧化铜固体中逐滴加入稀盐酸,容器中溶液总质量随时间的变化图像如图所示。下列说法正确的是( )
A.该图像也能反映溶液中溶剂质量随时间的变化关系
B.m点到n点的过程中,溶液中氯化铜质量逐渐增加
C.p点对应的溶液中,一定含有两种不同的溶质
D.m点和n点对应溶液蒸发结晶后得到的固体不同
变式训练4.一定质量的稀硫酸与足量氧化铜粉末发生反应时,容器中溶液的总质量随时间的变化曲线如图所示。下列说法中正确的是( )
①该实验是将氧化铜粉末加入到盛有稀硫酸的容器中
②该图像还可反映溶液质量随加入氧化铜质量的变化趋势
③a点和b点均能表示稀硫酸和氧化铜恰好完全反应
④a点和b点对应溶液的颜色深浅不同
⑤a点和b点对应溶液中铜元素质量相同
A.①②⑤B.①③⑤C.②④⑤D.②③⑤
变式训练5.物质的结构决定性质。某同学对稀硫酸和稀盐酸的结构关系用如图所示表示。在图中的②位置表示的是稀硫酸和稀盐酸共有的结构成分是 (用符号表示);请根据稀硫酸和稀盐酸的结构差异鉴别这两种溶液 (用化学方程式表示,写一个即可)。
变式训练6.如图是某同学在复习科学时构建酸通性的“手掌图”,其中五个手指表示能与酸发生化学反应的五类物质。
(1)“小拇指”上漏填的这类物质是 。
(2)铁锈对应“小拇指”类,它与盐酸反应的化学方程式为 。
变式训练7.氧化物、酸、碱、盐相互之间的关系是初中科学中重要学习内容之一。现有如图所示的转换关系。
(1)请写出下列物质的化学式B 。
(2)CuO与A溶液反应的实验现象为 。
变式训练8.某兴趣小组同学进行如图甲所示的实验。实验结束后,他们把A、B两支试管中的物质倒入乙图烧杯中,充分混合后观察到有红褐色絮状沉淀生成,溶液呈黄色。
(1)图甲中A试管充分反应后,有剩余的反应物为 。
(2)通过以上现象能确定烧杯中溶液含有的溶质是 。
变式训练9.化学使世界变得绚丽多彩。如图是物质之间发生化学反应时的颜色变化。
(1)编号②处的物质是 (填化学式,下同);蓝色溶液的溶质是 。
(2)编号①指示剂可以为 。
(3)若编号④的选用的物质是氢氧化钡,请你写出该反应的化学方程式: 。
变式训练10.如图是小科构建的硫酸部分知识网络,其中“—”表示相连物质能发生化学反应。
(1)石蕊试液在H2SO4溶液中显红色,该溶液中能使石蕊试液变红的离子是 。
(2)在实验室中常用浓硫酸做干燥剂,这是利用它的 。
(3)硫酸与4种物质发生的化学反应中,没有体现酸的通性的方程式是: 。
变式训练11.归纳是学习的重要方法,小红在复习盐酸的性质时,归纳出了盐酸的一些化学性质。(如图所示,连线表示两种物质可发生反应)
(1)写出图中A所代表的一种物质: 。
(2)镁和锌可以用来验证盐酸的性质②,小红要探究镁和锌与盐酸反应的快慢,需要控制不变(相同)的量是 。
A.两种金属的形状
B.盐酸的质量分数
C.反应容器的大小
D.温度
变式训练12.小明为探究酸、碱、盐的化学性质,做了如图实验:
(1)实验后液体颜色变红的试管是 ;
(2)反应后试管C溶液中一定存在的大量阳离子是 ;
(3)小明把D、E反应后的液体倒入一个洁净的烧杯中,观察到只有白色沉淀生成,过滤后得到白色沉淀和无色滤液,小明分别对试管D、E反应时的反应物用量有如下描述,正确的是 。
A.试管D中氢氧化钙溶液一定过量
B.试管D中稀盐酸可能过量
C.试管E中碳酸钠一定过量
D.试管E中稀盐酸一定过量
变式训练13.细心的灵灵同学观察到老师演示的“酸与氧化铜粉末反应”的实验时,发现向少量CuO粉末的试管中加入6毫升盐酸,观察到黑色粉末很快溶解,并得到蓝绿色溶液。而向放有少量CuO粉末的试管中加入6毫升硫酸溶液,常温下无明显现象。为什么会产生这种差异呢?他对此进行了科学探究:
[建立猜想]CuO
①两种酸溶液的pH不同。(注:pH相同,则单位体积溶液中H+数目相同)
②两种酸溶液中的 不同。
[实验过程]针对猜想②进行实验如下:
第4次实验中空格处该填什么。
[实验结论]常温下,pH相同的盐酸和硫酸溶液与氧化铜反应现象出现差异的原因是由于 促进了反应的进行。
变式训练14.如图实验所示是酸碱中和反应的实验研究。
(1)为探究图①反应后稀盐酸是否过量,可选用的试剂有 。
A.氢氧化钙溶液
B.锌粒
C.碳酸钠溶液
D.紫色石蕊试液
(2)图①实验,烧杯中的各个量随稀盐酸的滴入变化情况示意图如图,其中不正确的有 。
考点2.酸的个性掌握
例1.下列物质敞口放置在空气中,一段时间后会变质的是( )
A.氯化钠B.氢氧化钠C.浓硫酸D.大理石
例2.下列药品敞口放置一段时间,质量会明显减小的是( )
A.浓硫酸B.浓盐酸
C.硫酸铜粉末D.氯化钠固体
例3.下列说法正确的是( )
A.浓盐酸敞口放置一段时间后,溶液的质量增加
B.浓盐酸在空气中会冒白烟
C.浓盐酸敞口放置一段时间后,溶液的溶质质量分数会减小
D.浓盐酸敞口放置一段时间后,溶液的溶质质量分数会增大
例4.用玻璃棒蘸取浓硫酸在纸上写字,过一会儿字迹会变黑,这说明浓硫酸具有( )
A.酸性B.碱性C.吸水性D.脱水性
变式训练1.盛放药品的试剂瓶,敞口放置一段时间,药品由于发生变质导致溶液质量减小的是( )
A.氢氧化钠溶液B.氢氧化钙溶液
C.浓硫酸D.浓盐酸
变式训练2.下列物质敞口放置在空气中质量会增加的是( )
①浓硫酸
②浓盐酸
③碳酸钠晶体
④烧碱
⑤生石灰
A.①④⑤B.①③④⑤C.①②③④⑤D.①③④
变式训练3.下列物质露置在空气中,质量增加且会变质的是( )
A.浓硫酸B.浓盐酸C.氢氧化钠D.碳酸钙
变式训练4.盐酸、硫酸是实验室和工业上常用的酸。请回答下列问题:
(1)打开浓盐酸的瓶塞,看到瓶口有白雾形成,这是因为浓盐酸具有 性。
(2)用毛笔蘸取稀硫酸在竹片上画花,然后把竹片放在小火上烘干,再用水洗净,在竹片上就得到一幅精美的呈黑色或褐色的竹片画。在烘干的过程中稀硫酸变为浓硫酸,在制作竹片画的过程中利用了浓硫酸的 性。
(3)在加热的条件下浓硫酸与铜反应的化学方程式是Cu+2H2SO4(浓)CuSO4+SO2↑+2X,则X的化学式是 。
三.课后作业
1.小金想要研究酸的性质,开展了一系列实验,如图所示。下列说法正确的是( )
A.实验②和③中产生的气体种类相同
B.实验④和⑤中溶液变色现象相同
C.由实验①的现象可知稀硫酸具有酸性
D.实验③是小苏打治疗胃酸过多的反应
2.归纳总结、对比分析是常用的学习方法。如图所示:两圆重叠的区域表示两种物质的共同特征(相似点),重叠区域以外的部分表示它们的独有特征(不同点),某同学对(甲)(乙)(丙)(丁)区域相对应的内容填写正确的是( )
A.(甲):能使酚酞试液变色
B.(乙):跟所有非金属氧化物反应
C.(丙):由氢、氧原子组成
D.(丁):可以用于制取氧气
3.稀硫酸、稀盐酸以及其它的酸溶液中都含有氢离子,所以它们具有相似的化学性质,这就是酸的通性。下列有关稀硫酸的实验中,不能体现酸的通性的是( )
A.NaOHB.Ba(NO3)2C.Fe粉D.CuO粉末
4.胃酸过多的患者可以服用胃舒平来缓解不适症状,你认为胃舒平是呈( )
A.中性B.酸性C.碱性D.无法判断
5.下列试剂敞口放置于空气中,溶液的质量减轻的是(不考虑溶剂的蒸发)( )
A.浓硫酸B.烧碱溶液
C.澄清石灰水D.饱和硫酸铜溶液
6.天平的左端和右端分别放着盛有浓盐酸和浓硫酸的敞口烧杯,过段时间后,天平( )
A.左端下沉B.右端下沉C.仍平衡D.无法判断
7.思维导图有利于系统地归纳整理知识。如图为硫酸相关知识的思维导图,下列叙述中正确的是( )
A.若金属为Mg和Cu,分别加入稀硫酸中,金属表面都能产生气泡
B.若金属氧化物是Fe2O3,可用稀硫酸与Fe2O3反应制取FeSO4
C.若碱为NaOH,可以在氢氧化钠溶液中滴加酚酞试液,证明两者发生了反应
D.若盐为Na2CO3,则反应中有白色沉淀生成
7.小明想在鸡蛋壳(主要成分CaCO3)上腐蚀出一个“福”字(如图),送给奶奶作为生日礼物。下列溶液能帮他实现愿望的是( )
A.食盐水B.白酒C.蔗糖水D.白醋
8.中国古代文献记载了丰富的化学知识。
(1)《天工开物》中记载了金、铜、铁、锌等金属,这些金属中能与稀盐酸反应的有 (写化学式)。
(2)古典籍中有“银针验毒”的记载。请你对相关化学方程式配平:4Ag+2H2S+O2=2 +2H2O
(3)我国是最早应用湿法冶铜的国家:用铁与“胆水”(含CuSO4的溶液)反应获得铜,其原理为 (用化学方程式表示)。
9.学习了酸的化学性质后,小科同学以稀硫酸为主题,绘制了“多彩酸世界”思维导图。请据图回答:
(1)若用紫色石蕊试液实现①,会得到 色溶液。
(2)若要实现④,可选用 (填化学式)和稀硫酸反应。
10.某科学活动小组以“酸的化学性质”为主题进行探究性学习,请回答下列问题:
(1)实验中观察到产生气泡是试管 (选填“①”、“②”、“③”、“④”、“⑤”)。
(2)试管③中反应的化学方程式是 。
(3)完成对酸的性质探究,观察到试管⑤中溶液变蓝色物质,X可能是 。
11.科学课上同学们来到化学实验室进行实验,加强对酸的化学性质的整体认识。他们将适量的稀盐酸分别滴加到六支试管中进行实验(如图所示),请回答下列问题:
(1)上述六支试管中有气泡产生的是 (填序号)。
(2)能证明“C试管中发生了化学反应”的现象是 。
12.为验证“酸的化学通性”,某班同学在实验室进行如下实验。请分析并回答相关问题:
(1)写出能证明A中反应发生的现象 。
(2)写出上述实验中酸与金属氧化物反应的化学方程式 。
(3)要全面验证酸的化学通性,D试管中能与酸反应的固体单质是 (写一种即可)。
(4)实验完成后,将全部废液倒入废液缸内,测得pH=2,则废液中所含溶质最多有 种(溶质不计指示剂与气体)。
13.为验证稀硫酸的化学性质,小金做了如图实验:
(1)②号试管中出现的现象是 。
(2)能观察到冒气泡的试管有 号管(填试管序号);选择其中一个写出其反应的化学方程式 。
(3)将⑤中的试剂换成 可以得到同样的实验现象。
14.如图所示装置,小试管内盛有神秘物质,滴管内装有稀盐酸,U型管内盛有氢氧化钠溶液,反应前U形管两侧液面相平,把滴管内的盐酸滴入小试管里。若神秘物质是碳酸钙和金属锌,则U型管右端液面会先下降再回升。
(1)最终回升后的液面 左端液面(选填“高于”、“低于”或“平于”)。
(2)分析出现以上现象的原因。
15.学习科学的重要方法之一是对知识点的归纳和总结,在学习酸的性质后,如图是小敏同学总结的酸的化学性质,请你根据要求完成下列问题。
(1)酸溶液有相似化学性质的原因是溶液中都含有 (离子符号)。
(2)图中的X代表一类物质,则X为 (填物质类别)。
(3)性质③发生的反应的实质是 。
16.如图化学反应的溶液颜色变化体现了“魔法世界,魅力科学”。请回答:
(1)若X是稀盐酸,B是红色的氧化物,则B的化学式为 。
(2)若X是稀硫酸,C是单质,则C的名称为 ;X与C反应的化学方程式为 。
(3)若X是稀硫酸,D是碱,则X与D反应的化学方程式为 。
教学内容
酸与指示剂,金属氧化物,碱反应的掌握,酸的通性,个性掌握
教学目标
让学生熟练掌握上述教学内容
教学重点
酸的通性,个性掌握
教学难点
酸的个性掌握
课程难度
简单
次数
试剂
实验条件
实验现象
1
0.2克CuO粉末+6毫升pH=2的盐酸
常温
黑色粉末溶解,溶液呈蓝绿色
2
0.2克CuO粉末+6毫升pH=2的硫酸
常温
无明显现象
3
0.2克CuO粉末+6毫升pH=2的硫酸+0.35克NaCl
常温
黑色粉末溶解,溶液呈蓝绿色
4
0.2克CuO粉末+6毫升pH=2的硫酸+0.35克 。
常温
无明显现象
浙教版(2024)九年级上册第3节 能量转化的量度导学案及答案: 这是一份浙教版(2024)九年级上册<a href="/kx/tb_c98627_t4/?tag_id=42" target="_blank">第3节 能量转化的量度导学案及答案</a>,文件包含浙教版科学九上科学33能量转换的量度学案解析版doc、浙教版科学九上科学33能量转换的量度学案原卷版doc等2份学案配套教学资源,其中学案共26页, 欢迎下载使用。
浙教版(2024)第2节 金属的化学性质第一课时学案: 这是一份浙教版(2024)<a href="/kx/tb_c98619_t4/?tag_id=42" target="_blank">第2节 金属的化学性质第一课时学案</a>,文件包含浙教版科学九上科学22金属性质第一课时学案原卷版doc、浙教版科学九上科学22金属性质第一课时学案解析版doc等2份学案配套教学资源,其中学案共25页, 欢迎下载使用。
初中科学浙教版(2024)九年级上册第1节 金属材料学案: 这是一份初中科学浙教版(2024)九年级上册<a href="/kx/tb_c98618_t4/?tag_id=42" target="_blank">第1节 金属材料学案</a>,文件包含浙教版科学九上科学21金属材料学案解析版doc、浙教版科学九上科学21金属材料学案原卷版doc等2份学案配套教学资源,其中学案共19页, 欢迎下载使用。













