





鲁科版 (2019)选择性必修1第2节 化学反应的限度完美版课件ppt
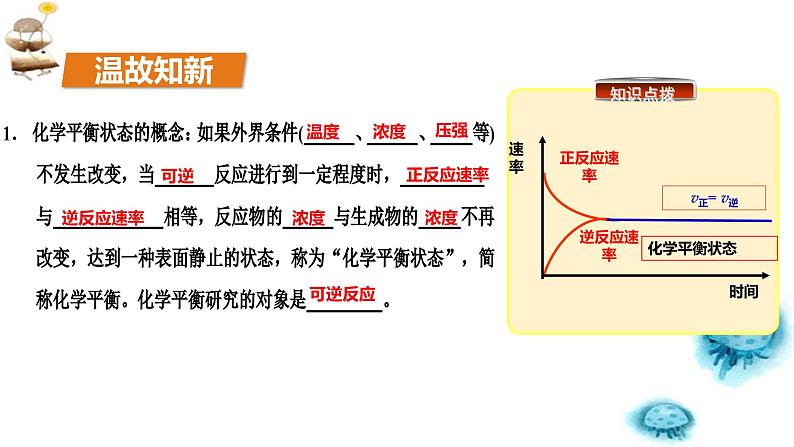
展开外界条件(温度、浓度、压强等)一旦改变,化学平衡状态就会被破坏,并在新的条件下建立新的化学平衡。
2. 化学平衡状态的特征:
化学平衡状态是一种动态平衡。达到平衡状态时,反应并没有停止,这时正反应和逆反应都依然在进行。
反应物的浓度和生成物的浓度不再改变。
在工业生产和实验室中,人们会遇到各种各样的可逆反应,如合成氨的反应:
该反应在一定条件下不可能进行完全,即存在一定的限度。反应限度对人类的生产活动和日常生活有着重要影响。因此,对化学反应来说,仅研究化学反应的方向是远远不够的,还需要关注化学反应的限度问题。那么,怎样才能定量地描述化学反应的限度呢?
研究表明,可逆反应在适当条件下进行一段时间后一定会达到化学平衡状态。此时,平衡混合物的组成不再随时间的延续而变化,反应达到一定的限度。在研究了大量实验的基础上,人们发现可以用化学平衡常数来定量描述化学反应的限度。
那么什么是化学平衡常数?该如何表示?如何计算?怎么用它来比较反应的限度大小呢?
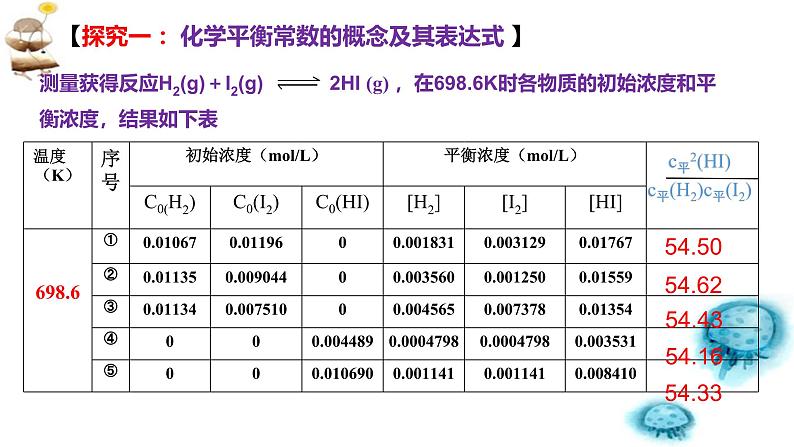
【探究一 :化学平衡常数的概念及其表达式 】
分析计算所得数据,寻找其中的规律。
(1)相同温度,达到化学平衡状态时 的数值相同吗?
(2)这个常数与反应的起始浓度大小有关吗?
(3)这个常数与正向建立还是逆向建立平衡有关系吗?
无关。即与平衡建立的过程无关。
对于一般的可逆反应,mA(g)+nB(g)pC(g)+qD(g),当在一定温度下达到平衡时,
一定温度下,当一个可逆反应达到平衡状态时,生成物浓度以化学计量数为指数的幂的乘积与反应物浓度以化学计量数为指数的幂的乘积的比值是一个常数。这个常数就是该反应的化学平衡常数(简称平衡常数,用K表示)。
写出下表中各反应的平衡常数表达式和单位。
【交流.研讨】写出下表中各反应的平衡常数表达式。并讨论下面的问题
问题1:对于一个反应,其平衡常数的表达式是唯一的吗?平衡常数的表达式与哪些因素有关?
不唯一。化学平衡常数的表达式取决于化学方程式的系数,对于确定反应还与温度有关。
问题2:对于一可逆反应,其正反应和逆反应的K有什么关系?
问题3:如果浓度的单位是ml•L-1,将浓度单位代入化学平衡常数表达式,可得到K的单位。由上述结果分析K的单位与反应的化学方程式存在什么关系?
K的单位与化学方程式的书写方式相对应。
c平(Ag+)c平(Cl-)
纯固体和液体浓度为1,不列入K 的表达式
探究二:化学平衡常数意义及应用
使用平衡常数应注意的问题:
(1)化学平衡常数只受温度影响,与反应物或生成物的浓度变化无关。
C(s)+H2O(g)CO(g)+H2(g)FeO(s)+CO(g)Fe(s)+CO2(g)
(2)在平衡常数表达式中,水(液态)的浓度、固体物质的浓度不写。
意义:反映了化学反应可能进行的程度,平衡常数的数值越大,说明反应进行得越完全。
K>105或106时 ,反应进行的较完全;
K<10-5或10-6时,反应很难正向进行。
思考:如何判断某温度下可逆反应是否达到平衡状态?
对于可逆反应aA(g)+bB(g) ⇌ cC(g)+dD(g)
达到平衡状态时, K=
在某温度下,用浓度商Q与K比较大小来判断是否达到平衡。
Q = K 反应状态 。 Q < K 反应状态 。 Q > K 反应状态 。
1.已知某化学反应的平衡常数表达式为 ,在不同的温度下该反应的平衡常数如表所示:
下列有关叙述不正确的是( )A.该反应的化学方程式是CO(g)+H2O(g)⇌CO2(g)+H2(g)B.上述反应的正反应是放热反应C.若在1 L的密闭容器中通入CO2和H2各1 ml,5 min后温度升高到830 ℃,此时测得CO为0.4 ml,则该反应达到平衡状态D.若平衡浓度符合下列关系式: ,则此时的温度为1 000 ℃
2.在密闭容器中充入4 ml X,在一定的温度下4X(g) 3Y (g) + Z (g),达到平衡时,有30%的发生分解,则平衡时混合气体总物质的量是( ) A. 3.4ml B. 4ml C. 2.8ml D. 1.2 ml
3.在一定条件下,密闭容器中可发生可逆反应:N2(g) + 3H2(g) ⇌ 2NH3(g),下列说法中,表明这一反应已经达到化学平衡状态的是( )A. N2、H2、NH3的浓度相等 B. N2、H2、NH3的浓度不再变化C. N2、H2、NH3在密闭容器中共存 D. 反应停止,正、逆反应速率都等于零
化学选择性必修1第2节 化学反应的限度完美版ppt课件: 这是一份化学选择性必修1<a href="/hx/tb_c4002581_t3/?tag_id=26" target="_blank">第2节 化学反应的限度完美版ppt课件</a>,文件包含22化学反应的限度第4课时压强对化学平衡的影响2019鲁科版选修1化学反应原理pptx、压强对化学平衡的影响mp4等2份课件配套教学资源,其中PPT共19页, 欢迎下载使用。
高中化学鲁科版 (2019)选择性必修1第2章 化学反应的方向、 限度与速率第2节 化学反应的限度评优课ppt课件: 这是一份高中化学鲁科版 (2019)选择性必修1<a href="/hx/tb_c4002581_t3/?tag_id=26" target="_blank">第2章 化学反应的方向、 限度与速率第2节 化学反应的限度评优课ppt课件</a>,文件包含22化学反应的限度第3课时浓度温度对化学平衡的影响2019鲁科版选修1化学反应原理pptx、浓度对化学平衡的影响mp4、温度对化学平衡的影响mp4等3份课件配套教学资源,其中PPT共18页, 欢迎下载使用。
高中鲁科版 (2019)第2节 化学反应的限度优秀ppt课件: 这是一份高中鲁科版 (2019)<a href="/hx/tb_c4002581_t3/?tag_id=26" target="_blank">第2节 化学反应的限度优秀ppt课件</a>,共16页。PPT课件主要包含了温故知新,方法导引,三段式法,归纳总结,课堂练习等内容,欢迎下载使用。













