




四川省成都市新津中学2022-2023学年高一下学期4月月考化学试题(Word版附解析)
展开考试时间:75分钟
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
原子量:Zn-65 Cu-64 H-1
第I卷(选择题)
一、单选题(每小题3分)
1. 《厉害了,我的国》“中国名片”中航天、军事、天文等领域的发展受到世界瞩目。它们与化学有着密切联系。下列说法正确的是
A. “中国天眼”的“眼眶”是钢铁结成的圈梁,属于新型无机非金属材料
B. “复兴号”车厢连接处关键部位使用的增强聚四氟乙烯板属于无机非金属材料
C. “神舟十一号”宇宙飞船返回舱外表面使用的高温结构陶瓷是新型无机非金属材料
D. “天宫二号”空间实验室的太阳能电池板的主要材料是二氧化硅
2. 硫黄在空气中燃烧生成气体甲,甲溶于水得乙溶液,向乙溶液中滴加双氧水,乙溶液变成丙溶液。向丙溶液里加入Na2S生成气体丁,把丁通入乙溶液中得到沉淀戊。甲、乙、丙、丁、戊均含有硫元素,则它们分别为
A. SO3、H2SO4、H2SO3、H2S、S
B. SO2、H2SO3、H2SO4、S、H2S
C. SO3、H2SO4、H2SO3、S、H2S
D. SO2、H2SO3、H2SO4、H2S、S
3. 某科学探究小组为探究电化学原理,设计了如图所示的装置进行探究实验。下列对实验中观察到的现象或相关结论的叙述不正确的是
A. a和b不连接时,铁片上有红色的铜析出
B. a和b用导线连接时,铜片为正极
C. 无论a和b是否连接,反应的本质相同,溶液中均有Fe2+生成
D. a和b用导线连接时,溶液中的Cu2+应向铁电极移动且能更快地析出铜
4. 实验室制取、收集NH3,并组装NH3的喷泉实验装置。下列图示装置和原理能达到实验目的的是
A. 制NH3B. 干燥NH3
C. 收集NH3D. 喷泉实验装置
5. 下列说法正确的是( )
A. 凡经加热而发生的化学反应都是吸热反应
B. C(石墨,s) == C(金刚石,s),反应中既没有电子的得失也没有能量的变化
C. 干冰升华时,二氧化碳分子中的共价键不发生断裂
D. 伴有能量变化的物质变化,都是化学变化
6. 为除去粗盐中的Ca2+、Mg2+、以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下:
下列说法正确的是:
A. 上述实验过程中共有两处用到玻璃棒
B. ②③④的顺序可以任意调换
C. ⑤可以在⑥之后进行
D. 检验是否除完的方法是:取②之后的溶液于试管中,加入BaCl2溶液,观察是否有沉淀生成
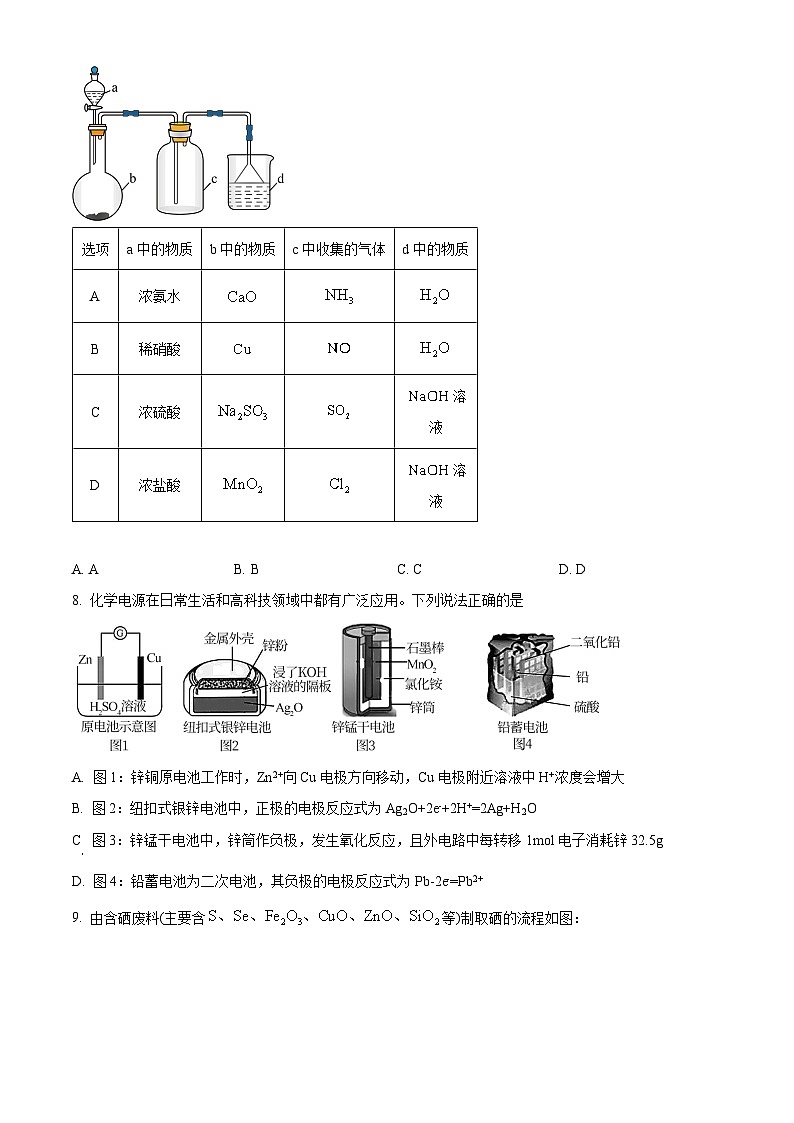
7. 实验室某些气体的制取、收集及尾气处理装置如图所示(省略夹持装置)。仅用如图装置和表中提供的物质完成相关实验,最合理的选项是
A. AB. BC. CD. D
8. 化学电源在日常生活和高科技领域中都有广泛应用。下列说法正确的是
A. 图1:锌铜原电池工作时,Zn2+向Cu电极方向移动,Cu电极附近溶液中H+浓度会增大
B. 图2:纽扣式银锌电池中,正极的电极反应式为Ag2O+2e-+2H+=2Ag+H2O
C 图3:锌锰干电池中,锌筒作负极,发生氧化反应,且外电路中每转移1ml电子消耗锌32.5g
D. 图4:铅蓄电池为二次电池,其负极的电极反应式为Pb-2e-=Pb2+
9. 由含硒废料(主要含等)制取硒的流程如图:
下列有关说法不正确的是
A. “分离”时得到含硫煤油的方法是过滤
B. “酸溶”时能除去废料中的全部氧化物杂质
C. “浸取”发生反应的化学方程式为:
D. “酸化”的离子反应为:
10. 将32gCu投入到80mL5ml/L的HNO3溶液中,充分反应后,向溶液中再加入200mL2ml/LH2SO4溶液,使之充分反应,两步反应共生成NO在标况下的体积
A 2.24LB. 6.72LC. 8.96LD. 11.2L
二、多选题(每个小题有两个或两个以上的答案,每小题3分,多选或错选不给分,漏选给1分)
11. 下列有关硫酸的化学事实与硫酸表现出的性质(括号中)的描述中,正确的是
A. 久置在敞口容器中的浓硫酸,溶液质量增大(脱水性)
B. 在加热条件下铁与浓硫酸反应(氧化性、酸性)
C. 蔗糖与浓硫酸反应的“黑面包”实验(吸水性)
D. 浓硫酸与氯化钠固体反应制HCl(难挥发性)
12. 镁燃料电池以镁合金作为电池的一极,另一极充入过氧化氢,电解质溶液是酸化的氯化钠溶液,放电时总反应为Mg+2H++H2O2=Mg2++2H2O。关于该电池说法正确的是
A. 镁合金作为电池的负极,发生还原反应
B. 放电时H2O2在正极得电子,被还原
C. 负极反应式:Mg-2e-=Mg2+
D 放电时正极附近溶液酸性增强
13. 为了证明NH4Fe(SO4)2·12H2O(硫酸铁铵晶体)的成分中含有NH、Fe3+、SO和H2O,下列实验叙述中不正确的是
A. 取少量密封保存的硫酸铁铵晶体放入试管,加热,试管口有液体生成,则可证明晶体的成分中含有结晶水
B. 硫酸铁铵晶体溶于水,得黄色溶液,滴入2滴KSCN溶液,溶液变为血红色,则可证明晶体的成分中含有Fe3+
C. 硫酸铁铵晶体溶于水,加少量稀硝酸,无现象;再滴入几滴BaCl2溶液,有白色沉淀生成,则可证明晶体的成分中含有SO
D. 取少量硫酸铁铵晶体放入试管,加浓NaOH溶液并加热,试管口湿润的蓝色石蕊试纸变红,则可证明晶体的成分中含有NH
14. 如图装置,将溶液A逐滴加入固体B中,下列叙述正确的是
A. 若A为浓硫酸,B为Na2SO3固体,C中盛石蕊溶液,则C中溶液先变红后褪色
B. 若A为醋酸,B为贝壳,C中盛过量澄清石灰水,则C中溶液变浑浊
C. 若A为浓盐酸,B为MnO2,C中盛品红溶液,则C中溶液褪色
D. 若A为浓氨水,B为生石灰,C中盛AlCl3溶液,则C中产生白色沉淀,白色沉淀不溶解
第I1卷(非选择题)
15. 已知H2(g)+O2(g)=H2O(g),如图是1mlH2燃烧过程中的能量变化示意图。
请回答下列问题:
(1)下列说法正确的是_____。
A. a为反应物的总能量
B. b为断裂反应物化学键的需要的能量
C. 反应物的总能量高于生成物总能量
D. c表示反应吸收的热量
(2)该反应是_____(填“吸热”或“放热”)反应。
(3)氢气在氧气中燃烧,破坏1mlH—H吸收Q1kJ的能量,破坏1mlO=O吸收Q2kJ的能量,形成1mlH—O释放Q3kJ的能量,则下列关系式正确的是_____。
A. 2Q1+Q2>4Q3B. 2Q1+Q2<4Q3
C. Q1+Q2
(5)燃料电池是一种高效、环境友好的发电装置。氢氧燃料电池已用于航天飞机。以氢氧化钾溶液为电解质溶液的这种电池的负极反应式为_____,这种电池在放电使用一段时间后,电解质溶液中的c(OH-)将_____(填“增大”“减小”或“不变”)。
(6)如图是银锌原电池装置的示意图,以硫酸铜为电解质溶液。回答下列问题:
锌为_____极,电极反应式为_____,若反应前两电极质量相等,工作一段时间后两电极质量相差12.9g,则外电路通过的电子数为_____。
16. 某化学兴趣小组利用如图所示的装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的制备装置,C为纯净干燥的氯气与氨气发生反应的装置(加热及夹持装置已略去)。
回答下列问题:
(1)仪器a的名称为_______。
(2)需要加热的装置为_______(填“A”或“F”),该装置中发生反应的离子方程式为_______。
(3)装置D中所盛装的试剂为_______,装置E中饱和氯化钠溶液的作用为_______。
(4)装置F中发生反应的化学方程式为_______。
(5)反应过程中,装置C的集气瓶中有大量白烟产生,且另一种产物为空气的主要成分之一。
①该反应中氧化剂与还原剂的物质的量之比为_______。
②每转移0.3ml电子,同时消耗_______L(标准状况下)。
17. 二氧化硫为无色气体,有强烈刺激性气味,是大气主要污染物之一。某化学兴趣小组欲制备并探究某些性质。
【的制备】用亚硫酸钠与较浓的硫酸反应制备的装置如图所示(夹持仪器省略):
(1)图中的装置错误的是_____;B中发生反应的化学方程式为_____;D的作用是_____。
【的性质】探究气体性质的装置如图所示:
(2)装置Ⅰ中的现象是_____,说明具有_____(选填“氧化”或“还原”)性。写出装置Ⅰ中通入少量的离子方程式:_____。
(3)在上述装置中通入过量的,为了验证Ⅱ中发生了氧化还原反应,取Ⅱ中溶液分成两份,并设计了如下实验:
方案一:向第一份溶液中加入少量酸性溶液,紫红色褪去;
方案二:向第二份溶液中加入KSCN溶液,不变红,再加入新制的氯水,溶液变红。
上述方案不合理的是_____(选填“一”或“二”),原因是_____,写出解释该原因的离子方程式:_____。
(4)可以用来制备硫代硫酸钠,硫代硫酸钠可用于照相业作定影剂,也可用于纸浆漂白作脱氯剂等。实验室可通过和共同反应来制取。写出如图所示装置三颈瓶中制取的化学方程式:_____。
18. 填空
(1)硒是动物和人体所必需的微量元素之一,也是一种重要的工业原料。硒在自然界中稀少而分散,常从精炼铜的阳极泥中提取硒。阳极泥中的硒主要以Se和CuSe的形式存在,工业上常用硫酸化焙烧法提取硒,主要步骤如下:(已知S、Se、Te为同一主族元素)
i.将含硒阳极泥与浓硫酸混合焙烧,产生SO2、SeO2的混合气体
ii.用水吸收i中混合气体,可得Se固体
①写出步骤ii中的化学方程式:_____。
②下列说法合理的是_____(填字母)。
a.SeO2既有氧化性又有还原性,其还原性比SO2强
b.浓硒酸可能具有强氧化性、脱水性
c.热稳定性:H2Se
已知TeO2微溶于水,易溶于较浓的强酸和强碱溶液。
①“碱浸”时发生反应的离子方程式为_____
②碱浸后的“滤渣”可以部分溶于稀硝酸,发生反应的化学方程式是_____。
③“酸溶”过程中发生的化学方程式为:_____。选项
a中的物质
b中的物质
c中收集的气体
d中的物质
A
浓氨水
B
稀硝酸
C
浓硫酸
溶液
D
浓盐酸
溶液
四川省成都市新津中学2021-2022学年高一下学期期末考试化学试题(Word版附解析): 这是一份四川省成都市新津中学2021-2022学年高一下学期期末考试化学试题(Word版附解析),文件包含四川省成都市新津中学2021-2022学年高一下学期期末考试化学试题Word版含解析docx、四川省成都市新津中学2021-2022学年高一下学期期末考试化学试题Word版无答案docx等2份试卷配套教学资源,其中试卷共27页, 欢迎下载使用。
四川省成都市石室中学2022-2023学年高一上学期期中考试化学试题(Word版附解析): 这是一份四川省成都市石室中学2022-2023学年高一上学期期中考试化学试题(Word版附解析),共15页。试卷主要包含了本试卷包括选择题和非选择两部分,满分100分,考试时间75分钟,5 K, 设为阿伏加德罗常数的值,2,B错误;, “东风夜放花千树等内容,欢迎下载使用。
四川省成都市石室中学2023-2024学年高一上学期期中化学试题(Word版附解析): 这是一份四川省成都市石室中学2023-2024学年高一上学期期中化学试题(Word版附解析),共24页。试卷主要包含了可能用到的相对原子质量, 下列说法正确的是,05L×1ml/L×2=0等内容,欢迎下载使用。












