

广东省揭阳市两校2024-2025学年高三上学期8月月考化学试题(原卷版)
展开(满分100分考试时间75分钟)
可能用到的相对原子质量:H1 C12 N14 O16 S32 Fe56
一、选择题:本题共16小题,共44分。第1-10小题,每小题2分;第11-16小题,每小题4分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 南粤大地,岭南风情。下列广东工艺品主要由有机高分子材料制成的是
A. AB. BC. CD. D
2. 科教兴国,我国科技发展在多个领域获得突破。下列说法不正确的是
A. 新能源甲醇燃料电池汽车在行驶时将电能转化化学能
B. 深中通道海底沉管混凝土中的Si元素位于元素周期表的p区
C. 空间站存储器所用的材料石墨烯与金刚石互为同素异形体
D. 核电站核能发电时发生核裂变产生的放射性核素与互为同位素
3. 雪龙二号是我国自主建造的全球第一艘采用艏艉双向破冰技术的极地科考破冰船,展现了我国科技发展的巨大成就。下列说法不正确的是
A. 螺旋桨采用镍铝青铜合金有强度大、不易锈蚀的特点
B. 船载雷达系统所用半导体材料碳化硅属于共价晶体
C. 具有良好电绝缘性和耐热性的酚醛树酯可以通过加聚反应制得
D. 船用发动机使用的燃料是柴油,柴油是石油分馏产品,分馏属于物理变化
4. 广东美食享誉全国。下列说法不正确的是
A. 客家酿豆腐鲜香滑嫩,烹饪豆腐所用的花生油主要成分为高级脂肪酸
B. 广州包点松软可口,制作包点所用面粉的主要成分为淀粉
C. 潮汕牛肉丸肉质饱满,蒸煮牛肉丸时蛋白质发生变性
D. 东莞烧鹅肥而不腻,涂在烧鹅表皮上的麦芽糖能水解
5. 测定浓硫酸试剂中含量主要操作包括:
①量取一定量的浓硫酸,稀释;
②转移定容得待测液;
③移取待测液,用的溶液滴定。
上述操作中,不需要用到的仪器为
A. B. C. D.
6. 全世界每年因钢铁锈蚀会造成巨大的损失,为了保护地下的钢铁输水管所采取的措施如图所示。下列说法不正确的是
A. 钢铁发生吸氧腐蚀正极反应为O2+2H2O+4e-=4OH-
B. 导线与Zn块连接为牺牲阳极法
C. 导线应连接外接电源的负极
D. 导线与Cu块连接也可保护钢铁输水管
7. “幸福不会从天降,美好生活靠劳动创造。”下列劳动项目与所述的化学知识没有关联的是
A. AB. BC. CD. D
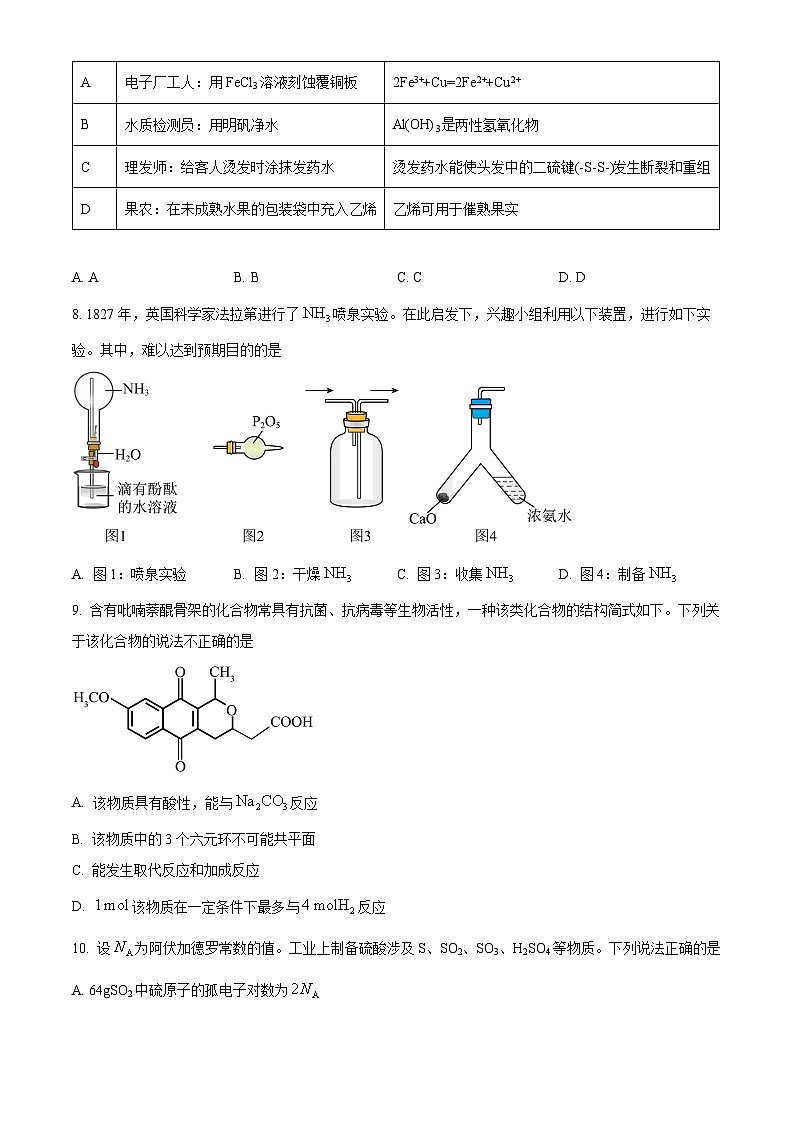
8. 1827年,英国科学家法拉第进行了喷泉实验。在此启发下,兴趣小组利用以下装置,进行如下实验。其中,难以达到预期目的的是
A. 图1:喷泉实验B. 图2:干燥C. 图3:收集D. 图4:制备
9. 含有吡喃萘醌骨架的化合物常具有抗菌、抗病毒等生物活性,一种该类化合物的结构简式如下。下列关于该化合物的说法不正确的是
A. 该物质具有酸性,能与反应
B. 该物质中的3个六元环不可能共平面
C. 能发生取代反应和加成反应
D. 该物质在一定条件下最多与反应
10. 设为阿伏加德罗常数的值。工业上制备硫酸涉及S、SO2、SO3、H2SO4等物质。下列说法正确的是
A. 64gSO2中硫原子的孤电子对数为
B. 2mlSO2和1mlO2在密闭容器中充分反应后的分子数目为
C. 标准状况下,2.24LSO3中分子的数目为
D. 常温下1.0LpH=2的H2SO4溶液中H+数目为
11. 利用下图所示装置进行实验,先向W形管中通入,一段时间后,再用注射器向其中加入浓盐酸,当充满整个W形管后点燃酒精灯,下列说法正确的是
A. ①处固体为
B. ②处试纸变蓝,说明具有氧化性
C. ③处可观察到钠块剧烈燃烧,且产生大量白雾
D. ④处碱石灰的主要作用是防止空气中的、水蒸气与钠反应
12. 一种可用于头孢菌素改性剂的结构如下图所示,其中X、Y、Z、W是原子序数递增的短周期主族元素,下列说法正确的是
A. 第一电离能:Z
C. 沸点:X2Z>X2W
D. YW2为极性分子
13. 下列实验操作能达到实验目的的是
A. AB. BC. CD. D
14. 部分含铜物质的分类与相应化合价关系如图所示,其中e为氯化物。下列推断不合理的是
A. 转化a→c→d在给定条件下均可一步反应实现
B. b可与盐酸反应生成e和a,b既有氧化性又有还原性
C. 新制的d可用于检验葡萄糖中的醛基
D. 电解e溶液可得到金属铜和氯气
15. 在一定温度下,以为催化剂,氯苯和在中发生平行反应,分别生成邻二氯苯和对二氯苯
已知:
①两产物浓度之比与反应时间无关。
②反应物起始浓度均为,反应30min测得氯苯15%转化为邻二氯苯,25%转化为对二氯苯。下列说法不正确的是
A. 反应Ⅰ的活化能大于反应Ⅱ
B. 保持其他条件不变,改变反应物浓度可以提高产物中邻二氯苯的比例
C. 保持其他条件不变,改变催化剂可以提高产物中邻二氯苯的比例
D. 保持其他条件不变,适当提高反应温度可以提高产物中邻二氯苯的比例
16. 一种锌钒电池的工作原理如图所示,电解质为ZnSO4溶液,电池反应式为:Zn+ V2O5ZnV2O5。下列说法错误的是
A. 放电时,b电极的反应式:Zn2++V2O5 + 2e-=ZnV2O5
B. 放电时,Zn2+从a电极区向b电极区迁移
C 充电时,b电极与电源负极相连
D. 充电时,若转移0.4 ml 电子,理论上a电极增重13 g
二、非选择题:本题共4小题,共56分。
17. 某学习小组欲探究苯酚的化学性质。
回答下列问题:
Ⅰ.探究苯酚的酸性。
小组分别进行了下列实验:
(1)实验______(填编号)的对比现象能说明苯酚的酸性较弱。
(2)为进一步探究苯酚的酸性,学习小组采用电位滴定法进行测定。分别取20mL浓度均为的盐酸、醋酸溶液、苯酚溶液、乙醇溶液于四个50mL的烧杯中,用电导率传感器测定其电导率,用数据采集器和计算机进行分析,数据结果如图所示:
①苯酚溶液的电导率曲线为______(填图中字母)。
②推测、、的酸性强弱:______(用结构简式表示)。
Ⅱ.探究苯酚与溴水的反应。
设计实验相关量如表所示,分别向蒸馏水和苯酚溶液中逐滴滴入浓溴水,同时进行磁力搅拌,观察并记录电导率的变化,电导率随时间的变化曲线如图所示:
(3)根据实验信息推测,______,______。
(4)苯酚溶液与浓溴水反应的电导率曲线为______(填图中字母);根据曲线信息推断该反应为______(填“取代”或“加成”)反应;结合化学反应方程式和必要的文字说明推断理由:____________。
(5)实验采用的苯酚溶液为稀溶液,溴水为浓溶液,若两者的浓度关系相反,则产生的后果是____________。
(6)写出苯酚在生产生活中的一种用途:____________。
18. 赤泥是氧化铝生产排放的固体废弃物。由赤泥(主要成分为Al2O3、SiO2、Fe2O3、FeO、CaO、Na2O等)制备一种高效净水剂聚合硫酸铝铁(PAFS)的工艺流程如下:
(1)基态铝原子价层电子轨道表示式为_______,SO的空间构型是_______。
(2)加快“浸取”速率可采取的措施为_______(答出一种方法即可),酸浸渣的主要成分是_______(填化学式)。
(3)“氧化”时发生反应的离子方程式为_______;室温下,向氧化后的溶液中滴加NaOH溶液至pH=4时,溶液中的c(Fe3+)=_______ml/L(已知常温下,Fe(OH)3的Ksp=4.0×10-38)。
(4)为了测试所制得的聚合硫酸铝铁的性能,取某水样在不同pH条件下加入PAFS并测定其去浊率,结果如图所示,(已知去浊率越高,净水效果越好)由图可知在设定的偏酸性和偏碱性条件下,水样的去浊率均不高,试分析pH<7时,去浊率较低的可能原因为_______。
(5)一种碳溶解在铁单质中形成合金的晶胞如下图所示,则该物质的化学式为_______,晶胞中与铁原子距离最近且相等的铁原子共有_______个;若晶胞中最近的铁原子与碳原子的距离为apm,则该晶体的密度为ρ=_______g·cm-3(阿伏加德罗常数的值用表示,写出计算式即可)。
19. 随着我国碳达峰、碳中和目标的确定,二氧化碳资源化利用倍受关注。CO2经催化加氢可以生成低碳有机物,主要有以下反应:
反应I:
反应Ⅱ:
反应Ⅲ:
(1)_______
(2)一定温度下,将1mlCO2和3mlH2加入密闭容器中发生反应I。
①下列情况能够说明该反应达到化学平衡状态的是_______(填标号)。
A.v(CO2):v(H2)=1:3
B.恒容条件下,容器内混合气体的密度保持不变
C.H2(g)有1.5mlH-H键断裂,同时H2O(g)有1mlH-O键断裂
D.恒容条件下,容器内的总压强不再改变
②该反应达到平衡后,保持温度不变,能提高CO2的平衡转化率的措施有_______(任写一种)。
(3)在某温度下,反应Ⅱ的平衡常数为0.25,此温度下,在密闭容器中加入一定量的CH3OCH3(g)和H2O(g)发生反应Ⅱ,某时刻时,测得各组分浓度如下:
此时v正_______v逆(填“>”、“<”或“=”),当反应达到平衡状态时,混合气体中CH3OH的体积分数=_______%。
(4)某压强下,在不同温度、不同投料比条件下发生反应Ⅲ,CO2的平衡转化率如下图所示,T1温度下,将12mlH2和6mlCO2充入2L的密闭容器中,5min后反应达到平衡状态,则0-5min内的平均反应速率v(CH3OCH3)=_______;KA、KB、KC三者之间的大小关系为_______。
(5)电化学法还原二氧化碳制取乙烯:在强酸性溶液中通入CO2气体,用惰性电极进行电解可制得乙烯,其原理如图所示:
上述装置中,阴极的电极反应式为_______。
20. 有机物Ⅰ结构对称,是一种优良的抗菌药成分,其合成路线如下。
已知:
①
②
回答下列问题:
(1)化合物A的分子式为________。
(2)反应①中,化合物A与气体x反应,生成化合物B,原子利用率100%。x为________。
(3)芳香族化合物M为B的同分异构体,其能够发生银镜反应、水解反应,且在核磁共振氢谱上只有4组峰,则M的结构简式为________,其含有的官能团名称为________。
(4)关于由D→E的说法中,不正确的是________。
A. 反应过程中,有C-O单键的断裂和C=C双键的形成
B. HCHO为平面结构,分子中存在由p轨道“头碰头”形成的π键
C. 化合物D中含有氧原子,能与水形成氢键,因此其易溶于水
D. 化合物E中,碳原子采取、杂化,但不存在顺反异构
(5)根据化合物E的结构特征,分析预测其可能的化学性质,完成下表。
(6)以甲苯、乙醛为含碳原料,利用反应③和④的原理,合成化合物W()。基于自己设计的合成路线,回答下列问题:
(a)最后一步反应中,有机反应物为________(写结构简式)。
(b)相关步骤涉及到芳香烃制卤代烃,其化学方程式为________(注明反应条件)。A.光彩烧瓷
B.广州玉雕
C.佛山丝绸“香云纱”
D.青铜器
选项
劳动项目
化学知识
A
电子厂工人:用FeCl3溶液刻蚀覆铜板
2Fe3++Cu=2Fe2++Cu2+
B
水质检测员:用明矾净水
Al(OH)3两性氢氧化物
C
理发师:给客人烫发时涂抹发药水
烫发药水能使头发中的二硫键(-S-S-)发生断裂和重组
D
果农:在未成熟水果的包装袋中充入乙烯
乙烯可用于催熟果实
选项
实验目的
实验操作
A
除去苯中含有的少量苯酚
加入足量的溴水,过滤
B
比较水和乙醇中羟基氢活泼性
向乙醇和水中分别加入少量Na
C
检验溴乙烷中的溴原子
先加入适量NaOH溶液,振荡,加热,再滴加少量AgNO3溶液
D
验证淀粉能发生水解反应
将淀粉和稀硫酸混合后,水浴加热,冷却后加入新制Cu(OH)2悬浊液,加加热
实验编号
实验内容
实验现象
实验1
向盛有苯酚溶液的试管中逐滴加入5%NaOH溶液并振荡
无明显现象
实验2
向盛有苯酚浊液的试管中逐滴加入5%NaOH溶液并振荡
溶液变澄清
实验3
向盛有苯酚溶液的试管中加入几滴紫色石蕊溶液
无明显现象
物质
溶液浓度
溶液体积
加入浓溴水滴数
蒸馏水
0
30
10
苯酚溶液
0.1
物质
CH3OCH3(g)
H2O(g)
CH3OH(g)
浓度/(ml·L-1)
1.8
1.8
0.4
序号
反应试剂、条件
反应形成的新结构
反应类型
a
的溶液
_______
_______
b
_______
_______
水解反应
广东省部分学校2024-2025年高三上学期开学考试化学试题(原卷版): 这是一份广东省部分学校2024-2025年高三上学期开学考试化学试题(原卷版),共11页。试卷主要包含了可能用到的相对原子质量, 下列化学用语表示正确的是, 设为阿伏加德罗常数的值等内容,欢迎下载使用。
广东省佛山市南海区2024-2025学年高三上学期开学摸底测试化学试题(原卷版): 这是一份广东省佛山市南海区2024-2025学年高三上学期开学摸底测试化学试题(原卷版),共11页。试卷主要包含了 劳动成就梦想,技能点亮人生, 设为阿伏加德罗常数的值等内容,欢迎下载使用。
广东省揭阳市两校2024-2025学年高三上学期8月月考化学试题: 这是一份广东省揭阳市两校2024-2025学年高三上学期8月月考化学试题,共8页。












