




所属成套资源:高中化学人教版(2019)选择性必修1化学反应原理
化学选择性必修1第四节 化学反应的调控评优课教学课件ppt
展开
这是一份化学选择性必修1第四节 化学反应的调控评优课教学课件ppt,共13页。PPT课件主要包含了合成氨反应的特点,想一想,从化学平衡分析,从化学反应速率分析,综合分析,课堂小结等内容,欢迎下载使用。
01 能运用浓度、压强、温度和催化剂对化学反应速率、化学平衡的影响规律,能讨论化学反应条件的选择和优化。
02 初步掌握应用化学原理选择化工生产条件的思想和方法,培养科学态度与社会责任等方面的学科核心素养。
18世纪末,英国化学家克鲁克斯“先天下之忧而忧”,率先发出为了使子孙后代免于饥饿“向空气要氮肥”的号召。我国合成氨工业的发展是在20世纪30年代开始的,经过几十年的不懈奋斗和发展,我国已经拥有了许多不同流程、不同规模的合成氨工厂。我国目前拥有了一支能够进行合成氨生产的科研等方面的研究技术团队,让我国已成为世界上最大的合成氨生产国,产量约占世界总产量的1/3。合成氨工业是关系我国国民经济的重要行业,是我国化肥工业的基础,也是传统煤化工的重要组成部分。氨是重要的化工原料,主要用于制造氮肥、硝酸、丁腈橡胶等;氨在冶金、机械加工、电子、造纸等行业用途广泛。
合成氨的热化学方程式为N2(g)+3H2(g) 2NH3(g) ΔH= -92.4 kJ·ml-1
反应为 反应。
正反应是气体体积 的反应。
∆H 0,熵变:∆S 0
常温(298K)下,∆H-T∆S 0,能自发进行。
根据合成氨反应的特点,应如何选择反应条件,以增大合成氨的反应速率、提高平衡混合物中氨的含量?
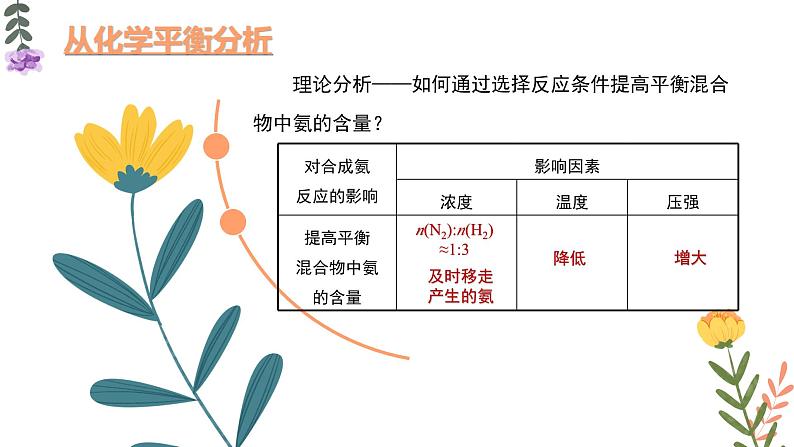
理论分析——如何通过选择反应条件提高平衡混合物中氨的含量?
n(N2):n(H2)≈1:3
实验验证理论
①温度理论分析:低温可以提高平衡混合物中氨的含量。实验结果:与理论预期一致
n(N2):n(H2) ≈ 1:3 10 MPa
②压强理论分析:压强越大越有利于提高平衡混合 物中氨的含量。实验结果:与理论预期一致
n(N2):n(H2) ≈ 1:3 400 ℃
合成氨反应为什么慢?
怎样降低反应的活化能?
如何增大合成氨的化学反应速率?
从化学反应速率与化学平衡考虑,都是压强越大越好。综合成本与设备耐压:10 MPa~30 MPa
②催化剂增大化学反应速率,不改变平衡混合物的组成。现在常用铁为主体的多成分催化剂,又称铁触媒,其活性最好的温度为500 ℃左右。
③温度低温可以提高平衡混合物中氨的含量,但低温会减小化学反应速率。综合考虑,特别是考虑催化剂的活性: 一般400~500 ℃
工业生产中选择适宜生产条件的原则
相关课件
这是一份化学第四节 化学反应的调控获奖ppt课件,共25页。PPT课件主要包含了学习目标,生活中化学反应的调控,延长食物储存时间,新课导入,新课讲解,增大反应物浓度,升高温度,降低温度,增大压强,使用催化剂等内容,欢迎下载使用。
这是一份高中化学人教版 (2019)选择性必修1第四节 化学反应的调控完美版ppt课件,共3页。
这是一份人教版 (2019)选择性必修1第四节 化学反应的调控评课课件ppt,共29页。PPT课件主要包含了空气变面包的反应,化学反应的调控等内容,欢迎下载使用。










