



高中人教版 (2019)第二节 电解池获奖教学课件ppt
展开从铜矿石到景泰蓝工艺品
掐丝、点蓝、烧蓝、磨光
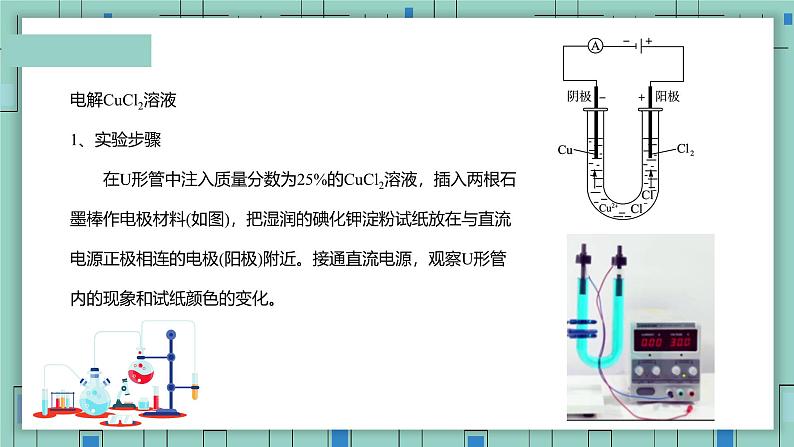
电解CuCl2溶液1、实验步骤 在U形管中注入质量分数为25%的CuCl2溶液,插入两根石墨棒作电极材料(如图),把湿润的碘化钾淀粉试纸放在与直流电源正极相连的电极(阳极)附近。接通直流电源,观察U形管内的现象和试纸颜色的变化。
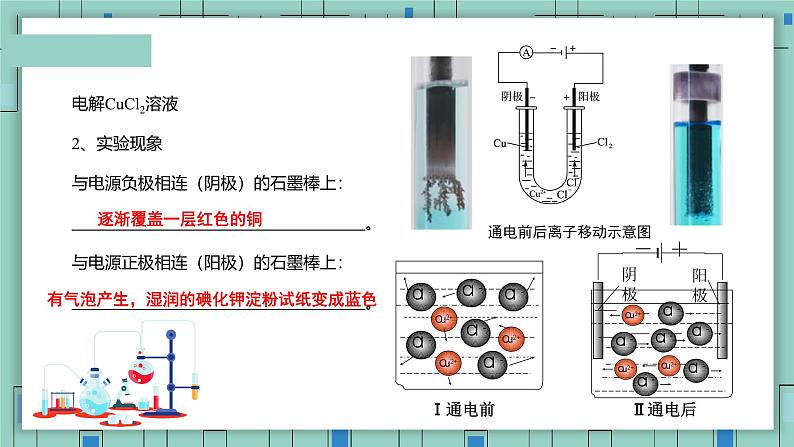
电解CuCl2溶液2、实验现象与电源负极相连(阴极)的石墨棒上: 。与电源正极相连(阳极)的石墨棒上: 。
通电前后离子移动示意图
有气泡产生,湿润的碘化钾淀粉试纸变成蓝色
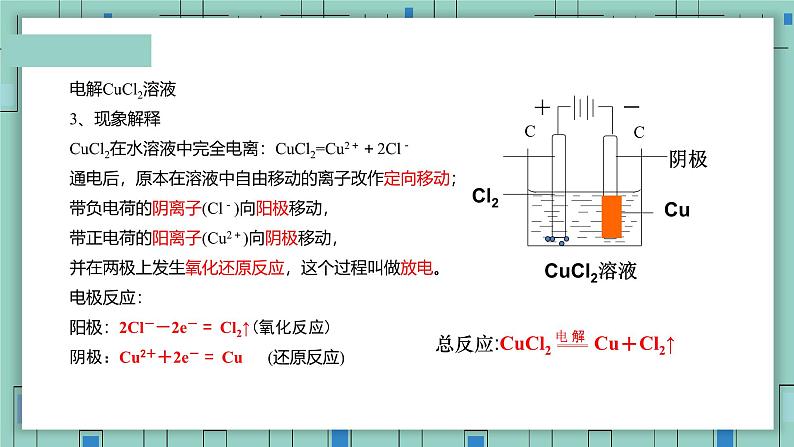
电解CuCl2溶液3、现象解释CuCl2在水溶液中完全电离:CuCl2=Cu2++2Cl-通电后,原本在溶液中自由移动的离子改作定向移动;带负电荷的阴离子(Cl-)向阳极移动,带正电荷的阳离子(Cu2+)向阴极移动,并在两极上发生氧化还原反应,这个过程叫做放电。电极反应:阳极:2Cl--2e- = Cl2↑(氧化反应)阴极:Cu2++2e- = Cu (还原反应)
电解1、定义:使电流通过电解质溶液而在阴、阳两极引起氧化还原反应的过程叫做电解。2、电离与电解的比较
1、定义:把电能转变为化学能的装置叫做电解池或电解槽。
2、电解池的两极 阳极——与电源正极相连,发生氧化反应。 阴极——与电源负极相连,发生还原反应。
3、电解池的构成条件(1)外接直流电源; (2)两个电极;(3)电解质溶液或熔融的电解质; (4)形成闭合回路。
4、电解池中电流、电子、离子的移动方向 电流方向:电源正极→阳极,阴极→电源负极。 电子流向:阳极→电源正极,电源负极→阴极。 离子流向:阳离子→阴极,阴离子→阳极。
5、电解池工作原理通电时,电子从电源的负极沿着导线流入电解池的阴极,经过阴、阳离子定向运动形成内电路,阳离子在阴极得到电子,发生还原反应,阴离子在阳极失去电子,发生氧化反应,电子沿导线流入直流电源的正极。电解的本质:电解质溶液的导电过程就是电解质溶液的电解过程。
惰性电极电解电解质溶液的规律
氯碱工业:电解饱和食盐水,制取烧碱、 氯气和氢气。 (1)电极反应式(并注明反应类型) 阳极:_______________(氧化反应) 阴极:______________ (还原反应)其中阴极反应中的H+是由水电离产生的。 (2)总反应式: _______________________________。
2Cl--2e-=Cl2↑
2H++2e-=H2↑
利用电解熔融盐或氧化物的方法来冶炼活泼金属Na、Ca、Mg、Al等。
高中化学人教版 (2019)选择性必修1第一节 原电池评优课教学课件ppt: 这是一份高中化学人教版 (2019)选择性必修1<a href="/hx/tb_c4002434_t3/?tag_id=26" target="_blank">第一节 原电池评优课教学课件ppt</a>,共18页。PPT课件主要包含了水果可以发电吗,化学能,2构成条件,电解质,自发的氧化还原,氧化反应,还原反应,思考讨论,原电池的设计,闭合回路等内容,欢迎下载使用。
高中化学人教版 (2019)选择性必修1第三节 盐类的水解优秀教学ppt课件: 这是一份高中化学人教版 (2019)选择性必修1<a href="/hx/tb_c4002428_t3/?tag_id=26" target="_blank">第三节 盐类的水解优秀教学ppt课件</a>,共25页。PPT课件主要包含了盐类的水解,盐类水解的应用等内容,欢迎下载使用。
高中人教版 (2019)第一节 电离平衡优秀教学课件ppt: 这是一份高中人教版 (2019)<a href="/hx/tb_c4002426_t3/?tag_id=26" target="_blank">第一节 电离平衡优秀教学课件ppt</a>,共18页。PPT课件主要包含了强电解质和弱电解质,实验3-1,醋酸的对比,弱电解质的电离平衡,影响电离平衡的条件,弱电解质的电离方程式,电离平衡常数等内容,欢迎下载使用。













