




所属成套资源:新高考化学三轮复习考前冲刺练习易错专题(2份打包,原卷版+解析版)
新高考化学三轮复习考前冲刺练习易错专题14 水溶液中离子平衡图像(2份打包,原卷版+解析版)
展开
这是一份新高考化学三轮复习考前冲刺练习易错专题14 水溶液中离子平衡图像(2份打包,原卷版+解析版),文件包含新高考化学三轮复习考前冲刺练习易错专题14水溶液中离子平衡图像原卷版docx、新高考化学三轮复习考前冲刺练习易错专题14水溶液中离子平衡图像解析版docx等2份试卷配套教学资源,其中试卷共65页, 欢迎下载使用。
►易错点二 滴定曲线
►易错点三 KW、Ksp的图像
►易错点四 分布系数图像
典例精讲
易错点一 稀释图像
【易错典例】
例1(2023·浙江温州·三模)在一定温度下,冰醋酸稀释过程中溶液的导电能力与pH的变化如图。下列有关说法中正确的是
A.a点溶液未达到电离平衡状态
B.离子总浓度越大,溶液导电能力越强
C.向a、b两点溶液中分别滴入同一NaOH溶液至中性,溶液中的相同
D.b点后,溶液中加水稀释,所有离子浓度均减小
【解题必备】稀释图像(pH与稀释倍数的线性关系)
【变式突破】
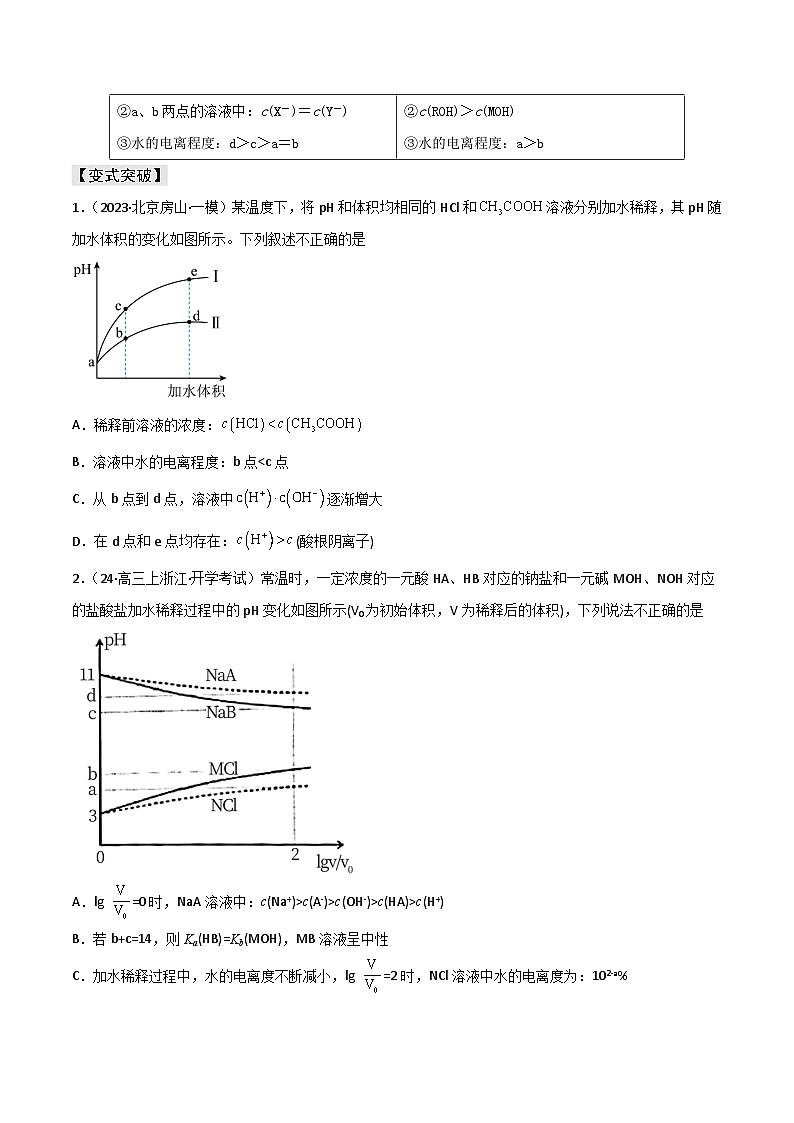
1.(2023·北京房山·一模)某温度下,将pH和体积均相同的HCl和溶液分别加水稀释,其pH随加水体积的变化如图所示。下列叙述不正确的是
A.稀释前溶液的浓度:
B.溶液中水的电离程度:b点c(A-)>c(OH-)>c(HA)>c(H+)
B.若b+c=14,则Ka(HB)=Kb(MOH),MB溶液呈中性
C.加水稀释过程中,水的电离度不断减小,lg =2时,NCl溶液中水的电离度为:102-a%
D.lg =0时,c(A-)>c(B-);c(N+)>c(M+)
易错点二 滴定曲线
【易错典例】
例2(2024·甘肃平凉·模拟预测)室温下,某实验兴趣小组用溶液标定某盐酸浓度,用甲基橙作指示剂,滴定曲线如图丁所示。下列说法正确的是
A.滴定中溶液应该盛放在乙仪器中
B.读数时,应双手一上一下持滴定管
C.标准溶液吸收了空气中的,会使测得的盐酸浓度偏大
D.滴定终点在b区域
【解题必备】滴定曲线
【变式突破】
3.(2024·河南·三模)已知AG的定义为,室温下用0.1的HCl溶液滴定10.00mL 0.1某一元碱MOH溶液,滴定过程中AG与HCl溶液体积变化关系如图所示。下列说法正确的是
A.MOH的电离常数的数量级为
B.A点时水的电离程度最大
C.A点时加入HCl溶液的体积等于10.00mL
D.B点时溶液中存在:
4.(2024·北京·一模)向10mLHCOOH-NH4Cl混合溶液(浓度均为0.1ml·L−1)中滴加0.1ml·L−1NaOH溶液,并监测溶液pH变化,实验数据如图。由该实验可得到的结论是
A.HCOOH电离方程式为HCOOH=H++HCOO−
B.由a点数据可推出电离能力:HCOOH>NH3·H2O
C.b点溶液中的OH−主要来自HCOO−水解
D.0.05ml·L−1氨水的pHb>a
6.(2024·新疆·二模)缓冲溶液在生产生活中有广泛应用,某缓冲溶液存在和缓冲对。常温下,该水溶液中各缓冲对微粒浓度之比的对数值lgG[G表示或与溶液pH的变化关系如图所示(已知:常温下,H3YO4的电离平衡常数为
下列说法不正确的是
A.H2XO3的Ka1的数量级为10-7
B.a→b的过程中,水的电离程度逐渐增大
C.当溶液pH逐渐增大时,逐渐增大
D.当时,
易错点四 分布系数图像
【易错典例】
例4(2024·云南曲靖·一模)常温下,向一定浓度溶液中加入NaOH固体,保持溶液体积和温度不变,测得pH与―1gX[X为、、]变化如图所示。下列说法错误的是
A.曲线N表示随pH的变化
B.常温下,的的数量级为
C.从a点至b点溶液中水的电离程度逐渐增大
D.a点溶液中:
【解题必备】分布系数图像[说明:pH为横坐标、分布系数(即组分的平衡浓度占总浓度的分数)为纵坐标]
【变式突破】
7.(2024·云南大理·二模)为二元弱酸,常温下,现配制一组的溶液,在不同pH环境下,不同形态的含X粒子(、、)的分布系数(平衡时某种含X粒子的物质的量占所有含X粒子物质的量之和的分数)如图所示。下列说法正确的是
A.a点对应的溶液的pH为7.6
B.在NaHX溶液中存在
C.c点对应的溶液中存在
D.室温下,a、b、c三点对应的溶液中,由水电离出的与的乘积数值由大到小顺序:a>b>c
8.(2024·云南·模拟预测)25℃时,用0.1溶液滴定同浓度的溶液,被滴定分数与值、微粒分布分数,X表示、或]的关系如图所示,下列说法正确的是
A.用溶液滴定0.1溶液可以用酚酞作指示剂
B.25℃时,第二步电离平衡常数
C.c点溶液中:
D.a、b、c、d四点溶液中水的电离程度:
考点精练
1.(2024·山东·二模)一定温度下,M2+在不同pH的Na2A溶液中存在形式不同,Na2A溶液中pM[pM=-lgc(M2+)]随pH的变化如图1,Na2A溶液中含A微粒的物质的量分数随pH的变化如图2。
已知①MA,M(OH)2均为难溶物;②初始c(Na2A)=0.2ml/L。
下列说法错误的是
A.c(A2-)=c(H2A)时,pH=8.5
B.初始状态a点发生反应:A2-+M2+=MA↓
C.I曲线上的点满足c(M2+)·c2(OH-)=Ksp[M(OH)2]
D.初始状态的b点,平衡后溶液中存在c(A2-)+c(HA-)+c(H2A)=0.2ml/L
2.(2024·辽宁沈阳·模拟预测)常温下,用NaOH溶液滴定磷酸的稀溶液,溶液的与或或的关系如图所示,下列说法错误的是
A.直线b表示与的关系
B.Y点溶液的
C.的平衡常数为
D.等浓度的溶液与溶液按体积比混合后,
3.(2024·江西景德镇·二模)常温下向饱和溶液(始终有固体存在)中滴加HCl溶液或者NaOH溶液调节pH,测得溶液中浓度的对数lg(Ca)与溶液的pH之间的关系如下图。已知的电离常数的负对数:,;下列说法正确的是
A.溶液中始终存在:
B.的数量级为
C.pH=7时,
D.A点时,
4.(2024·江西新余·二模)为三元弱酸,在溶液中存在多种微粒形态。将溶液滴到溶液中,各种含R微粒的分布分数随变化曲线如图所示。下列说法正确的是
A.的
B.当调至11~12时发生反应的离子方程式为:
C.时,溶液中
D.时,溶液中
5.(2024·辽宁·二模)常温下,向饱和溶液[有足量固体]中滴加氨水,发生反应:,溶液中与的关系如图所示,其中表示的浓度,单位为。下列说法正确的是
A.表示溶液中与的关系
B.的溶度积常数
C.时,溶液中:
D.的平衡常数
6.(2024·陕西西安·二模)常温下,在含有(s)的溶液中,一定pH范围内,存在平衡:;;;。平衡常数依次为、、、。已知、、、随pH变化关系如图所示。其中,和交点,和交点为,和交点为。下列说法错误的是
A.直线表示的变化情况
B.N点时,
C.随pH增大,溶液中含A微粒的总浓度一直增大
D.
7.(2024·天津河西·二模)现有的HCl和的混合溶液10mL,常温下用的NaOH标准溶液进行滴定。滴定过程中溶液的pH随[]的变化曲线如下图所示。下列说法正确的是
A.点a:
B.由点b数据推知约为
C.点c:
D.溶液中水的电离程度:点d7
21.(2024·四川成都·三模)秦俑彩绘中含有铅白和黄色的。常温下,和黄色的在不同溶液中分别达到溶解平衡时pM(阳离子浓度的负对数)与pR(阴离子浓度的负对数)的关系如图所示。下列说法正确的是
A.表示达到沉淀溶解平衡时pM与pR的关系
B.在1ml/L的KI溶液中,的溶解度为ml/L
C.对于分散质,X点:
D.向浓度均为0.lml/L的、NaI的混合溶液中滴入溶液,先产生黄色沉淀
22.(2024·福建漳州·三模)已知为二元弱酸,且,向溶液中逐滴加入一元弱酸HB溶液,溶液中的离子浓度变化关系如图所示:
下列说法错误的是
A.为随的变化关系
B.的数量级为
C.NaHA溶液中:
D.向溶液中滴入足量HB溶液的离子方程式为
23.(2024·北京朝阳·一模)常温下,用0.20ml·L-1盐酸滴定·L-1NH3·H2O溶液,所得溶液的pH、NH4+和NH3·H2O的物质的量分数(x)与滴加盐酸体积的关系如图所示。下列说法不正确的是
A.曲线①代表x(NH3·H2O)
B.当溶液显中性时,滴入盐酸的体积小于25.00mL
C.NH3·H2O的电离常数约为1×10-9.26
D.a点的溶液中存在c(NH)=c(NH3·H2O)>c(Cl-)
24.(2024·河南信阳·二模)已知的电离常数,,常温下,难溶物在不同浓度盐酸(足量)中恰好不再溶解时,测得混合液中与的关系如图所示,下列说法正确的是
A.约为
B.点:
C.点:约为
D.直线上任一点均满足:
25.(2024·湖南·二模)盐酸与碳酸钠溶液相互滴定,下图为反应过程中、、微粒浓度以及pH随溶液总体积变化曲线。下列说法不正确的是
A.上图是盐酸滴定碳酸钠溶液的曲线变化图
B.
C.碳酸的电离平衡常数数量级是
D.已知草酸酸性大于碳酸,若用同浓度溶液代替溶液,其它实验条件不变,则A点下移
①HY为强酸、HX为弱酸
②a、b两点的溶液中:c(X-)=c(Y-)
③水的电离程度:d>c>a=b
①MOH为强碱、ROH为弱碱
②c(ROH)>c(MOH)
③水的电离程度:a>b
氢氧化钠滴定等浓度等体积的盐酸、醋酸
盐酸滴定等浓度等体积的氢氧化钠、氨水
曲线起点不同:强碱滴定强酸、弱酸的曲线,强酸起点低;强酸滴定强碱、弱碱的曲线,强碱起点高
突跃点变化范围不同:强碱与强酸反应(强酸与强碱反应)的突跃点变化范围大于强碱与弱酸反应(强酸与弱碱反应)
室温下,当等体积、等浓度的一元强碱和一元强酸反应时,pH=7;但当等体积、等浓度的一元强碱和一元弱酸(或一元强酸和一元弱碱)反应时,pH>7(或pH
相关试卷
这是一份新高考化学三轮复习考前冲刺练习易错专题16 化学实验基础(2份打包,原卷版+解析版),文件包含新高考化学三轮复习考前冲刺练习易错专题16化学实验基础原卷版docx、新高考化学三轮复习考前冲刺练习易错专题16化学实验基础解析版docx等2份试卷配套教学资源,其中试卷共50页, 欢迎下载使用。
这是一份新高考化学三轮复习考前冲刺练习易错专题13 化学平衡图像和计算(2份打包,原卷版+解析版),文件包含新高考化学三轮复习考前冲刺练习易错专题13化学平衡图像和计算原卷版docx、新高考化学三轮复习考前冲刺练习易错专题13化学平衡图像和计算解析版docx等2份试卷配套教学资源,其中试卷共59页, 欢迎下载使用。
这是一份新高考化学三轮复习考前冲刺练习易错专题10 反应机理(2份打包,原卷版+解析版),文件包含新高考化学三轮复习考前冲刺练习易错专题10反应机理原卷版docx、新高考化学三轮复习考前冲刺练习易错专题10反应机理解析版docx等2份试卷配套教学资源,其中试卷共49页, 欢迎下载使用。









