

四川省雅安市芦山中学2023-2024学年高三上学期入学考试++化学试题
展开命题人:卫雨露
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
全卷满分100分,考试时间75 分钟。
注意事项:
1.答题前,考生务必将自己的姓名、班级、考号用0.5毫米的黑色墨水签字笔填写在答题卡上。并检查条形码粘贴是否正确。
2.选择题使用2B铅笔填涂在答题卡对应题目标号的位置上,非选择题用0.5毫米黑色墨水签字笔书写在答题卡对应框内,超出答题区域书写的答案无效;在草稿纸、试题卷上答题无效。
3.考试结束后,将答题卡收回。
可能用到的相对原子质量:H- 1 C- 12 N-14 O- 16 Na-23 S-32 Cl-35.5 Fe-56
第 Ⅰ 卷
本卷共14小题。每小题 3 分,共 42 分。在每个小题给出的四个选项中,只有一项是符合题目要求的。
1. 化学与社会紧密相关,下列说法错误的是( )
A. 明矾可用于自来水的消毒杀菌
B. 食醋可用于除水垢
C. 夏天超市用干冰给物质降温
D. Si3N4可用于制作高温结构陶瓷
2. 下列反应的离子方程式正确的是( )
A. 碳酸氢铵溶液中滴加过量澄清石灰水:Ca(OH)2 + 2HCO = CaCO3↓+ 2H2O + CO
B. 向BaCl2溶液中通入CO2:Ba2++ H2O + CO2 = BaCO3↓+2H+
C. 印刷电路板反应原理:Fe3++ Cu = Fe2++Cu2+
D. 用稀硝酸洗涤做过银镜反应试管:3Ag + 4H+ + NO = 3Ag+ + 2H2O + NO↑
3. 下列说法正确的是( )
A. 正戊烷的沸点低于异戊烷
B 金刚石晶体中,碳原子数目与碳碳键数目之比1:4
C. SCl2的空间结构为V形,中心原子的杂化方式为sp3
D. 1ml[TiCl(H2O)5]Cl2▪H2O和足量AgNO3溶液反应,能产3ml AgCl
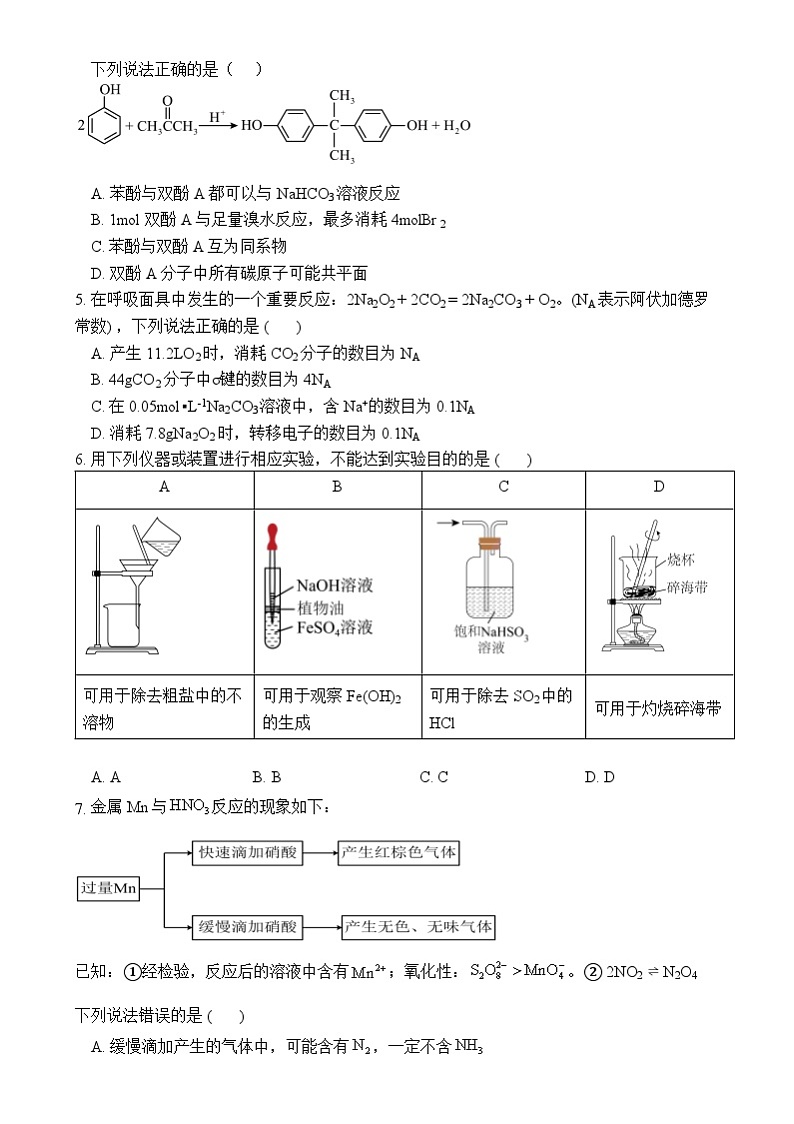
4. 双酚A是重要的有机化工原料,可用苯酚和丙酮利用以下原理来制备。
下列说法正确的是( )
A. 苯酚与双酚A都可以与NaHCO3溶液反应
B. 1ml双酚A与足量溴水反应,最多消耗4mlBr2
C. 苯酚与双酚A互为同系物
D. 双酚A分子中所有碳原子可能共平面
5. 在呼吸面具中发生的一个重要反应:2Na2O2 + 2CO2 = 2Na2CO3 + O2。(NA表示阿伏加德罗常数) ,下列说法正确的是 ( )
A. 产生11.2LO2时,消耗CO2 分子的数目为NA
B. 44gCO2 分子中σ键的数目为4NA
C. 在0.05ml▪L-1Na2CO3溶液中,含Na+的数目为0.1NA
D. 消耗7.8gNa2O2 时,转移电子的数目为0.1NA
6. 用下列仪器或装置进行相应实验,不能达到实验目的的是 ( )
A. A B. B C. C D. D
A
B
C
D
可用于除去粗盐中的不溶物
可用于观察Fe(OH)2的生成
可用于除去SO2中的HCl
可用于灼烧碎海带
金属Mn与反应的现象如下:
已知:①经检验,反应后的溶液中含有;氧化性:。② 2NO2 ⇌ N2O4
下列说法错误的是 ( )
A. 缓慢滴加产生的气体中,可能含有,一定不含
B. 快速滴加实验中,硝酸表现酸性、强氧化性
C. 收集快速滴加过程中获得的红棕色气体,干燥后会得到纯净的
D.向缓慢滴加实验所得溶液中加入,溶液变为紫红色
8.亚砷酸铵,易溶于水,可利用(分子结构如图)制备,该反应的化学方程式为。下列说法错误的是 ( )
A. 的的杂化形式为杂化
B. 砷的原子结构示意图为
C. 中阳离子的空间结构为正四面体形
D. 中元素的电负性由大到小的顺序为
9. 萤石是制作光学玻璃的原料之一,其主要成分氟化钙的晶胞结构如图所示。
下列说法错误的是 ( )
A. 一个晶胞中有4个Ca2+
B. 每个 Ca2+周围距离最近且等距的F-有8个
C. 氟化钙晶体中只含纯粹的离子键
D. 基态氟原子核外电子的原子轨道有四种取向
10. 下列实验操作及现象和所得的结论均正确的是 ( )
A. A B. BC. CD. D
11. X、Y、Z、W是原子序数依次增大的短周期主族元素,X的一种同位素可用于测定文物的年代,其中X与Z同族,Y与X同周期,Y的第一电离能高于同周期的相邻元素,W的原子序数是X原子价电子数的4倍,下列说法正确的是 ( )
A. 氢化物的沸点:X<Y B. Y在元素周期表中位于s区
C. 最高价含氧酸的酸性:W>X>Z D. X、Z形成的单质的晶体类型相同
12. 造纸、印刷等工业废水中含有大量的硫化物(主要成分为),可用如图转化方式除去,则下列说法错误的是 ( )
A. 溶液中存在
B. 反应②和③的转移电子数相等时,
还原剂之比为
C. 在废水处理过程中,为催化剂,
O2为氧化剂
反应④中Na2S与Na2SO3等物质的量反应,
反应的化学方程式为
13. CO2与 H2催化重整制取CH4的反应方程式为CO2(g)+4H2(g)⇌CH4(g)+2H2O(g) △H= -164.9kJ/ml,下列关于该反应的说法正确的是( )
A.4v 正( CO2)= v逆(H2), 表明反应达平衡状态
B. 该反应放热,在任意温度下都能自发进行
C. 增大压强,平衡向右移动,平衡常数K 增大
D.升温可加快反应速率并提高CH4的平衡产率
14. 某化学学习小组探究FeSO4与“84消毒液的反应过程,向酸化的FeSO4溶液中逐滴滴入“84消毒液,780s时停止滴入;滴加过程中bc、cd段产生刺激性气味的气体。采用pH传感器测得溶液的pH随时间t(s)的变化曲线如图所示。下列说法错误的是 ( )
A. ab段中有部分Fe2+ 变成了Fe3+
B. bc段的主要反应为
2ClO- + 2Fe2+ + 2OH- +2H2O= Cl2↑ + 2Fe(OH)3↓
C. cd段产生刺激性气味气体的反应为
ClO- + Cl- + 2H+ = Cl2↑ + H2O
D. de段pH减小的原因是氯气溶于水反应产生酸性物质
第 Ⅱ 卷
本卷共 4 小题。每空2分,共58 分。
15. (14分)铁是人类较早使用的金属之一,铁及其化合物在生产、生活中有重要的用途。运用所学知识回答下列问题。
(1)实验室鉴别Fe(OH)3胶体与饱和FeCl3溶液的方法是___________。
(2)电子工业用FeCl3溶液腐蚀敷在绝缘板上的铜,制造印刷电路板。
①发生反应的离子方程式为___________。
②为检验FeCl3腐蚀铜后所得溶液中含有Fe2+ ,应使用的试剂为_________。
③欲从腐蚀后的废液中回收铜并重新获得FeCl3溶液循环利用,现有下列试剂:
A.浓硝酸B.铁粉 C.氯气 D.烧碱 E.浓氨水,需要用到的试剂除盐酸外还需要________(选填字母)。
纳米Fe/Ni复合材料,可有效去除酸性废水中的NO3-,其反应过程(Ni不参与反应)如图所示:
①H、N、O三种元素的电离能从大到小的顺序是___________。
②反应ⅱ的离子方程式为___________。
③假设每步反应都能彻底进行,则反应i和ⅱ中消耗还原剂的质量之比为___________。
实验操作及现象
实验结论
A
把分别蘸有浓硫酸和浓氨水的玻璃棒靠近,有白烟产生
白烟为(NH4)2SO4
B
室温下,用pH计分别测定浓度为0.1ml▪L-1的HClO溶液和0.1ml▪L-1的HF溶液的pH,前者的pH大于后者
HClO的酸性大于HF
C
向亚硫酸钠试样中滴入盐酸酸化的Ba(NO3)2溶液,生成白色沉淀
试样已氧化变质
D
检验FeCl3溶液中是否含有Fe2+时,可滴入适量酸性KMnO4溶液,溶液紫红色褪去
不能证明溶液中含有Fe2+
16. (16分)化学创造美好生活。磷酸锌是一种绿色环保涂料,实验室用锌灰(含ZnO、PbO、CuO、FeO、Fe2O3、 SiO2等)为原料制备Zn3(PO4)2▪4H2O。(难溶于水)的流程如下,回答下列问题:
已知:
△anjiax
①本实验条件下高锰酸钾的还原产物为MnO2。
②ZnCO3▪2Zn(OH)2▪H2O+2H3PO4===Zn3(PO4)2▪4H2O+2H2O+CO2↑。
(1)滤渣I的主要成分为___________。
(2)步骤I的主要目的是除去铁元素,需先将溶液的pH调至5.0,再滴加KMnO4溶液,滴加时的离子方程式为___________。
(3)步骤Ⅱ的主要目的是除去铜元素,试剂a为___________(填化学式)。
(4)步骤Ⅲ在加热条件下生成一种温室气体和沉淀ZnCO3▪2Zn(OH)2▪H2O,其离子方程式为___________。
(5)步骤IV反应结束后,得到Zn3(PO4)2▪4H2O的操作包括________、_________和干燥。
(6)锌的某种氧化物的立方晶胞结构如下图所示,晶胞参数为r nm。
(晶胞中a为氧,b为锌)
①写出基态Zn原子的价层电子排布式___________。
②Zn和O之间最短的距离为___________nm。
17.(14分)甲醛(HCHO) 在石油化工、医药及能源等行业均有广泛用途,工业上可通过甲醇脱氢 的方法合成甲醛,反应原理为:CH3OH(g) = HCHO(g) + H2(g),回答下列问题:
(1)已知:
CH3OH的平衡体积分数%
反应CH3OH(g) = HCHO(g) + H2(g) △H3 > 0, 则 △H3= kJ/ml, 该反应涉及的
C、H、O元素的电负性由大到小的顺序是 。
(2)在密闭容器中加入1 ml CH3OH 和适量催化剂Ag。
发生反应CH3OH(g) = HCHO(g) + H2(g),CH3OH(g) 的
平衡体积分数随压强变化的曲线如图所示。
①图中温度T1 T2(填“>”,“<” 或“=”),
压强/kPa
判断的依据是 。
②T1温度下,根据图中点 A(80kPa,40%),计算该处CH3OH的平衡转化率为 ( 保留2位小数)。
(3)借助电解技术,可由甲醛为原料制得乙二醇(HOCH2CH2OH),装置如图所示。
H2O HCHO
H+
O2 HOCH2CH2OH
质子交换膜
惰性电极
惰性电极
①阴极上的反应式为 。
②产生标准状况下2.24 LO2,理论上可制得
乙二醇 ml。
18. (14分)有机化学中有很多人名反应,德国化学家Beckmann(贝克曼)在研究薄荷酮肟的空间排列时,发现了酮肟在酸性催化剂如硫酸、多聚磷酸等作用下可以重排成酰胺,后来被称之为Beckmann重排反应。
该反应在工业上的一个重要应用是合成己内酰胺(题目中用G表示),从而进一步合成
尼龙-6(锦纶),其反应过程如下:
(1)有机物B的名称___________。
(2)写出有机物E的结构简式___________。
(3)B→C和D→E的反应类型分别为___________、___________。
(4)有机物C转化为D所需的试剂和条件___________。
(5)由有机物F合成G反应的化学方程式为 。
(6)有机物F有多种同分异构体,写出一种满足以下条件的有机物结构简式___________。
①只含有一个环,且为六元环;②核磁共振氢谱显示有3组峰;③无碳碳双键。
四川省绵阳南山中学实验学校2023-2024学年高一上学期入学考试化学试题: 这是一份四川省绵阳南山中学实验学校2023-2024学年高一上学期入学考试化学试题,共6页。
四川省绵阳南山中学2023-2024学年高二下学期入学考试化学试题: 这是一份四川省绵阳南山中学2023-2024学年高二下学期入学考试化学试题,文件包含四川省绵阳南山中学2023-2024学年高二下学期入学考试化学试题docx、2024年春入学考试化学答题卡doc等2份试卷配套教学资源,其中试卷共13页, 欢迎下载使用。
14,四川省绵阳南山中学2023-2024学年高二下学期入学考试化学试题: 这是一份14,四川省绵阳南山中学2023-2024学年高二下学期入学考试化学试题,共10页。试卷主要包含了考试结束后将答题卡收回等内容,欢迎下载使用。












