

江苏省南通市海安高级中学2024-2025学年高三上学期9月月考化学试题(解析版)
展开
这是一份江苏省南通市海安高级中学2024-2025学年高三上学期9月月考化学试题(解析版),共22页。试卷主要包含了5 K-39 C-59, 反应可制含氯消毒剂等内容,欢迎下载使用。
注意:本试卷分第一部分选择题和第二部分非选择题,共100分,考试时间75分钟。
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 S-32 C1-35.5 K-39 C-59
单项选择题:本题包括13小题,每小题3分,共计39分。每小题只有一个选项符合题意。
1. 2024年4月24日是第九个“中国航天日”,主题是“极目楚天共襄星汉”。下列有关中国空间站说法不正确的是
A. 太阳能电池中的单晶硅——半导体材料
B. 外表面的高温结构碳化硅陶瓷——硅酸盐材料
C. 外层的热控保温材料石墨烯——无机材料
D. 外壳的烧蚀材料之一酚醛树脂——高分子材料
【答案】B
【解析】
【详解】A.太阳能电池中的单晶硅导电性介于导体和半导体之间,属于半导体材料,故A正确;
B.外表面的高温结构陶瓷碳化硅属于无机非金属材料,故B错误;
C.外层的热控保温材料石墨烯主要成分是碳单质,属于无机材料,故C正确;
D.外壳的烧蚀材料之一酚醛树脂是高聚物,属于高分子材料,故D正确;
答案选B。
2. 反应可制含氯消毒剂。下列说法正确的是
A. HCl和NaCl所含化学键类型相同
B. 是由极性键构成的非极性分子
C. 的空间结构为三角锥形
D. 中子数为18的Cl原子:
【答案】C
【解析】
【详解】A.氯化氢是含有共价键的共价化合物,氯化钠是含有离子键的离子化合物,两者所含化学键类型不同,A错误;
B.中的O—H键为极性键,空间结构为V型,是由极性键构成的极性分子,B错误;
C.氯酸根离子中氯原子的价层电子对数为4、孤对电子对数为1,离子的空间构型为三角锥型,C正确;
D.Cl的原子序数为17,则中子数为18的Cl原子:,D错误;
故选C。
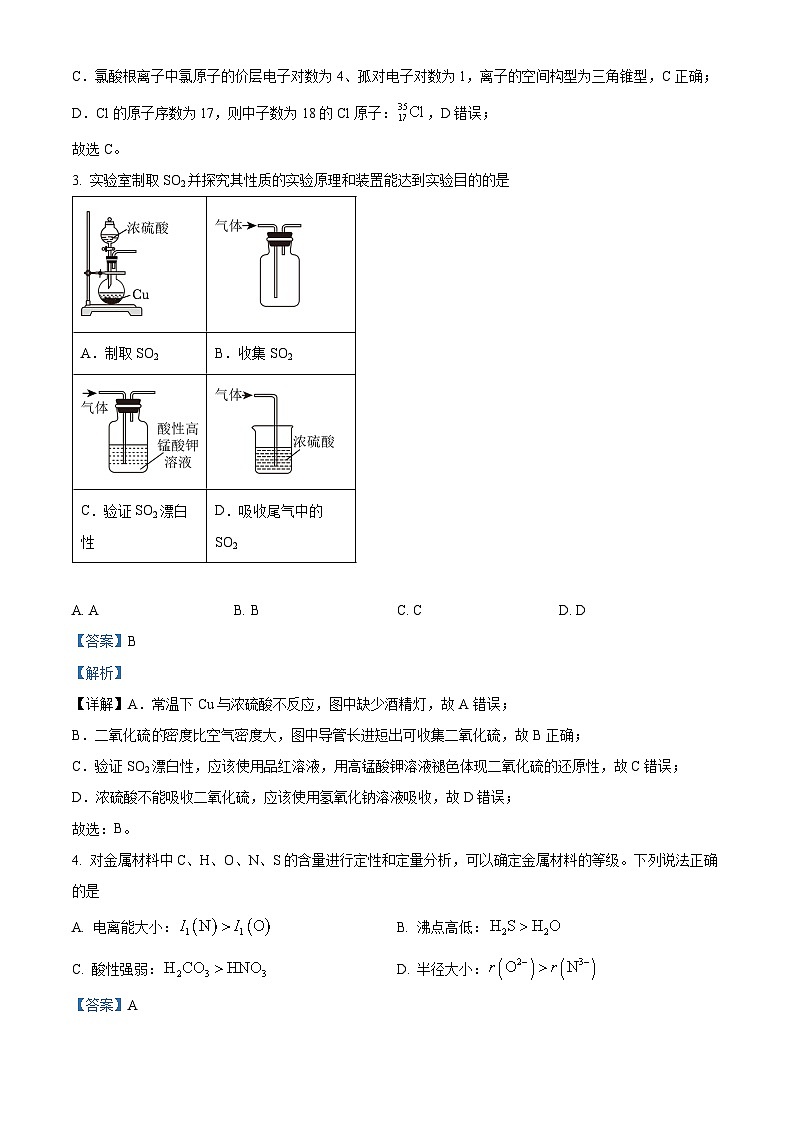
3. 实验室制取SO2并探究其性质的实验原理和装置能达到实验目的的是
A. AB. BC. CD. D
【答案】B
【解析】
【详解】A.常温下Cu与浓硫酸不反应,图中缺少酒精灯,故A错误;
B.二氧化硫密度比空气密度大,图中导管长进短出可收集二氧化硫,故B正确;
C.验证SO2漂白性,应该使用品红溶液,用高锰酸钾溶液褪色体现二氧化硫的还原性,故C错误;
D.浓硫酸不能吸收二氧化硫,应该使用氢氧化钠溶液吸收,故D错误;
故选:B。
4. 对金属材料中C、H、O、N、S的含量进行定性和定量分析,可以确定金属材料的等级。下列说法正确的是
A. 电离能大小:B. 沸点高低:
C. 酸性强弱:D. 半径大小:
【答案】A
【解析】
【详解】A.N的2p轨道有三个电子半充满,因此第一电离能,故A正确;
B.水存在分子间氢键,沸点较高,因此沸点:,故B错误;
C.元素的非金属性越强,最高价氧化物对应的水化物酸性越强,N的非金属性强于C,因此酸性:,故C错误;
D. O2-和N3-的核外电子排布相同,而N的核电荷数小,半径:,故D错误;
故选A。
阅读下列材料,完成下面小题
周期表中第ⅤA族元素及其化合物应用广泛。以为原料可制得、等产品;可以用来防治仓库害虫,次磷酸()是一元酸,具有较强还原性,可由与反应制得;砷化镓可用作半导体材料,其晶胞结构如图所示;锑(Sb)导电性能好,在电池行业有独特应用。
5. 下列说法正确的是
A. 中心原子轨道杂化方式为
B. 与足量NaOH溶液反应可生成
C. 砷化镓化学式为
D. 中共价键键角是120°
6. 下列物质结构与性质或物质性质与用途具有对应关系的是
A. 氨与水分子之间形成氢键,在水中溶解度比大
B. 易挥发,用于防治害虫
C. 次磷酸是无色液体,可用作强还原剂
D. 砷化镓硬度大,可用作半导体材料
7. 新型电池充电时的工作原理如图所示。下列说法不正确的是
A. 放电时电极A为负极
B. 放电时化学能转化为电能
C. 放电时电极B的电极反应式为
D. 放电时理论上每生成转移
【答案】5. D 6. A 7. D
【解析】
【分析】为一元酸,与足量NaOH溶液发生反应;新型电池充电时Na+移向A电极,根据电解池内电路阳离子移向阴极,可知充电时A为阴极,B为阳极;放电时A为负极,B为正极。
【5题详解】
A.中心原子P价层电子对数为,P杂化方式为,故A错误;
B.为一元酸,与足量NaOH溶液发生反应,生成,故B错误;
C.根据晶胞图可知1个晶胞中含有4个Ga,个As,砷化镓化学式为,故C错误;
D.中N价层电子对数,孤电子对数为0,中N采取sp2杂化,离子为平面三角形,键角为120°,故D正确;
故答案为:D。
【6题详解】
A.氨与水分子之间形成氢键,有利于氨气在水中的溶解,所以在水中溶解度比大,故A正确;
B.有毒,用于防治害虫,故B错误;
C.次磷酸中P为+1价,可用作强还原剂,故C错误;
D.砷化镓具有优异的光学性能和电学性能,可用作半导体材料,故D错误;
故答案为:A。
【7题详解】
新型电池充电时Na+移向A电极,根据电解池内电路阳离子移向阴极,可知充电时A为阴极,B为阳极;放电时A为负极,B为正极。
A.根据分析可知放电时电极A为负极,故A 正确;
B.放电时原电池工作将化学能转化为电能,故B正确;
C.放电时电极B为正极,得电子发生还原反应,对应电极反应式为,故C正确;
D.放电时,理论上每生成转移,故D正确;
故答案:D。
8. 实验室以含锌废液(主要成分为ZnSO4,含少量的Fe2+、Mn2+)为原料制备ZnCO3·2Zn(OH)2的实验流程如下:
下列说法正确的是
A. 过二硫酸钠(Na2S2O8)中硫元素的化合价为+7价
B. 氧化除锰后的溶液中存在:Na+、Zn2+、Fe2+、
C. 调节pH时试剂X可以选用Zn、ZnO、ZnCO3等物质
D. 沉锌时的离子方程式为3Zn2++6=ZnCO3·2Zn(OH)2↓+5CO2↑+H2O
【答案】D
【解析】
【分析】由题给流程可知,向含锌废液中加入过二硫酸钠溶液,将溶液中的亚铁离子氧化为铁离子,锰离子氧化为二氧化锰,过滤得到二氧化锰和滤液1;向滤液1中加入氧化锌或碳酸锌等调节溶液pH,将铁离子转化为氢氧化铁沉淀,过滤得到氢氧化铁和滤液2;向滤液2中加入碳酸氢铵溶液,将锌离子转化为ZnCO3·2Zn(OH)2沉淀,过滤得到滤液和ZnCO3·2Zn(OH)2。
【详解】A.过二硫酸钠中含有过氧链,分子中硫元素的化合价为+6价,故A错误;
B.由分析可知,氧化除锰后的溶液中存在的离子为Na+、Zn2+、Fe3+、,故B错误;
C.溶液中铁离子能与锌反应生成氯化亚铁和氯化锌,所以调节溶液pH时试剂X不能选用锌,故C错误;
D.沉锌时发生的反应为溶液中锌离子与碳酸氢根离子反应生成ZnCO3·2Zn(OH)2沉淀、二氧化碳和水,反应的离子方程式为3Zn2++6=ZnCO3·2Zn(OH)2↓+5CO2↑+H2O,故D正确;
故选D。
9. 有机物G的部分合成路线如下,下列推断正确的是
A. 上述转化中,只发生了取代反应
B. 1mlZ最多能与发生加成反应
C Y→Z转换时加入有利于反应进行
D. G分子中含有2个手性碳原子
【答案】C
【解析】
【详解】A.根据信息可知发生取代反应,发生取代反应,反应中碳碳双键变为碳碳单键,该反应不是取代反应,A错误;
B.Z结构中的苯环和羰基均可和氢气发生加成反应,1mlZ中的苯环和3mlH2发生加成反应,1ml羰基和1mlH2发生加成反应,最多能与发生加成反应,B错误;
C.Y→Z转换时加入防止苯酚被氧化,有利于反应进行,C正确;
D.饱和碳原子连接4个不同的原子或原子团为手性碳原子,G分子中含有1个手性碳原子,D错误;
故答案为:C。
10. 雌黄(As2S3)和雄黄(As4S4)都是自然界中常见的砷化物,中国自古有“信口雌黄”、“雄黄入药”之说。早期曾用作绘画颜料,因有抗病毒疗效也用来入药。砷元素有+2、+3 两种常见价态。一定条件下,雌黄和雄黄的转化关系如图所示。下列说法错误的是
A. 反应Ⅰ中Sn4+为氧化产物
B. 反应Ⅰ中As2S3和Sn²⁺恰好完全反应时,其物质的量a之比为2:1
C. 若反应Ⅱ中转移电子0.7 ml,则生成0.1mlSO2
D. 反应Ⅲ和Ⅳ均属于非氧化还原反应
【答案】B
【解析】
【详解】A.反应I中Sn元素化合价升高,Sn4+为氧化产物,A正确;
B.反应I方程式2As2S3+2Sn2++4H+=As4S4+2Sn4++2H2S↑,As2S3与Sn2+恰好完全反应的物质的量之比为1:1,B错误;
C.反应Ⅱ中As4S4+7O2=2As2O3+4SO2,转移28ml电子,生成4ml SO2,所以转移0.7ml电子,生成0.1ml SO2,C正确;
D.反应Ⅲ和Ⅳ中各元素化合价都没有变化,均属于非氧化还原反应,D正确;
本题选B。
11. 由下列实验事实可推导出结论的是
A. AB. BC. CD. D
【答案】D
【解析】
【详解】A.未告知NaClO溶液和溶液两种溶液的浓度大小,无法判断HClO、HNO2电离常数的相对大小, A错误;
B.向固体中加入过量饱和溶液有生成,只要满足就能生成沉淀,不能证明, B错误;
C.向苯酚钠溶液中通入少量,生成苯酚和碳酸氢钠证明(苯酚), C错误;
D.在溶液中加入乙醇,析出蓝色晶体,则表明在乙醇中的溶解度比在水中小,从而说明乙醇的极性比水的弱,D正确;;
选D。
12. 一种吸收再经氧化得到硫酸盐的过程如下图所示。室温下,用0.1ml/L的NaOH溶液吸收,若通入所引起的溶液体积变化和挥发可忽略,溶液中含硫物种的浓度。的电离常数为、。
下列说法正确的是
A. 若“吸收”后,则
B. 若“吸收”后溶液,则
C. 若“吸收”后,则溶液中
D. 若“吸收”后溶液,则氧化过程中主要反应为:
【答案】A
【解析】
【分析】采用NaOH溶液吸收SO2,再经氧化得到硫酸盐
【详解】A.若“吸收”后溶液即为Na2SO3溶液,则质子守恒:,A正确;
B.若“吸收”后溶液(溶液溶质为NaHSO3和Na2SO3), ,所以==0.624
相关试卷
这是一份江苏省南通市海安市2024-2025学年高三上学期开学考试+化学试题(无答案),共8页。试卷主要包含了下列说法正确的是,下列化学反应表示正确的是等内容,欢迎下载使用。
这是一份江苏省南通市海安高级中学2024-2025学年高三上学期9月月考化学试题,共11页。试卷主要包含了5 K-39 C-59,7ml,则生成等内容,欢迎下载使用。
这是一份江苏省南通市海安市2024-2025学年高三上学期开学考试+化学试题,共6页。









