



高中人教版 (2019)第二章 海水中的重要元素——钠和氯第三节 物质的量优质课件ppt
展开1.了解物质的量、阿伏加德罗常数、摩尔质量的含义和应用,体会定量研究对化学科学的重要作用2.能运用物质的量、 粒子数、摩尔质量之间的相互关系进行简单的计算3.从定量的角度认识宏观物质与微观粒子的相互关系,建构以n为中心的计算体系
外观越小的物质用集团计量越方便。
生活中不同的物质用一打计量12这一集团。
假如让10亿人来数一滴水里的水分子,每人每分钟数100个,日夜不停,需要30000多年才能数清!
思考1:18 mL水所含的水分子数为多少?
结论:微观粒子不方便以个数来计量!
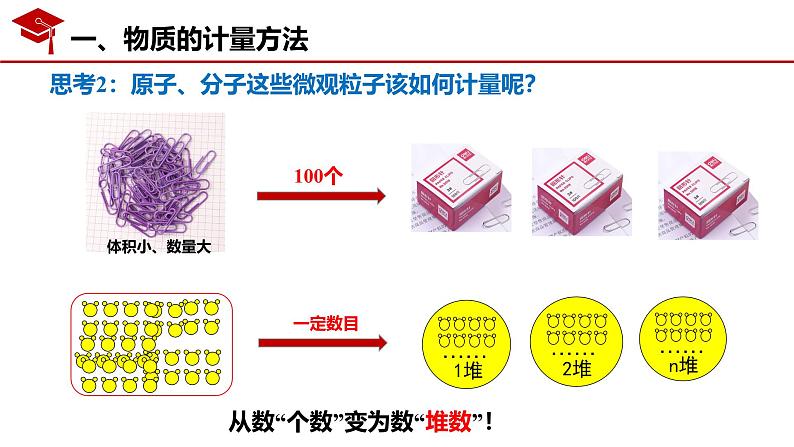
思考2:原子、分子这些微观粒子该如何计量呢?
从数“个数”变为数“堆数”!
表示含有一定数目粒子的集合体
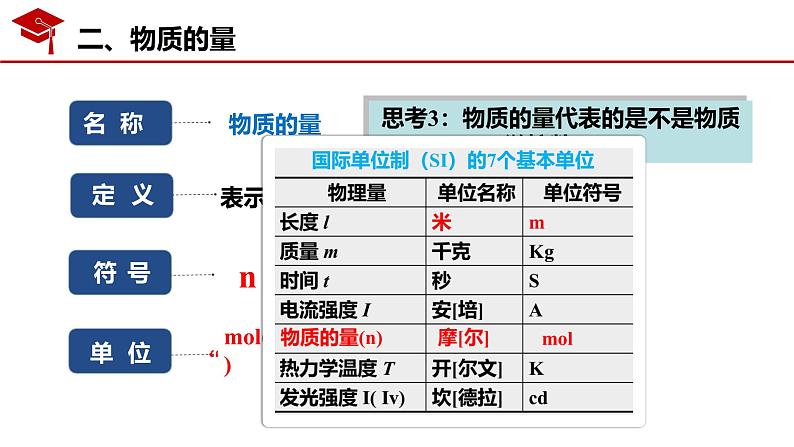
思考3:物质的量代表的是不是物质微粒数目?
1 ml 大米(鸡蛋) 1.5 ml O21 ml 氧原子0.5 ml H2O1 ml 氢 2 ml e-
【练习】判断下列说法是否正确,并加以说明
通过以上体验,你觉得“物质的量”这—物理量在使用时应该注意些什么?
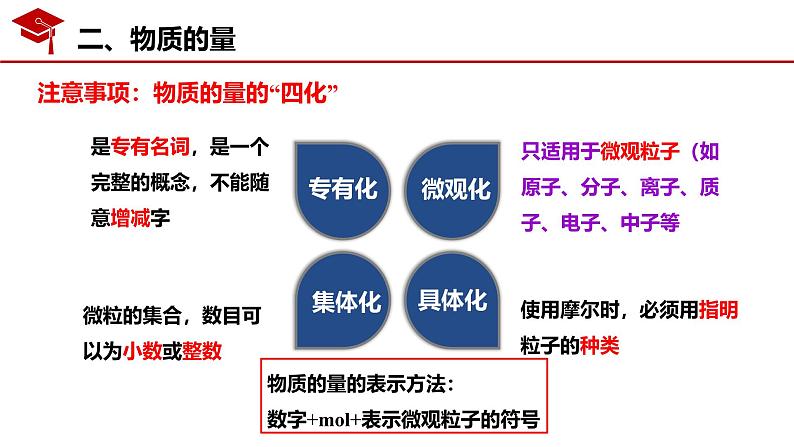
是专有名词,是一个完整的概念,不能随意增减字
注意事项:物质的量的“四化”
只适用于微观粒子(如原子、分子、离子、质子、电子、中子等
使用摩尔时,必须用指明粒子的种类
微粒的集合,数目可以为小数或整数
物质的量的表示方法:数字+ml+表示微观粒子的符号
思考4:1ml H2O中有多少水分子呢?
旧定义:1971年,第14届国际计量大会上,正式宣布“物质的量”成为国际单位制中的一个基本物理量,单位为摩尔。同时规定0.012kg12C中所含的碳原子数目作为1 ml的标准。【已知:一个12C原子的质量为1.993×10-26 kg】
新定义:2018年,第26届国际计量大会上决定不再以任何物质作为标准,而是以常数的方式定义"物质的量”:规定包含6.02214076×1023个微粒的集合体为1 ml的标准。
1 ml任何微观粒子所含的粒子数
阿伏加德罗常数(NA)
约为6.02×1023
(1)1ml H2O含水分子的个数___________(2)2 ml H2O含水分子的个数___________(3)NA个水分子是___________ml(4)0.5NA个水分子是___________ml(5)N个水分子的物质的量是___________ml。
根据以上五个小题,能否得出物质的量(n),阿伏加德罗常数(NA)与粒子数(N)的关系?
1 ml任何粒子的粒子数(N)
物质的量(n)、阿伏加德罗常数(NA)、粒子数(N)之间的关系
两种物质的微粒数(N)之比 == 物质的量(n)之比 N1:N2=n1:n2
物质的量与微粒数之间的关系
1 ml H2O中有?ml H和?ml O
1 2 1
NA 2 NA NA
1ml 2 ml 1ml
(1) 3ml H2SO4中含有_________ml H+; (2) 4ml O2中约含有_______________个O; (3) 10ml NaCl中含有________________个Na+; (4) 0.1 ml NH3中约含有_______________个H ,约含______________个N
8 × 6.02×1023
0.3 × 6.02×1023
0.1 × 6.02×1023
根据下表,请找出1ml物质的质量有什么规律?
思考5:1 ml任何粒子都含约6.02×1023个粒子,那1ml H2O的质量是多少?
1 ml任何粒子或物质的质量以克为单位时,其数值都与其相对分子(原子)质量相等
单位物质的量的物质所具有的质量
(1) Mg的摩尔质量是_____________,2ml O2的质量是________,1 ml Na+的质量是________(2) H2SO4的相对分子质量是________ ,摩尔质量是__________ , 2ml H2SO4的质量是___________(3) KCl的摩尔质量是___________,149g KCl对应的物质的量是_______
解:H2O的相对分子质量为18,摩尔质量为18 g/ml
N = n﹒NA = 1 ml × 6.02 × 1023 ml-1 = 6.02 × 1023
18 mL水中含有水分子数目为多少?
人教版 (2019)必修 第一册第三节 物质的量获奖ppt课件: 这是一份人教版 (2019)必修 第一册<a href="/hx/tb_c161983_t3/?tag_id=26" target="_blank">第三节 物质的量获奖ppt课件</a>,共18页。PPT课件主要包含了物质的量,通关秘籍,摩尔质量,老朋友的茶话会等内容,欢迎下载使用。
高中第三节 物质的量课文课件ppt: 这是一份高中第三节 物质的量课文课件ppt,共25页。PPT课件主要包含了符号NA,课堂练习等内容,欢迎下载使用。
高中化学第三节 物质的量说课课件ppt: 这是一份高中化学第三节 物质的量说课课件ppt,共24页。PPT课件主要包含了物质的量摩尔,阿伏加德罗常数,摩尔质量,课堂练习,1mol,05mol,5mol等内容,欢迎下载使用。













