






还剩15页未读,
继续阅读
所属成套资源:高中化学新教材同步必修第一册全册课件
成套系列资料,整套一键下载
高中化学新教材同步必修第一册 第4章 本章核心素养聚焦课件
展开
这是一份高中化学新教材同步必修第一册 第4章 本章核心素养聚焦课件,共23页。
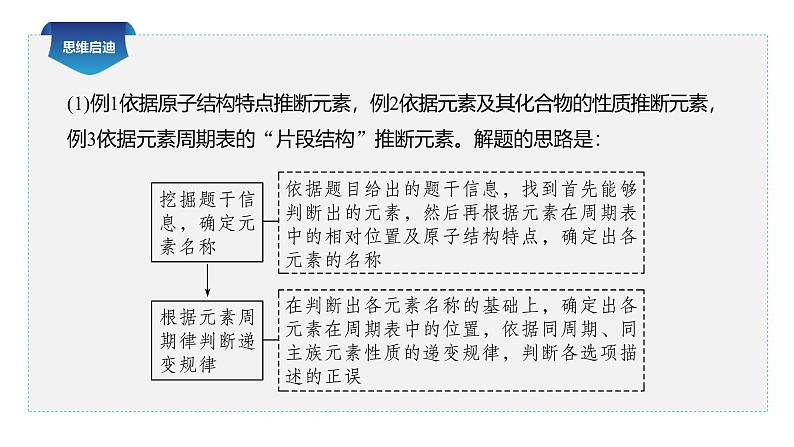
本章核心素养聚焦第四章 物质结构 元素周期律一、宏观辨识与微观探析化学研究的重点是在原子、分子水平上认识物质的结构、组成、性质和变化规律,并据此改造或创造物质。本章是从原子结构的角度认识元素及其物质的性质与变化规律,建立原子结构与元素性质、元素性质与物质性质的关系,会用原子结构的知识解释元素性质及其变化规律,能从元素周期表的构成、元素周期律的递变认知上,形成“结构决定性质”的观念,从宏观和微观相结合的视角分析与解决实际问题。例1 短周期元素a、b、c、d的原子序数依次增大,a的最外层电子数是电子层数的2倍,b的最外层电子数是电子层数的3倍,a、c的最外层电子数之和为6,d的核外电子数等于b的核外电子数加8。下列叙述错误的是A.a和b可形成气态化合物B.c的原子半径小于d的原子半径C.b和c可以形成化合物D.a和d最高价氧化物的水化物均呈酸性√解析 由题意可知a为碳,b为氧,c为镁,d为硫。C、O可以形成气态化合物CO、CO2等,A项正确;Mg、S同周期,原子半径:Mg>S,B项错误;MgO为化合物,C项正确;C、S的最高价氧化物对应的水化物分别为H2CO3、H2SO4,均呈酸性,D项正确。例2 A、B、C、D是原子序数依次增大的四种短周期元素,在所有物质中,A的单质密度最小,B的一种氧化物是温室气体;A、C组成的化合物常温下为液态,在短周期元素中,D的半径最大,则下列说法错误的是A.原子半径:D>B>CB.元素的非金属性:B>C>AC.A、B、C、D可以形成化合物D.A分别与B、C形成的简单化合物中,A与B形成的简单化合物的熔点低解析 由题意可知,A为氢,B为碳,C为氧,D为钠。原子半径:Na>C>O,A项正确;非金属性:O>C>H,B项错误;四种元素可形成化合物NaHCO3,C项正确;CH4和H2O相比,CH4为气体,熔点低,D项正确。√例3 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知Y、W的原子序数之和是Z的3倍,下列说法正确的是A.原子半径:X<Y<ZB.气态氢化物的稳定性:X>ZC.Z、W均可与Mg形成化合物D.最高价氧化物对应水化物的酸性:Y>W√解析 由题意可知,X为硅,Y为氮,Z为氧,W为氯。Si为第三周期元素,N、O为第二周期元素,原子半径:r(Si)>r(N)>r(O),A项错误;非金属性:O>Si,则气态氢化物的稳定性:H2O>SiH4,B项错误;O、Cl可与Mg形成MgO、MgCl2,均为化合物,C项正确;N、Cl最高价氧化物对应的水化物分别为HNO3和HClO4,酸性:HClO4>HNO3,D项错误。思维启迪(1)例1依据原子结构特点推断元素,例2依据元素及其化合物的性质推断元素,例3依据元素周期表的“片段结构”推断元素。解题的思路是:(2)解题的关键是熟知“位—构—性”之间的关系,并将周期表、原子的电子层结构、元素单质及其化合物的性质等内容结合起来进行综合运用,才能推断出相关元素的名称并熟悉它们所形成的单质及其化合物的化学性质,得出正确结论。 二、证据推理与模型认知“证据推理与模型认知”在本章的具体体现:利用元素在元素周期表中的位置和原子结构分析、预测、比较元素及其化合物的性质,能用原子结构解释元素性质及其变化规律,并能结合实验及事实进行说明。在此基础上,建立相关知识应用的思维方法模型,如10电子、18电子微粒的识别与判断,微粒半径大小比较,元素金属性、非金属性强弱比较,元素“位—构—性”关系的应用、化学键类型的判断等。例4 下列关于微粒半径大小的叙述中不正确的是A.同一元素的不同粒子,核外电子数越多,半径越大B.同一元素形成的多种价态的离子,价态越低,半径越小C.同一元素的原子半径小于相应的阴离子半径D.同一元素的原子半径大于相应的阳离子半径√解析 同一元素的原子半径小于相应阴离子的半径,大于相应阳离子的半径,即同一元素粒子的核外电子数越多,其半径越大;同一元素形成的多种价态的离子,价态越低,半径越大。例5 已知同周期X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是HZO4>H2YO4>H3XO4,下列判断正确的是A.原子半径按X、Y、Z的顺序逐渐减小B.单质的氧化性按X、Y、Z的顺序减弱C.三种元素阴离子的还原性按X、Y、Z的顺序增强D.气态氢化物的稳定性按X、Y、Z的顺序减弱√解析 同周期X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是HZO4>H2YO4>H3XO4,可知X、Y、Z的原子序数为X<Y<Z。同周期元素从左到右单质的氧化性逐渐增强,阴离子的还原性逐渐减弱,原子半径逐渐减小,气态氢化物的稳定性逐渐增强,可知正确选项为A。例6 现有部分短周期元素的性质或结构如下表:(1)X的原子结构示意图________。解析 由表中信息推断出X为S,Y为Cl,Z为I,则根据元素非金属性强弱判断的依据和同主族元素非金属性的递变规律可解答本题。(2)Z在元素周期表中的位置________________。(3)判断非金属性:X____Y(填“>”“<”或“=”,下同)。(4)判断非金属性:Y____Z,写出结构上的原因____________________________________________________________________。第五周期ⅦA族<>二者最外层电子数相同,但I的电子层数多,原子半径大,得电子能力弱思维启迪通过构建“位—构—性”关系认知模型,发展对元素化合物化学性质的认知模型;从“物质类别——一般性质——氧化性和还原性”二维模型发展到“物质类别——一般性质——氧化性和还原性——相似性和递变性”三维模型。三、科学探究与创新意识“科学探究与创新意识”在本章的体现:根据元素周期表和元素周期律研究发现新元素并预测其性质,体会元素周期表和元素周期律在学习元素化合物知识与科学研究中的重要作用。设计实验探究同主族元素(碱金属元素、卤族元素)性质的相似性和递变性,设计实验并结合化学事实探究同周期(第三周期)元素性质递变规律。在探究过程中,运用科学的方法通过观察实验,收集、记录实验现象和数据,分析总结实验结论,并敢于质疑,勇于创新。例7 某校化学学习小组分别设计了一组实验来探究元素周期律。第一小组根据元素非金属性与其对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验探究。[查阅资料]Ⅰ.常温下浓盐酸与高锰酸钾能反应生成氯气。Ⅱ.H2SiO3难溶于水。实验药品:大理石、碳酸钠粉末、稀硝酸、硅酸钠溶液。[探究过程](1)第一小组为比较N、C、Si的非金属性强弱,以图1装置进行实验:①烧杯C中现象为__________________,发生反应的离子方程式为__________________________________。②实验预期结论:_________________。③存在问题:__________________________________________________。溶液变浑浊非金属性:C>Si稀硝酸有一定的挥发性,影响C和Si非金属性强弱的判断解析 验证元素的非金属性与其对应最高价含氧酸之间的关系,可根据强酸制弱酸的反应原理,用稀硝酸与大理石反应生成二氧化碳,再将二氧化碳通入硅酸钠溶液中,生成硅酸沉淀。由此可说明硝酸、碳酸及硅酸酸性的强弱,但硝酸有挥发性,影响了最后结果的判断。(2)第二小组设计了如图2装置来验证卤素单质的氧化性,A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉碘化钾试纸、湿润的红色纸条。①写出A处反应的离子方程式:_______________________。②B处实验现象是__________。③实验预期结论:______________________。④存在问题:________________________。Cl2+2Br-===Br2+2Cl-试纸变蓝氧化性:Cl2>Br2>I2无法判断Br2和I2的氧化性解析 氯气能与溴化钠溶液发生置换反应,生成单质溴和氯化钠;氯气能与碘化钾溶液发生置换反应,生成单质碘,碘遇淀粉变蓝色;但无法判断Br2和I2的氧化性。例8 某化学课外兴趣小组为验证卤素单质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。实验过程:Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。Ⅳ.……(1)盛放浓盐酸的仪器名称为__________。分液漏斗(2)在烧瓶内发生反应时,体现浓盐酸的性质为______________。(3)验证氯气的氧化性强于碘的实验现象是______________________。(4)B中溶液发生反应的离子方程式是________________________。(5)浸有NaOH溶液的棉花的作用为_________________________________。(6)为验证溴的氧化性强于碘,过程Ⅳ的操作步骤和现象是________________________________________________________________________________。(7)过程Ⅲ实验的目的是__________________________________________________。还原性和酸性湿润的淀粉KI-试纸变蓝Cl2+2Br-===Br2+2Cl-吸收挥发出来的Cl2,防止污染空气打开活塞b,将少量C中确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰溶液滴入D中,关闭活塞b,取下D振荡,静置后CCl4层变为紫红色解析 盛放浓盐酸的仪器名称为分液漏斗,A中滴加浓盐酸后,发生反应:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,体现浓盐酸的还原性和酸性,生成黄绿色气体Cl2,Cl2与KI反应生成I2和KCl,I2使试纸变蓝色;在B、C中均发生反应:Cl2+2NaBr===2NaCl+Br2,由于B、C中生成了Br2而使溶液变为黄色,打开活塞b,C中生成的Br2在D中发生反应:Br2+2KI===2KBr+I2。实验过程Ⅲ,当B中黄色溶液继续通入过量Cl2时,溶液变为红棕色,以此为对照,说明C中黄色溶液无Cl2,从而排除Cl2对溴置换碘实验的干扰,其中浸有NaOH溶液的棉花用于吸收挥发出来的Cl2,防止污染空气。本课结束
本章核心素养聚焦第四章 物质结构 元素周期律一、宏观辨识与微观探析化学研究的重点是在原子、分子水平上认识物质的结构、组成、性质和变化规律,并据此改造或创造物质。本章是从原子结构的角度认识元素及其物质的性质与变化规律,建立原子结构与元素性质、元素性质与物质性质的关系,会用原子结构的知识解释元素性质及其变化规律,能从元素周期表的构成、元素周期律的递变认知上,形成“结构决定性质”的观念,从宏观和微观相结合的视角分析与解决实际问题。例1 短周期元素a、b、c、d的原子序数依次增大,a的最外层电子数是电子层数的2倍,b的最外层电子数是电子层数的3倍,a、c的最外层电子数之和为6,d的核外电子数等于b的核外电子数加8。下列叙述错误的是A.a和b可形成气态化合物B.c的原子半径小于d的原子半径C.b和c可以形成化合物D.a和d最高价氧化物的水化物均呈酸性√解析 由题意可知a为碳,b为氧,c为镁,d为硫。C、O可以形成气态化合物CO、CO2等,A项正确;Mg、S同周期,原子半径:Mg>S,B项错误;MgO为化合物,C项正确;C、S的最高价氧化物对应的水化物分别为H2CO3、H2SO4,均呈酸性,D项正确。例2 A、B、C、D是原子序数依次增大的四种短周期元素,在所有物质中,A的单质密度最小,B的一种氧化物是温室气体;A、C组成的化合物常温下为液态,在短周期元素中,D的半径最大,则下列说法错误的是A.原子半径:D>B>CB.元素的非金属性:B>C>AC.A、B、C、D可以形成化合物D.A分别与B、C形成的简单化合物中,A与B形成的简单化合物的熔点低解析 由题意可知,A为氢,B为碳,C为氧,D为钠。原子半径:Na>C>O,A项正确;非金属性:O>C>H,B项错误;四种元素可形成化合物NaHCO3,C项正确;CH4和H2O相比,CH4为气体,熔点低,D项正确。√例3 短周期元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知Y、W的原子序数之和是Z的3倍,下列说法正确的是A.原子半径:X<Y<ZB.气态氢化物的稳定性:X>ZC.Z、W均可与Mg形成化合物D.最高价氧化物对应水化物的酸性:Y>W√解析 由题意可知,X为硅,Y为氮,Z为氧,W为氯。Si为第三周期元素,N、O为第二周期元素,原子半径:r(Si)>r(N)>r(O),A项错误;非金属性:O>Si,则气态氢化物的稳定性:H2O>SiH4,B项错误;O、Cl可与Mg形成MgO、MgCl2,均为化合物,C项正确;N、Cl最高价氧化物对应的水化物分别为HNO3和HClO4,酸性:HClO4>HNO3,D项错误。思维启迪(1)例1依据原子结构特点推断元素,例2依据元素及其化合物的性质推断元素,例3依据元素周期表的“片段结构”推断元素。解题的思路是:(2)解题的关键是熟知“位—构—性”之间的关系,并将周期表、原子的电子层结构、元素单质及其化合物的性质等内容结合起来进行综合运用,才能推断出相关元素的名称并熟悉它们所形成的单质及其化合物的化学性质,得出正确结论。 二、证据推理与模型认知“证据推理与模型认知”在本章的具体体现:利用元素在元素周期表中的位置和原子结构分析、预测、比较元素及其化合物的性质,能用原子结构解释元素性质及其变化规律,并能结合实验及事实进行说明。在此基础上,建立相关知识应用的思维方法模型,如10电子、18电子微粒的识别与判断,微粒半径大小比较,元素金属性、非金属性强弱比较,元素“位—构—性”关系的应用、化学键类型的判断等。例4 下列关于微粒半径大小的叙述中不正确的是A.同一元素的不同粒子,核外电子数越多,半径越大B.同一元素形成的多种价态的离子,价态越低,半径越小C.同一元素的原子半径小于相应的阴离子半径D.同一元素的原子半径大于相应的阳离子半径√解析 同一元素的原子半径小于相应阴离子的半径,大于相应阳离子的半径,即同一元素粒子的核外电子数越多,其半径越大;同一元素形成的多种价态的离子,价态越低,半径越大。例5 已知同周期X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是HZO4>H2YO4>H3XO4,下列判断正确的是A.原子半径按X、Y、Z的顺序逐渐减小B.单质的氧化性按X、Y、Z的顺序减弱C.三种元素阴离子的还原性按X、Y、Z的顺序增强D.气态氢化物的稳定性按X、Y、Z的顺序减弱√解析 同周期X、Y、Z三种元素的最高价氧化物的水化物的酸性由强到弱的顺序是HZO4>H2YO4>H3XO4,可知X、Y、Z的原子序数为X<Y<Z。同周期元素从左到右单质的氧化性逐渐增强,阴离子的还原性逐渐减弱,原子半径逐渐减小,气态氢化物的稳定性逐渐增强,可知正确选项为A。例6 现有部分短周期元素的性质或结构如下表:(1)X的原子结构示意图________。解析 由表中信息推断出X为S,Y为Cl,Z为I,则根据元素非金属性强弱判断的依据和同主族元素非金属性的递变规律可解答本题。(2)Z在元素周期表中的位置________________。(3)判断非金属性:X____Y(填“>”“<”或“=”,下同)。(4)判断非金属性:Y____Z,写出结构上的原因____________________________________________________________________。第五周期ⅦA族<>二者最外层电子数相同,但I的电子层数多,原子半径大,得电子能力弱思维启迪通过构建“位—构—性”关系认知模型,发展对元素化合物化学性质的认知模型;从“物质类别——一般性质——氧化性和还原性”二维模型发展到“物质类别——一般性质——氧化性和还原性——相似性和递变性”三维模型。三、科学探究与创新意识“科学探究与创新意识”在本章的体现:根据元素周期表和元素周期律研究发现新元素并预测其性质,体会元素周期表和元素周期律在学习元素化合物知识与科学研究中的重要作用。设计实验探究同主族元素(碱金属元素、卤族元素)性质的相似性和递变性,设计实验并结合化学事实探究同周期(第三周期)元素性质递变规律。在探究过程中,运用科学的方法通过观察实验,收集、记录实验现象和数据,分析总结实验结论,并敢于质疑,勇于创新。例7 某校化学学习小组分别设计了一组实验来探究元素周期律。第一小组根据元素非金属性与其对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成同主族元素非金属性强弱比较的实验探究。[查阅资料]Ⅰ.常温下浓盐酸与高锰酸钾能反应生成氯气。Ⅱ.H2SiO3难溶于水。实验药品:大理石、碳酸钠粉末、稀硝酸、硅酸钠溶液。[探究过程](1)第一小组为比较N、C、Si的非金属性强弱,以图1装置进行实验:①烧杯C中现象为__________________,发生反应的离子方程式为__________________________________。②实验预期结论:_________________。③存在问题:__________________________________________________。溶液变浑浊非金属性:C>Si稀硝酸有一定的挥发性,影响C和Si非金属性强弱的判断解析 验证元素的非金属性与其对应最高价含氧酸之间的关系,可根据强酸制弱酸的反应原理,用稀硝酸与大理石反应生成二氧化碳,再将二氧化碳通入硅酸钠溶液中,生成硅酸沉淀。由此可说明硝酸、碳酸及硅酸酸性的强弱,但硝酸有挥发性,影响了最后结果的判断。(2)第二小组设计了如图2装置来验证卤素单质的氧化性,A、B、C三处分别是蘸有溴化钠溶液的棉花、湿润的淀粉碘化钾试纸、湿润的红色纸条。①写出A处反应的离子方程式:_______________________。②B处实验现象是__________。③实验预期结论:______________________。④存在问题:________________________。Cl2+2Br-===Br2+2Cl-试纸变蓝氧化性:Cl2>Br2>I2无法判断Br2和I2的氧化性解析 氯气能与溴化钠溶液发生置换反应,生成单质溴和氯化钠;氯气能与碘化钾溶液发生置换反应,生成单质碘,碘遇淀粉变蓝色;但无法判断Br2和I2的氧化性。例8 某化学课外兴趣小组为验证卤素单质氧化性的相对强弱,用如图所示装置进行实验(夹持仪器已略去,气密性已检验)。实验过程:Ⅰ.打开弹簧夹,打开活塞a,滴加浓盐酸。Ⅱ.当B和C中的溶液都变为黄色时,夹紧弹簧夹。Ⅲ.当B中溶液由黄色变为红棕色时,关闭活塞a。Ⅳ.……(1)盛放浓盐酸的仪器名称为__________。分液漏斗(2)在烧瓶内发生反应时,体现浓盐酸的性质为______________。(3)验证氯气的氧化性强于碘的实验现象是______________________。(4)B中溶液发生反应的离子方程式是________________________。(5)浸有NaOH溶液的棉花的作用为_________________________________。(6)为验证溴的氧化性强于碘,过程Ⅳ的操作步骤和现象是________________________________________________________________________________。(7)过程Ⅲ实验的目的是__________________________________________________。还原性和酸性湿润的淀粉KI-试纸变蓝Cl2+2Br-===Br2+2Cl-吸收挥发出来的Cl2,防止污染空气打开活塞b,将少量C中确认C的黄色溶液中无Cl2,排除Cl2对溴置换碘实验的干扰溶液滴入D中,关闭活塞b,取下D振荡,静置后CCl4层变为紫红色解析 盛放浓盐酸的仪器名称为分液漏斗,A中滴加浓盐酸后,发生反应:2KMnO4+16HCl(浓)===2KCl+2MnCl2+5Cl2↑+8H2O,体现浓盐酸的还原性和酸性,生成黄绿色气体Cl2,Cl2与KI反应生成I2和KCl,I2使试纸变蓝色;在B、C中均发生反应:Cl2+2NaBr===2NaCl+Br2,由于B、C中生成了Br2而使溶液变为黄色,打开活塞b,C中生成的Br2在D中发生反应:Br2+2KI===2KBr+I2。实验过程Ⅲ,当B中黄色溶液继续通入过量Cl2时,溶液变为红棕色,以此为对照,说明C中黄色溶液无Cl2,从而排除Cl2对溴置换碘实验的干扰,其中浸有NaOH溶液的棉花用于吸收挥发出来的Cl2,防止污染空气。本课结束
相关资料
更多









