


高中化学苏教版必修二第三单元 化学能与电能的转化图文课件ppt
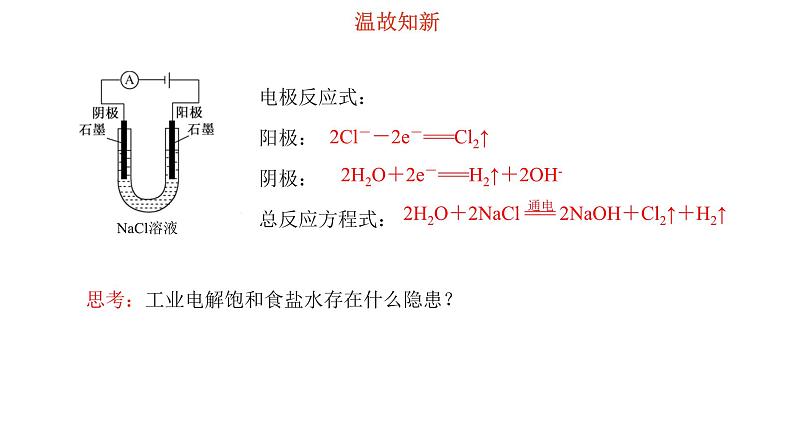
展开电极反应式:阳极: 阴极: 总反应方程式:
2H2O+2e-===H2↑+2OH-
2Cl--2e-===Cl2↑
思考:工业电解饱和食盐水存在什么隐患?
(2)避免生成物H2和Cl2混合,混合后遇火或遇强光爆炸。
(1)避免Cl2接触NaOH溶液发生反应,使产品不纯。反应方程式: 。
Cl2+2NaOH === NaCl+NaClO+H2O
解决方法:使用离子交换膜。
电解饱和食盐水必须解决两个主要问题:
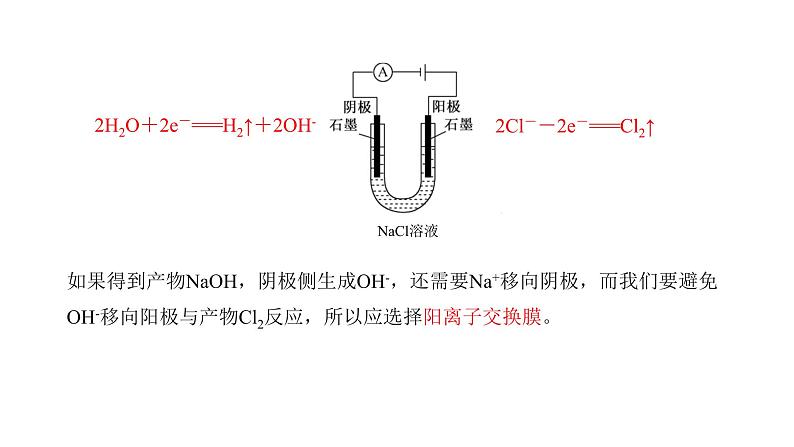
如果得到产物NaOH,阴极侧生成OH-,还需要Na+移向阴极,而我们要避免OH-移向阳极与产物Cl2反应,所以应选择阳离子交换膜。
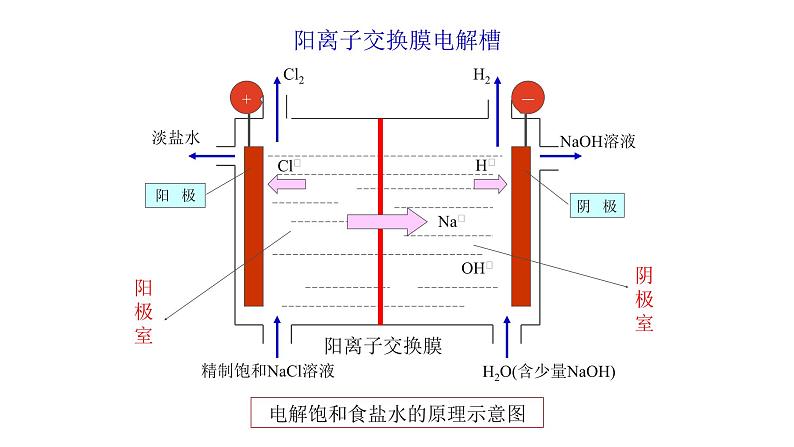
H2O(含少量NaOH)
电解饱和食盐水的原理示意图
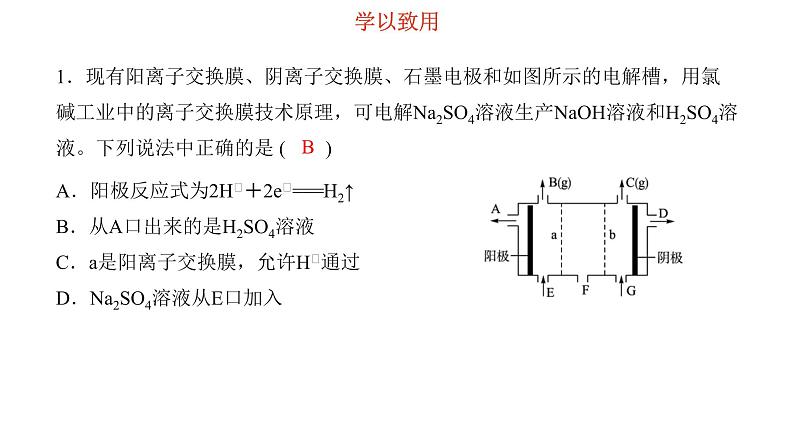
1.现有阳离子交换膜、阴离子交换膜、石墨电极和如图所示的电解槽,用氯碱工业中的离子交换膜技术原理,可电解Na2SO4溶液生产NaOH溶液和H2SO4溶液。下列说法中正确的是 ( )
A.阳极反应式为2H﹢+2e﹣===H2↑B.从A口出来的是H2SO4溶液C.a是阳离子交换膜,允许H﹢通过D.Na2SO4溶液从E口加入
1.概念应用电解原理在某些金属表面镀上一层其它金属或合金的过程。
2.电镀的目的增强金属抗腐蚀能力,增加美观和硬度。
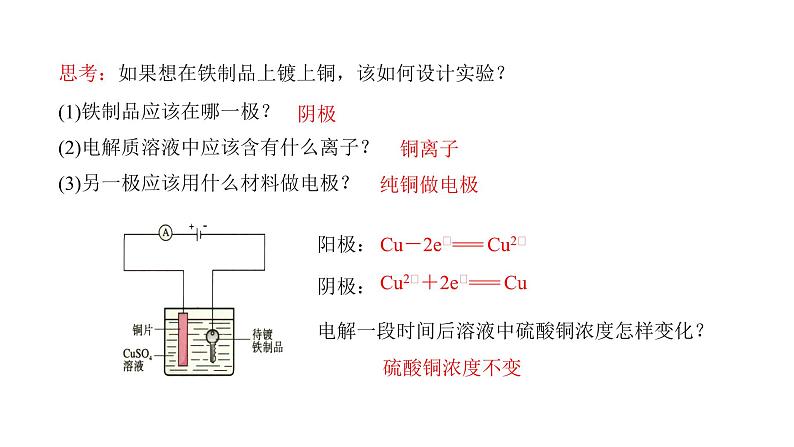
思考:如果想在铁制品上镀上铜,该如何设计实验?
(1)铁制品应该在哪一极?(2)电解质溶液中应该含有什么离子?(3)另一极应该用什么材料做电极?
Cu2﹢+2e﹣=== Cu
Cu-2e﹣=== Cu2﹢
电解一段时间后溶液中硫酸铜浓度怎样变化?
(1)阴极——待镀金属
(2)阳极——镀层金属
(3)电解液——含镀层金属阳离子的盐溶液
电镀液的组成及酸碱性保持不变
Zn、Fe、Ni、Ag、Au等
阳极——粗铜阴极——纯铜电解液——CuSO4溶液
Zn-2e﹣===Zn2﹢
Fe -2e﹣=== Fe2﹢
Ni-2e﹣=== Ni2﹢
Cu -2e﹣=== Cu2﹢
思考:精炼铜时,电解液中的Cu2+浓度是否会发生改变?
用电解精炼法所得到的铜叫做电解铜,它的纯度很高,可以达到99.95%~99.98%。
阴极:Cu2﹢+2e﹣=== Cu
应用电解原理在某些金属表面镀上一层其它金属的装置。
①镀层金属接电源正极,待镀金属接电源负极②电镀液须含有镀层金属的离子
阳极:镀层金属阴极:镀件
应用电解原理将不纯的金属提纯的装置。
①不纯金属接电源正极纯的金属接电源负极②电解质溶液须待提纯金属的离子
阳极:不纯金属阴极:纯金属
电解精炼池、电镀池的比较
(冶炼活泼金属钠、钾、钙、镁、铝等)
电解熔融状态的氯化钠。
2Cl﹣-2e﹣=== Cl2↑
2Na﹢+2e﹣=== 2Na
电解熔融状态的氧化铝。
6O2﹣-12e﹣=== 3O2↑
4Al3﹢+12e﹣=== 4Al
助熔剂:冰晶石(Na3AlF6 六氟合铝酸钠)阳极材料(碳)和熔融氧化铝需要定期补充。
如图所示,甲烧杯中盛有100 mL 0.50 ml·L-1 AgNO3溶液,乙烧杯中盛有100 mL 0.25 ml·L-1 CuCl2溶液,A、B、C、D均为质量相同的石墨电极,如果电解一段时间后,发现A极比C极重1.9 g,回答下列问题:
(1)电源E为____极,F为____极。(2)A极的电极反应式为______________________,析出物质________ml。
Ag﹢+e﹣=== Ag
电极 A B C D产物 Ag O2 Cu Cl2物质的量之比 4 1 2 2
(3)B极的电极反应式为______________________,析出气体_______mL(标准状况)。(4)C极的电极反应式为______________________,析出物质________ml。
2H2O-4e﹣=== 4H﹢+O2↑
高中化学苏教版必修二专题2 化学反应与能量转化第三单元 化学能与电能的转化授课课件ppt: 这是一份高中化学苏教版必修二<a href="/hx/tb_c22590_t3/?tag_id=26" target="_blank">专题2 化学反应与能量转化第三单元 化学能与电能的转化授课课件ppt</a>,共21页。PPT课件主要包含了了解原电池的工作原理,教学目标,电解池,电解原理,交流讨论,原理示意图,电解原理的应用等内容,欢迎下载使用。
苏教版选修4 化学反应原理专题一 化学反应与能量变化第三单元 金属的腐蚀与防护评课ppt课件: 这是一份苏教版选修4 化学反应原理<a href="/hx/tb_c22677_t3/?tag_id=26" target="_blank">专题一 化学反应与能量变化第三单元 金属的腐蚀与防护评课ppt课件</a>,共40页。PPT课件主要包含了化学腐蚀,金属的腐蚀,2原理,1定义,3影响因素,家用燃气灶,电化学腐蚀,科学探究,不同条件下铁钉的腐蚀,水膜呈弱酸性或中性等内容,欢迎下载使用。
苏教版必修二专题2 化学反应与能量转化第三单元 化学能与电能的转化教案配套ppt课件: 这是一份苏教版必修二<a href="/hx/tb_c22590_t3/?tag_id=26" target="_blank">专题2 化学反应与能量转化第三单元 化学能与电能的转化教案配套ppt课件</a>,共25页。PPT课件主要包含了温故知新,OH-,Cl2↑,H2↑,交流讨论,混合遇火或遇强光爆炸,总结归纳,氯碱工业,反应原理,Cl2等内容,欢迎下载使用。













