

还剩7页未读,
继续阅读
苏教版高中化学必修第一册专题3从海水中获得的化学物质练习含答案
展开
这是一份苏教版高中化学必修第一册专题3从海水中获得的化学物质练习含答案,共10页。
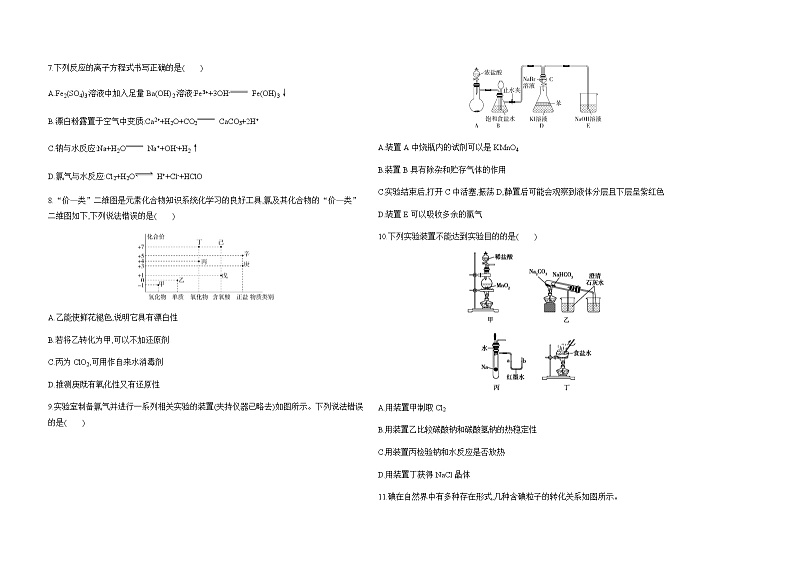
专题3 从海水中获得的化学物质一、选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)1.“84”消毒液(有效成分是NaClO)是大规模环境消毒剂。下列说法不正确的是( )A.用pH试纸检验该溶液,试纸变蓝B.“洁厕灵”与“84”消毒液混用容易造成氯气中毒C.用“84”消毒液喷洒衣物可能会造成脱色D.该溶液具有强氧化性,故可用于杀菌消毒2.碳酸钠粉末遇水生成含有结晶水的碳酸钠晶体——Na2CO3·10H2O,则下列有关说法错误的是( )A.属于纯净物B.Na2CO3·10H2O的化学名称为十水碳酸钠C.在干燥空气中逐渐失去结晶水变成碳酸钠粉末D.其中氧元素的质量分数约为45%3.下列物质的性质与用途具有对应关系的是( )A.Na具有还原性,可用于制作高压钠灯B.NaClO具有强氧化性,可用于消毒杀菌C.Cl2有毒,可用于消毒杀菌D.Na2CO3能沉淀Ca2+,可用于去除物品表面油污4.对陈述Ⅰ、Ⅱ及两者间是否具有因果关系的判断都正确的是( )5.某同学设计了一种制备精盐的实验方案,流程如图,下列说法正确的是( )粗盐滤液精盐A.操作A是溶解,操作C是过滤B.第①⑤⑦步操作都用到了一种相同的玻璃仪器C.第④步只发生反应Ca2++CO32- CaCO3↓D.第⑥步可以调至第④步和第⑤步之间6.下列离子组在指定溶液中能大量共存的是( )A.无色透明的溶液中:K+、Fe3+、SO42-、NO3-B.碱性溶液中:Na+、K+、SO42-、CO32-C.含有大量CuCl2的溶液中:Na+、NH4+、SO42-、OH-D.使紫色石蕊试液呈红色的溶液中:Ca2+、K+、CO32-、NO3-7.下列反应的离子方程式书写正确的是( )A.Fe2(SO4)3溶液中加入足量Ba(OH)2溶液:Fe3++3OH- Fe(OH)3↓B.漂白粉露置于空气中变质:Ca2++H2O+CO2 CaCO3+2H+C.钠与水反应:Na+H2O Na++OH-+H2↑D.氯气与水反应:Cl2+H2O H++Cl-+HClO8.“价—类”二维图是元素化合物知识系统化学习的良好工具,氯及其化合物的“价—类”二维图如下,下列说法错误的是( )A.乙能使鲜花褪色,说明它具有漂白性B.若将乙转化为甲,可以不加还原剂C.丙为ClO2,可用作自来水消毒剂D.推测庚既有氧化性又有还原性9.实验室制备氯气并进行一系列相关实验的装置(夹持仪器已略去)如图所示。下列说法错误的是( )A.装置A中烧瓶内的试剂可以是KMnO4B.装置B具有除杂和贮存气体的作用C.实验结束后,打开C中活塞,振荡D,静置后可能会观察到液体分层且下层呈紫红色D.装置E可以吸收多余的氯气10.下列实验装置不能达到实验目的的是( ) A.用装置甲制取Cl2B.用装置乙比较碳酸钠和碳酸氢钠的热稳定性C.用装置丙检验钠和水反应是否放热D.用装置丁获得NaCl晶体11.碘在自然界中有多种存在形式,几种含碘粒子的转化关系如图所示。I- 单质X IO3-以下说法不正确的是( )A.①反应是2I-+Cl2 I2+2Cl-B.I-与过量Cl2发生的反应是I-+3Cl2+3H2O IO3-+6Cl-+6H+C.①②反应中,氯气都体现还原性,具体表现为氯元素由0价降低为-1价D.通过以上信息可预测:若在加入淀粉的KI溶液中逐滴滴加新制氯水,能观察到溶液变蓝的现象12.Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料:Cl2氧化能力略强于H2O2。为了检验Cl2能否将H2O2氧化,某学生设计了如图所示的实验装置(加热和夹持装置略去)。将浓盐酸注入圆底烧瓶中,反应一段时间后关闭止水夹,试管D中液面下降,长颈漏斗中液面上升,试管D中的气体无色,经检验该气体能使带火星的木条复燃。除反应H2O2+Cl2 2HCl+O2可能发生外,对试管D中气体来源的判断最不可能的是( )A.C中HClO分解产生的氧气B.C中H2O2分解产生的氧气C.D中NaClO分解产生的氧气D.C中生成的氧气和少量没有排净的空气13.ClO2是一种广谱消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为自来水的消毒剂。工业制备ClO2的方法有多种,用NaClO3和H2C2O4(草酸)的混合溶液加硫酸酸化可制取ClO2,该反应中还原剂和氧化剂的物质的量之比是( )A.1∶1 B.2∶1 C.1∶2 D.2∶314.以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的步骤如下:步骤1:将电石渣与水混合,形成浆料。步骤2:控制电石渣过量,75 ℃时向浆料中通入Cl2,该过程会生成Ca(ClO)2,Ca(ClO)2会进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2,一段时间后过滤。步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25 ℃结晶,得KClO3。下列说法正确的是( )A.控制通入Cl2的速率,可以提高Cl2的利用率B.25 ℃时,Ca(ClO3)2的溶解能力比KClO3小C.步骤2中,过滤所得滤液中n(CaCl2)n[Ca(ClO3)2]=51D.生成Ca(ClO)2的化学方程式为Cl2+Ca(OH)2 Ca(ClO)2+H215.向NaOH和Na2CO3的混合溶液中滴加0.1 mol/L的盐酸,生成CO2的物质的量与加入盐酸的体积的关系如图所示。下列叙述不正确的是( )A.051,C错误;氯气与Ca(OH)2反应的化学方程式为2Cl2+2Ca(OH)2 CaCl2+Ca(ClO)2+2H2O,D错误。15.D 结合氢离子的能力:OH->CO32->HCO3-,向NaOH和Na2CO3的混合溶液中滴加0.1 mol/L的盐酸,依次发生反应的离子方程式:①OH-+H+ H2O、②CO32-+H+ HCO3-、③HCO3-+H+ H2O+CO2↑。根据图像可知,发生反应③生成0.01 mol二氧化碳,则反应③消耗盐酸的体积是0.1 L,所以发生反应②消耗盐酸的体积也是0.1 L,发生反应①消耗0.2 L盐酸,则a=0.3。0
专题3 从海水中获得的化学物质一、选择题(本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的)1.“84”消毒液(有效成分是NaClO)是大规模环境消毒剂。下列说法不正确的是( )A.用pH试纸检验该溶液,试纸变蓝B.“洁厕灵”与“84”消毒液混用容易造成氯气中毒C.用“84”消毒液喷洒衣物可能会造成脱色D.该溶液具有强氧化性,故可用于杀菌消毒2.碳酸钠粉末遇水生成含有结晶水的碳酸钠晶体——Na2CO3·10H2O,则下列有关说法错误的是( )A.属于纯净物B.Na2CO3·10H2O的化学名称为十水碳酸钠C.在干燥空气中逐渐失去结晶水变成碳酸钠粉末D.其中氧元素的质量分数约为45%3.下列物质的性质与用途具有对应关系的是( )A.Na具有还原性,可用于制作高压钠灯B.NaClO具有强氧化性,可用于消毒杀菌C.Cl2有毒,可用于消毒杀菌D.Na2CO3能沉淀Ca2+,可用于去除物品表面油污4.对陈述Ⅰ、Ⅱ及两者间是否具有因果关系的判断都正确的是( )5.某同学设计了一种制备精盐的实验方案,流程如图,下列说法正确的是( )粗盐滤液精盐A.操作A是溶解,操作C是过滤B.第①⑤⑦步操作都用到了一种相同的玻璃仪器C.第④步只发生反应Ca2++CO32- CaCO3↓D.第⑥步可以调至第④步和第⑤步之间6.下列离子组在指定溶液中能大量共存的是( )A.无色透明的溶液中:K+、Fe3+、SO42-、NO3-B.碱性溶液中:Na+、K+、SO42-、CO32-C.含有大量CuCl2的溶液中:Na+、NH4+、SO42-、OH-D.使紫色石蕊试液呈红色的溶液中:Ca2+、K+、CO32-、NO3-7.下列反应的离子方程式书写正确的是( )A.Fe2(SO4)3溶液中加入足量Ba(OH)2溶液:Fe3++3OH- Fe(OH)3↓B.漂白粉露置于空气中变质:Ca2++H2O+CO2 CaCO3+2H+C.钠与水反应:Na+H2O Na++OH-+H2↑D.氯气与水反应:Cl2+H2O H++Cl-+HClO8.“价—类”二维图是元素化合物知识系统化学习的良好工具,氯及其化合物的“价—类”二维图如下,下列说法错误的是( )A.乙能使鲜花褪色,说明它具有漂白性B.若将乙转化为甲,可以不加还原剂C.丙为ClO2,可用作自来水消毒剂D.推测庚既有氧化性又有还原性9.实验室制备氯气并进行一系列相关实验的装置(夹持仪器已略去)如图所示。下列说法错误的是( )A.装置A中烧瓶内的试剂可以是KMnO4B.装置B具有除杂和贮存气体的作用C.实验结束后,打开C中活塞,振荡D,静置后可能会观察到液体分层且下层呈紫红色D.装置E可以吸收多余的氯气10.下列实验装置不能达到实验目的的是( ) A.用装置甲制取Cl2B.用装置乙比较碳酸钠和碳酸氢钠的热稳定性C.用装置丙检验钠和水反应是否放热D.用装置丁获得NaCl晶体11.碘在自然界中有多种存在形式,几种含碘粒子的转化关系如图所示。I- 单质X IO3-以下说法不正确的是( )A.①反应是2I-+Cl2 I2+2Cl-B.I-与过量Cl2发生的反应是I-+3Cl2+3H2O IO3-+6Cl-+6H+C.①②反应中,氯气都体现还原性,具体表现为氯元素由0价降低为-1价D.通过以上信息可预测:若在加入淀粉的KI溶液中逐滴滴加新制氯水,能观察到溶液变蓝的现象12.Cl2和H2O2是高中阶段最常见的两种氧化剂,经查阅资料:Cl2氧化能力略强于H2O2。为了检验Cl2能否将H2O2氧化,某学生设计了如图所示的实验装置(加热和夹持装置略去)。将浓盐酸注入圆底烧瓶中,反应一段时间后关闭止水夹,试管D中液面下降,长颈漏斗中液面上升,试管D中的气体无色,经检验该气体能使带火星的木条复燃。除反应H2O2+Cl2 2HCl+O2可能发生外,对试管D中气体来源的判断最不可能的是( )A.C中HClO分解产生的氧气B.C中H2O2分解产生的氧气C.D中NaClO分解产生的氧气D.C中生成的氧气和少量没有排净的空气13.ClO2是一种广谱消毒剂,根据世界环保联盟的要求,ClO2将逐渐取代Cl2成为自来水的消毒剂。工业制备ClO2的方法有多种,用NaClO3和H2C2O4(草酸)的混合溶液加硫酸酸化可制取ClO2,该反应中还原剂和氧化剂的物质的量之比是( )A.1∶1 B.2∶1 C.1∶2 D.2∶314.以电石渣[主要成分为Ca(OH)2和CaCO3]为原料制备KClO3的步骤如下:步骤1:将电石渣与水混合,形成浆料。步骤2:控制电石渣过量,75 ℃时向浆料中通入Cl2,该过程会生成Ca(ClO)2,Ca(ClO)2会进一步转化为Ca(ClO3)2,少量Ca(ClO)2分解为CaCl2和O2,一段时间后过滤。步骤3:向滤液中加入稍过量KCl固体,蒸发浓缩、冷却至25 ℃结晶,得KClO3。下列说法正确的是( )A.控制通入Cl2的速率,可以提高Cl2的利用率B.25 ℃时,Ca(ClO3)2的溶解能力比KClO3小C.步骤2中,过滤所得滤液中n(CaCl2)n[Ca(ClO3)2]=51D.生成Ca(ClO)2的化学方程式为Cl2+Ca(OH)2 Ca(ClO)2+H215.向NaOH和Na2CO3的混合溶液中滴加0.1 mol/L的盐酸,生成CO2的物质的量与加入盐酸的体积的关系如图所示。下列叙述不正确的是( )A.0
相关资料
更多









