




初中化学科粤版(2024)九年级下册7.3 溶液浓稀的表示图文课件ppt
展开
这是一份初中化学科粤版(2024)九年级下册7.3 溶液浓稀的表示图文课件ppt,共32页。PPT课件主要包含了加速溶解等内容,欢迎下载使用。
1.知道溶质质量分数可以表示浓度;能从定量的视角,说明溶质质量分数的含义。2.能进行溶质质量分数的简单计算。3.能根据需要配制一定溶质质量分数的溶液。4.理解溶解度与溶质质量分数的区别与联系。
1.溶液浓稀的判断(1)溶液颜色的深浅可以通过颜色的深浅粗略判断有色溶液(如硫酸铜溶液)的浓稀程度。比如不同浓度的硫酸铜溶液,颜色越深则浓度越大。(2)浓度想要准确地判断有色或无色溶液的浓稀,就涉及溶液浓稀的定量表示,即浓度的问题。在溶液中,浓度是指一定量的溶液中所含溶质的量。
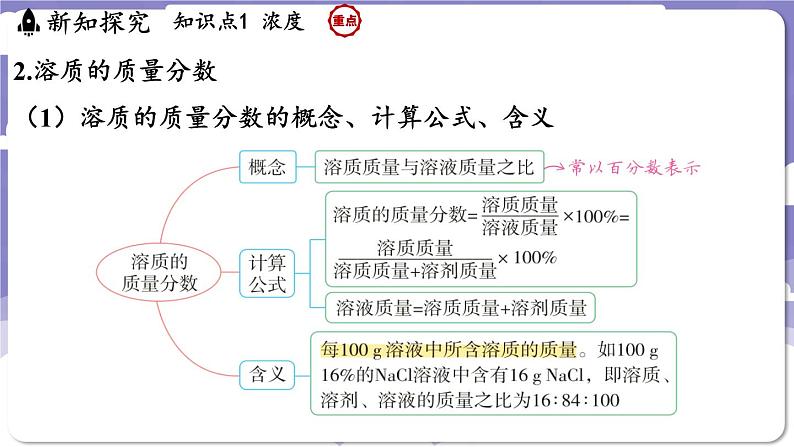
2.溶质的质量分数(1)溶质的质量分数的概念、计算公式、含义
特别提醒对溶液中溶质的质量分数的理解1.溶液具有均一性,故溶液中各部分溶质的质量分数都相等;溶液具有稳定性,一瓶溶液长期放置,只要外界条件不变,其溶质的质量分数不变。2.运用溶质的质量分数表示溶液浓度时,必须分清溶质质量、溶剂质量与溶液质量。
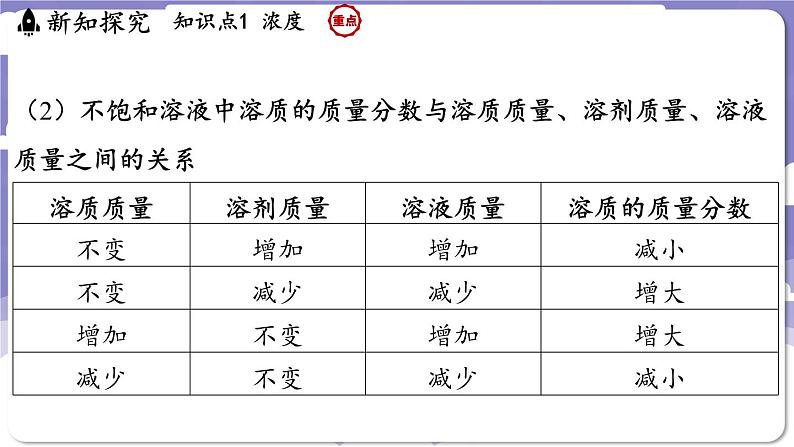
(2)不饱和溶液中溶质的质量分数与溶质质量、溶剂质量、溶液质量之间的关系
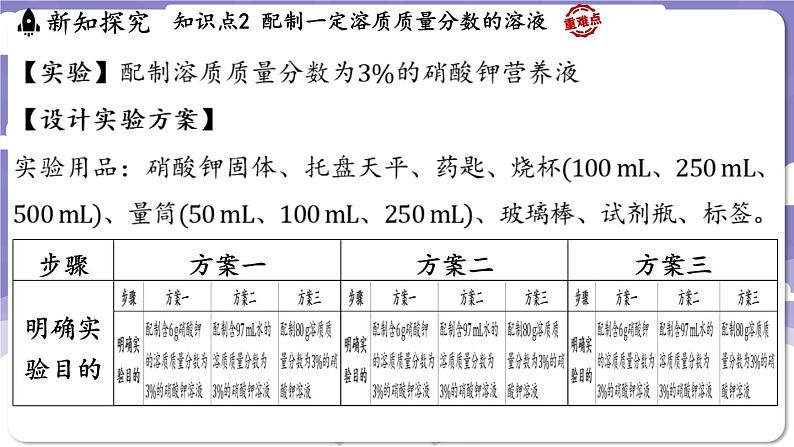
根据实际需要并考虑到方便课堂小组配制溶液,选择方案二进行实施。
(2)液体量取操作要点:视线要与量筒内液体凹液面的最低处保持水平。(3)倾倒操作要点:将量筒中的水沿烧杯壁倒入烧杯中,切勿洒出。(4)搅拌操作要点:搅拌时玻璃棒不要碰烧杯壁和烧杯底。
1. 溶液稀释和增浓(无溶质析出)的计算
向溶液中加水,即稀释溶液,所得溶液的溶质质量分数减小,B错误。
2.溶质的质量分数与化学方程式的综合计算(1)在溶液中发生化学反应时,参加反应的一般是溶液中的溶质。所以利用化学方程式列有关反应物、生成物的质量比时,要以溶质的质量列比例,而不能用溶液的质量列比例。
(2)该稀硫酸中溶质的质量分数。
相关课件
这是一份初中化学科粤版九年级下册7.3 溶液浓稀的表示评课ppt课件,共58页。PPT课件主要包含了逐点导讲练,课堂小结,作业提升,学习目标,课时讲解,课时流程,课时导入,感悟新知,溶质的质量分数,左物右码等内容,欢迎下载使用。
这是一份科粤版九年级下册7.3 溶液浓稀的表示教课内容ppt课件,共16页。PPT课件主要包含了学习目标,新知学习,操作步骤,溶液中质量分数偏大,量取液体时俯视读数,称量的溶质偏大,溶液中质量分数偏小,物体中有杂质,配制溶液的烧杯中有水,量取液体时仰视读数等内容,欢迎下载使用。
这是一份初中化学科粤版九年级下册7.3 溶液浓稀的表示课文内容课件ppt,共17页。PPT课件主要包含了溶液是浓还是稀,学习目标,新知学习,溶液的溶度,颜色越深浓度越大,溶质的质量分数,2计算公式,比较深,在一定的温度下,不受外界条件的影响等内容,欢迎下载使用。









