

山东省济宁市兖州区第六中学2024-2025学年高三上学期10月月考化学试题
展开
这是一份山东省济宁市兖州区第六中学2024-2025学年高三上学期10月月考化学试题,共6页。试卷主要包含了10),982偏高等内容,欢迎下载使用。
本试卷满分100分,考试时间90分钟。
可能用到的相对原子质量:H 1 C 12 O 16 Na 23 S 32 Cl 35.5
Fe 56 Cu 64
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.汉·陈琳《武军赋》:“铠则东胡阙巩,百炼精钢”。下列说法正确的是( )
A.钢是合金,合金是指含有两种或两种以上金属的混合物
B.炼铁常用的CO可以通过CO2与C高温下反应获得
C.铁比铜活泼,铁的发现、大量冶炼和使用均早于铜
D.铁是比较活泼的金属,自然界中不存在游离态的铁
2.下列关于物质或微粒分类说法正确的是( )
A.含有金属元素的离子不一定是阳离子
B.某物质只含有一种元素,该物质一定是一种纯净物
C.能与酸反应的氧化物,一定是碱性氧化物
D.CO2和NO2均能与H2O反应生成酸,故二者都是酸性氧化物
3.高中生应德智体美劳全面发展。下列劳动项目与所述的化学知识没有关联的是( )
4.CO2低压合成甲醇反应为CO2 + 3H2 = CH3OH + H2O,反应涉及的4种物质沸点最高的是( )
A.CO2B.H2C.CH3OHD.H2O
5.NA为阿伏加德罗常数的值,下列说法正确的是( )
A.Na与H2O反应生成11.2 L H2,转移电子数目为NA
B.1.0 L 1.0 ml·L-1的Na2CO3溶液中CO32-的数目为1.0 NA
C.标准状况下,2.24 LNO和N2O混合气体中氧原子数为0.1NA
D.5.6g铁粉与0.1L 1 ml·L-1的HCl的溶液充分反应,产生的气体分子数目为0.1NA
6.少量Na2O2与H2O反应生成H2O2和NaOH。下列说法正确的是( )
A.Na2O2的电子式为B.H2O的空间构型为直线形
C.H2O2中O元素的化合价为-1D.NaOH仅含离子键
7.在溶液中能大量共存的离子组是( )
A.H+、Fe2+、Ba2+、NO3-B.Fe3+、K+、CN-、Cl-
C.Na+、CO32-、Br-、Ca2+D.NH4+、SO42-、CH3COO-、HCO3-
8.用绿矾(FeSO4·7H2O)将酸性工业废水中的Cr2O72-转化为Cr3+:6Fe2+ + Cr2O72- +14H+ = 6Fe3+ +2Cr3++7H2O。关于该反应的下列说法正确的是( )
A.Cr3+是氧化产物B.Fe2+发生还原反应
C.氧化剂与还原剂的物质的量之比为6∶1
D.生成1ml Cr3+时,转移3ml电子
9.宏观辨识与微观探析是化学学科核心素养之一。下列物质性质实验对应的反应方程式书写正确的是( )
A.SO2通入酸性KMnO4溶液中:5SO2+2H2O+2MnOeq \\al(-,4) = 5SO42-+4H++2Mn2+
B.NaHCO3溶液与NaOH溶液反应:HCO3-+OH- = H2O+CO2↑
C.Na与CuSO4水溶液反应:2Na + Cu2+ = Cu +2Na+
D.铜丝插入热的浓硫酸中:Cu+H2SO4 CuSO4+H2↑
10.下列离子的检验方法合理的是( )
A.向某溶液中滴入KSCN溶液呈红色,说明不含Fe2+
B.向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
C.向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
D.向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.氯化铁溶液腐蚀铜电路板是电子工业中的常见做法。有关该反应描述正确的是( )
A. 该反应生成Fe,属于置换反应 B. 该反应体现了Fe3+的氧化性
C. 每腐蚀1ml Cu,转移2ml e-
D. 改用酸性H2O2溶液腐蚀铜,反应为2Cu + 4H+ + H2O2 = 2Cu2+ + H2↑ + 2H2O
12.超氧化钾(KO2)可用作潜水或宇航装置的CO2吸收剂和供氧剂,反应为4KO2 + 2CO2 = 2K2CO3 + 3O2。下列说法正确的是( )
A.1 ml KO2晶体中离子的物质的量为2 ml B.KO2中K为+4价
C.CO2与Na2O2也能反应,两反应中CO2的作用不同
D.该反应中每转移1 ml电子生成O2 1.5 ml
13.Na可以作强吸水剂。下列有关说法正确的是( )
A.要除去乙醇中少量的水,可以加入金属Na,再过滤
B.Na吸水的原理与NaOH吸水的原理不同
C.Na吸水比CaCl2吸水更安全
D.检验乙醇中是否含有水,可以加入Na,观察现象
14.由下列事实或现象能得出相应结论的是( )
15. 可采用Deacn催化氧化法将工业副产物HCl制成Cl2,实现氯资源的再利用。反应
的化学方程式:4HCl + O2 2Cl2 + 2H2O。下图所示为该方法的一种催化机理。下列
说法正确的是( )
A. Z为O2,W为Cl2 B. 图中转化涉及的反应均为氧化还原反应
C. 制取1mlCl2,须投入2mlCuOD. CuCl2也可以做该反应的催化剂
三、非选择题:本题共5小题,共60分,每空2分。
16.(12分)实验室配制不同pH、一定物质的量浓度的KMnO4溶液,探究它与KI溶液的反应。回答下列问题:
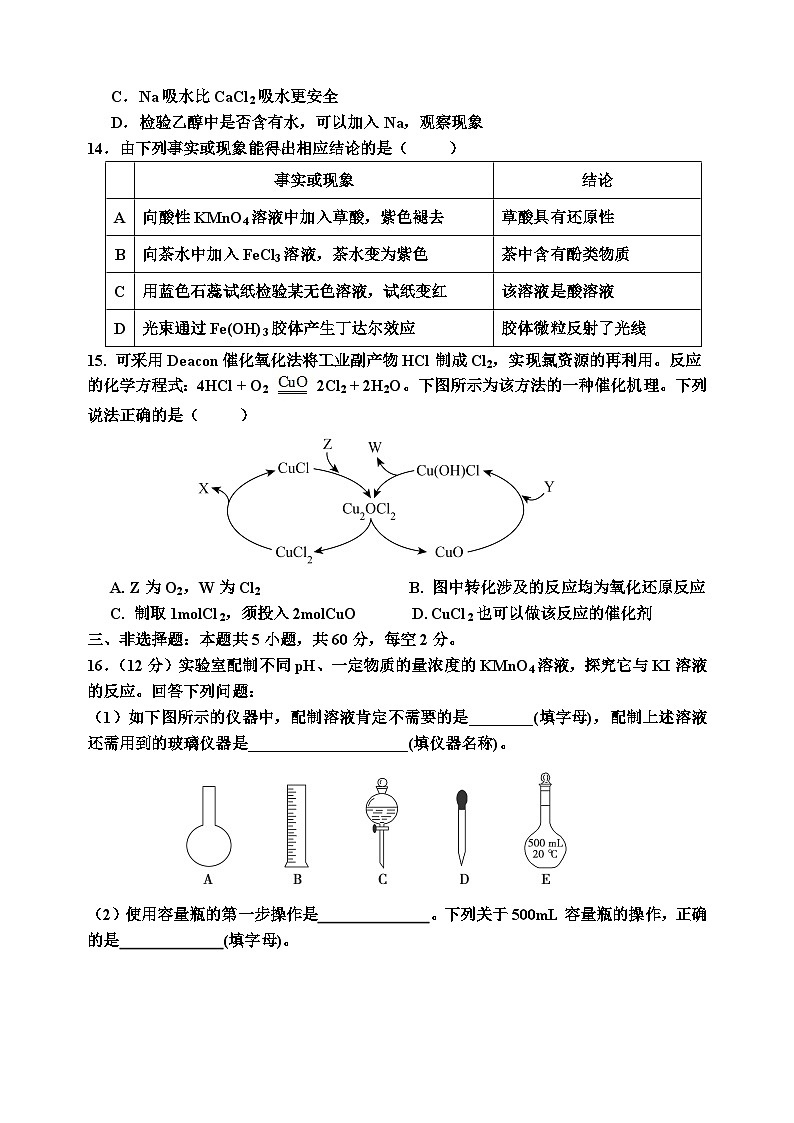
(1)如下图所示的仪器中,配制溶液肯定不需要的是________(填字母),配制上述溶液还需用到的玻璃仪器是____________________(填仪器名称)。
(2)使用容量瓶的第一步操作是 。下列关于500mL容量瓶的操作,正确的是 (填字母)。
(3)酸性KMnO4溶液与KI溶液反应后,向其中加入淀粉溶液,发现溶液变蓝,写出该反应的离子方程式 。
(4)在中性条件下,KMnO4溶液与KI溶液反应后,静置,观察到生成黑色沉淀,上层溶液为无色。查阅资料得知该条件下生成IO3-,则该反应的还原产物为 。
17.(12分)氢氧化亚铁可以用来制颜料、药物、催化剂、吸收剂和砷解毒剂等。设计以下实验探究氢氧化亚铁的制备。
Ⅰ.用FeSO4溶液与不含O2的蒸馏水配制的NaOH溶液反应制备Fe(OH)2。
(1)除去蒸馏水中溶解的O2常采用____________的方法。
(2)生成Fe(OH)2白色沉淀的操作是用长滴管吸取不含O2的NaOH溶液,
插入FeSO4溶液液面下,再挤出NaOH溶液,这样操作的目的是
________________________________;还可以在FeSO4溶液上面加苯等保护
层。如不采取上述措施,会看到白色沉淀 (答现象),反应的化学方程式为 。
Ⅱ.选用稀硫酸、铁粉、NaOH溶液进行实验,装置如图。
(4)实验时,先________(填“打开”或“关闭”,下同)止水
夹K,然后打开分液漏斗的玻璃塞和活塞,使稀硫酸与铁
粉反应,一段时间后,________止水夹K,利用氢气造成
试管内的压强增大,将FeSO4溶液压至NaOH溶液中反
应制得白色Fe(OH)2沉淀,且沉淀能持续一段时间不变色。
18.(12分)侯氏制碱法工艺流程中的主反应为QR + YW3 + XZ2 + W2Z = QWXZ3 + YW4R,其中W、X、Y、Z、Q、R分别代表相关化学元素,且原子序数依次增大。回答下列问题:
(1)上述元素中,电负性最小的是 (填元素符号)。
(2)常温常压下,YW3与XZ2在水中的溶解度更大的是 (填化学式)。
(3)假设起始时,加入的YW3与W2Z原子数相同,则二者的物质的量之比为 。
(4)QW与W2Z反应的化学方程式为 。
(5)称取1.840 g小苏打样品(含少量NaCl),配制成250 mL溶液,取出25.00 mL用0.1000 ml·L-1盐酸滴定,消耗盐酸21.50 mL。
样品中NaHCO3质量分数为_____________________。(保留3位有效数字)
(6)将一定质量小苏打样品(含少量NaCl)溶于足量盐酸,蒸干后称量固体质量,也可测定小苏打的含量。若蒸发过程中有少量液体溅出,则测定结果__________。(选填“偏高”、
“偏低”或“不受影响”)
19.(12分)钧瓷是宋代五大名瓷之一,其中红色钧瓷的发色剂为Cu2O。为探究Cu2O的性质,取等量少许Cu2O分别加入甲、乙、丙、丁、戊五支试管,进行如下实验。已知CuCl为白色沉淀。回答下列问题:
(1)试管甲、丙的反应现象相同,说明其中酸的作用是表现了 ,反应的离子方程式为 。
(2)试管乙中,溶液中反应的离子方程式为 。
(3)对比试管乙、丙中的现象,可以推知6ml·L-1的两种酸中,氧化性较强的是
(填化学式)。
(4)查阅资料,试管丁、戊中分别生成[CuCl2]-、[Cu(NH3)2]+配离子,两种配离子的相同点有 (答出一种即可),不同点有
。
20.(12分)亚氯酸钠(NaClO2)是一种高效的漂白剂和氧化剂,可用于各种纤维和某些食品的漂白。马蒂逊(Mathiesn)法制备亚氯酸钠的流程如下:
回答下列问题:
(1)反应①阶段,参加反应的NaClO3和SO2的物质的量之比为 。
(2)NaHSO4溶于水的电离方程式为 。
(3)酸碱是工业生产的基础原料。根据反应原理和生产实际,下列关于该生产流程中酸
碱使用的说法正确的是 。
A.硫酸可以换为硝酸,氢氧化钠可以换为氢氧化钙
B.硫酸可以换为硝酸,氢氧化钠不能换为氢氧化钙
C.硫酸不能换为硝酸,氢氧化钠可以换为氢氧化钙
D.硫酸不能换为硝酸,氢氧化钠不能换为氢氧化钙
(4)写出反应②的化学方程式 ,该反应条件下,ClO2的氧化性 (填“大于”或“小于”)H2O2。
(5)假设第①阶段生成的ClO2气体在第②阶段完全反应,则两阶段转移电子的物质的量之比为 。
【答案】1B 2A 3C 4D 5C 6C 7D 8D 9A 10B
11BC 12A 13B 14AB 15D
16.(12分)(每空2分)(1)AC 烧杯、玻璃棒(漏1个扣1分)
(2)查漏 C (3)2MnO4- + 16H+ + 10 I- = 2Mn2+ + 5I2 + 8H2O (4)MnO2
17.(12分,每空2分)(1)煮沸 (2)避免生成的Fe(OH)2沉淀接触O2而被氧化
(3)迅速变为灰绿色,最后变成红褐色 4 Fe(OH)2 + O2 + 2H2O = 4Fe(OH)3
(4)打开 关闭
18.(12分)(每空2分)(1)Na (2)NH3 (3)3:4
(4)NaH+H2O=NaOH+H2↑ (5)0.982(或98.2%) (6)偏高
19.(8分)(每空2分)(1)酸性 Cu2O + 2 H+ = Cu2++ Cu +H2O
(2)3Cu2O + 14H+ + 2NO3- = 6Cu2+ + 2NO↑ + 7H2O (3)HNO3
(4)铜均为+1价(或溶液均为无色等,合理均给分) [CuCl2]-稀释后可生成CuCl沉淀,[Cu(NH3)2]+容易被氧化(合理均给分)
20.(12分)(每空2分)(1)2:1 (2)NaHSO4 = Na+ + H+ + SO42- (3)D
(4)2ClO2 + H2O2 + 2NaOH = 2NaClO2 +2H2O + O2 大于 (5)1:1劳动项目
化学知识
A
烹饪活动:向煮沸的豆浆中加入卤水制作豆腐
电解质溶液使胶体聚沉
B
烘焙活动:碳酸氢钠与柠檬酸的混合物用作复合膨松剂
NaHCO3能与酸反应产生气体
C
家务活动:擦干已洗净铁锅表面的水,以防生锈
铁与水蒸气反应生成Fe3O4
D
清洁活动:用过氧碳酸钠漂白衣物
Na2CO4具有较强氧化性
事实或现象
结论
A
向酸性KMnO4溶液中加入草酸,紫色褪去
草酸具有还原性
B
向茶水中加入FeCl3溶液,茶水变为紫色
茶中含有酚类物质
C
用蓝色石蕊试纸检验某无色溶液,试纸变红
该溶液是酸溶液
D
光束通过Fe(OH)3胶体产生丁达尔效应
胶体微粒反射了光线
实验操作及现象
试管甲
滴加过量0.3ml·L-1 HNO3溶液并充分振荡,砖红色沉淀转化为紫红色沉淀,溶液显浅蓝色
试管乙
滴加适量6 ml·L-1 HNO3溶液并充分振荡,沉淀逐渐溶解,溶液显蓝色,试管口有红棕色气体产生
试管丙
滴加适量6ml·L-1H2SO4溶液并充分振荡,砖红色沉淀转化为紫红色沉淀,溶液显蓝色
试管丁
滴加适量12ml·L-1盐酸并充分振荡,沉淀逐渐溶解,溶液颜色为无色;加水稀释,析出白色沉淀
试管戊
滴加过量6 ml·L-1氨水并充分振荡,沉淀逐渐溶解,溶液颜色为无色;静置一段时间后,溶液颜色变为深蓝色
相关试卷
这是一份山东省济宁市兖州区2023-2024学年高一上学期期中考试化学试题,共9页。试卷主要包含了下列物质中含有自由移动的的是,下列说法正确的是,下列离子方程式书写正确的是,下列物质的分类正确的是等内容,欢迎下载使用。
这是一份山东省济宁市兖州区2023-2024学年高三上学期期中考试化学试题,共11页。试卷主要包含了5 Fe 56 Cu 64,反应应用于玻璃雕刻,碳量子点等内容,欢迎下载使用。
这是一份山东省济宁市兖州区2022-2023学年高一下学期4月月考化学试题(Word版含答案),文件包含化学答案docx、化学试题docx等2份试卷配套教学资源,其中试卷共18页, 欢迎下载使用。










