

辽宁省沈阳市第二中学2024-2025学年高二上学期10月阶段测试 化学试题
展开
这是一份辽宁省沈阳市第二中学2024-2025学年高二上学期10月阶段测试 化学试题,共10页。试卷主要包含了考试时长75分钟,满分100分,常温下完成下列实验,部分弱电解质的电离常数如下表等内容,欢迎下载使用。
命题人:高二化学组 审校人:高二化学组
说明:1.考试时长75分钟,满分100分
2.考生务必将答案答在答题卡相应位置上,在试卷上作答无效。
可能用到的相对原子质量
第I卷(45分)
1.下图所示为工业合成氨的流程图。有关说法错误的是
A.步骤①中“净化”可以防止催化剂中毒
B.步骤②中“加压”既可以提高原料的转化率,又可以加快反应速率
C.步骤③、④、⑤均有利于提高原料平衡的转化率
D.产品液氨除可生产化肥外,还可用作制冷剂
2.一定条件下,在容积均为2L的两个恒温恒容密闭容器中加入一定量的一氧化碳和水蒸气,发生反应:
,达平衡后获得数据如下表。下列说法错误的是
A.Q等于65.6
B.反应①比反应②达到平衡时间短
C.①中反应达平衡时,的转化率为
D.该温度下,中反应的平衡常数
3.某温度下,,该温度下的溶液与的溶液按一定比例混合,所得溶液,则溶液与溶液的体积比为
A.B.C.D.
4.在石墨烯负载型单原子催化剂()上还原生成和的路径机理及活化能(kJ/ml)如图所示。下列说法错误的是
A.还原生成过程中,速率最慢的基元反应为
B.上还原,更容易生成
C.根据如图数据可计算的
D.由图可知,相同催化剂条件下反应可能存在多种反应历程
5.下列说法正确的是
A.电离平衡向右移动,弱电解质的电离程度一定增大
B.随着温度的升高,弱电解质溶液和金属的导电能力均增强
C.向溶液中通入直至过量,混合溶液的导电能力增强
D.把醋酸溶液用蒸馏水稀释到,的值减小
6.常温下完成下列实验。其中实验I中浑浊不消失,实验II和实验III中浊液变澄清。下列说法中,不正确的是
A.实验III中加入溶液后,比值增大
B.实验II中加入浓氨水后,
C.实验I中加入8滴水后溶液的不变
D.实验II和实验III中浊液变澄清可能与的电离平衡、水解平衡有关
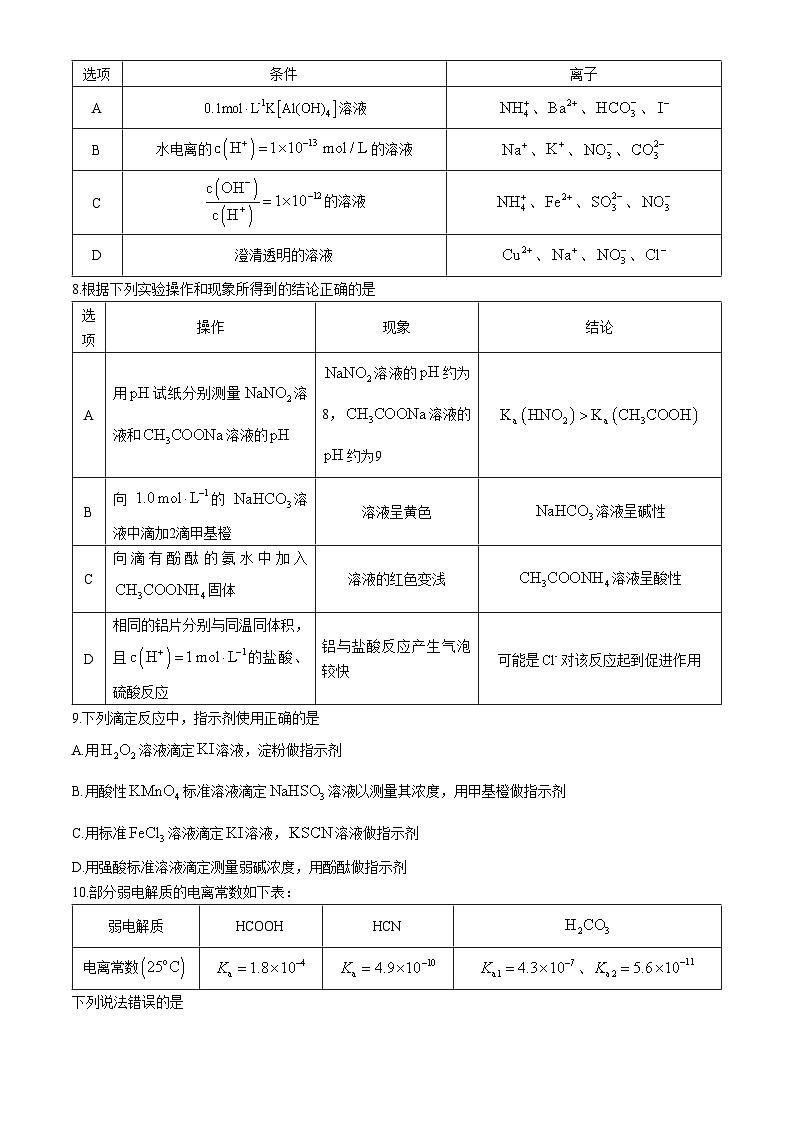
7.常温下,下列各组离子在所限定的条件下一定能大量共存的是
8.根据下列实验操作和现象所得到的结论正确的是
9.下列滴定反应中,指示剂使用正确的是
A.用溶液滴定溶液,淀粉做指示剂
B.用酸性标准溶液滴定溶液以测量其浓度,用甲基橙做指示剂
C.用标准溶液滴定溶液,溶液做指示剂
D.用强酸标准溶液滴定测量弱碱浓度,用酚酞做指示剂
10.部分弱电解质的电离常数如下表:
下列说法错误的是
A.根据电离常数,可判断酸性
B.等体积、等浓度的和溶液中离子总数:前者小于后者
C.向溶液中通入少量,离子方程式为:
D.时,反应的化学平衡常数为
11.下列装置正确且进行实验可以达到相应实验目的的是
12.是一种易溶的碱,与足量盐酸反应生成。常温下,将稀释体积为,与的关系如图所示。下列说法正确的是
A.将的溶液稀释至,溶液
B.是弱碱,电离常数
C.溶液稀释过程中,和均逐渐增大
D.溶液中存在
13.已知:。一定条件下与反应的图像如图。30min、40min时分别只改变一个条件。下列说法正确的是( )
A.时,可以是降低体系压强或加入催化剂
B.时,增加或的浓度
C.平衡常数:
D.转化率:
14.常温下,用标准溶液滴定三元酸(的第一步电离方程式为),测得溶液的与氢氧化钠溶液体积的关系如图所示,下列说法正确的是
A.滴定过程中可用石蕊作指示剂
B.a点满足:
C.点满足:
D.随着氢氧化钠溶液的不断加入,水的电离程度不断增大
15.常温下,向新制氯水中滴加溶液,溶液中水电离出的浓度与溶液体积之间的关系如图所示。下列推断正确的是
A.、点溶液的分别为3和7
B.点对应的溶液中:
C.点对应的溶液中:
D.点对应的溶液中,
第II卷(55分)
16.(16分)下列物质在工业生产中有着广泛的应用
(1)和在加热的条件下可以获得无水,该反应的化学反应方程式为_______________。
(已知该反应为非氧化还原反应)
(2)配制溶液时,应该先将溶于________(填名称),然后加水稀释到所需的浓度。
(3)为探究水解的影响因素,学习小组用传感器采集以下溶液的:
对照溶液的配制方法如下:在溶液中滴加盐酸,使其与溶液一致,得溶液,将溶液稀释10倍,得溶液。
实验②和③是为了探究_____________对水解的影响,根据表格数据_______c(填“>”或“ (2)减小 (3)A
(4) (5)CD
19(15分)(1) 丙烷直接脱氢反应的正反应是一个吸热反应,升高温度化学平衡正向移动,的体积分数随温度升高而增大
(2) Ⅱ
(3)3.3(3分)
(4)温度越高,催化剂活性越大,反应速率越快,相同时间内反应掉的越大,故的转化率越大
(5)降低 升高温度,更有利于副反应的发生容器编号
起始时各物质的物质的量/ml
达到平衡时体系能量的变化
CO
①
1
4
0
0
放出热量
②
2
8
0
0
放出QkJ热量
选项
条件
离子
A
溶液
、、、
B
水电离的的溶液
、、、
C
的溶液
、、、
D
澄清透明的溶液
、、、
选项
操作
现象
结论
A
用试纸分别测量溶液和溶液的
溶液的约为8,溶液的约为9
B
向的溶液中滴加2滴甲基橙
溶液呈黄色
溶液呈碱性
C
向滴有酚酞的氨水中加入固体
溶液的红色变浅
溶液呈酸性
D
相同的铝片分别与同温同体积,且的盐酸、硫酸反应
铝与盐酸反应产生气泡较快
可能是对该反应起到促进作用
弱电解质
HCOOH
HCN
电离常数
、
A.制备无水
B.测稀硫酸的
C.比较和的金属性
D.探究浓度对化学反应速率的影响
编号
待测溶液/50mL
溶液温度/℃
pH
①
溶液
25
1.9
②
溶液
25
a
③
溶液
35
b
④
对照溶液X
25
1.9
⑤
对照溶液Y
25
c
①用酸性溶液滴定溶液
②测定某盐酸的浓度
③记录滴定终点读数:12.20mL
④排除滴定管内气泡
⑤测定某NaOH溶液的浓度
实验1
用试纸测得溶液的约为8
实验2
向溶液中加入等体积盐酸
实验3
向溶液中加入等体积溶液
实验4
向浓溶液中加入浓溶液,有气体和沉淀生成
反应温度/℃
465
480
495
510
的转化率/%
5.5
12.1
17.3
28.4
的产率/%
4.7
9.5
12.8
18.5
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
C
B
A
C
C
A
D
D
C
B
A
C
A
C
B
相关试卷
这是一份辽宁省沈阳市第二十中学2023-2024学年高二下学期4月阶段测试化学试题(含答案),共9页。试卷主要包含了4LCO2,00t苯可制得 1,3%,5mI,振荡后加热等内容,欢迎下载使用。
这是一份辽宁省沈阳市第二十中学2023-2024学年高二下学期4月阶段测试化学试题(PDF版含答案),共14页。
这是一份辽宁省实验中学2023-2024学年高二上学期期中阶段测试化学试题,共8页。试卷主要包含了单选题,填空题等内容,欢迎下载使用。









