

第15讲 氨气和铵盐-新高一化学暑假精品课程(鲁科版2019)(原卷版)
展开
这是一份第15讲 氨气和铵盐-新高一化学暑假精品课程(鲁科版2019)(原卷版),共9页。
1.掌握氨气和铵盐的主要性质和用途。
2.了解氨气和铵盐的检验方法。
3.了解化学肥料可能产生的负面影响。
【基础知识】
一、氨气的性质
1.物理性质
(1)色味态:______色、有_______气味的气体
(2)密度:比空气___________
(3)溶解性
①____溶于水,常温、常压下,一体积水能溶解约_____体积氨
②不溶于_________
(4)熔沸点:氨的沸点为-33.5℃,易________
2.碱性气体
(1)水:________________________________
(2)指示剂:能够使紫色石蕊试液变_________,酚酞试液变_______
(3)盐酸
①反应:________________________________
②现象:遇挥发性酸产生_______,同_______
③应用:检验氨气
(4)硫酸:________________________________
3.还原性
(1)催化氧化:________________________________
(2)热的CuO:________________________________
4.用途
(1)制硝酸和硝酸铵:N2→NH3→NO→NO2→HNO3→NH4NO3
(2)致冷剂:______气化时要吸收大量的热,使周围的温度急剧降低
(3)制化肥
①硝铵:________________________________
②硫铵:________________________________
③碳铵:________________________________
(4)化学氮肥的分类
1.将氨气通过一个盛有红热的Pt丝和氧气的锥形瓶中,在锥形瓶中可能生成哪些含氮化合物?
2.喷泉实验前如何证明圆底烧瓶中几乎充满了氨气?
3.喷泉实验后如何验证原来圆底烧瓶中是否充满了氨气?
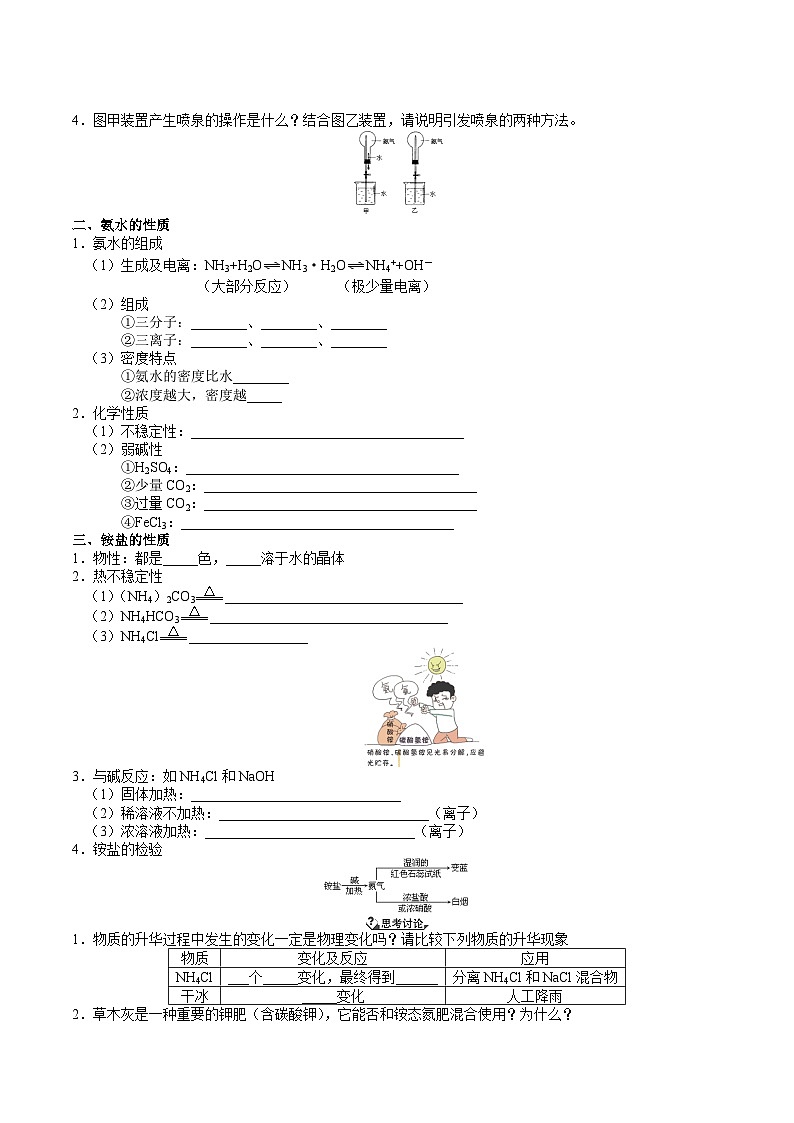
4.图甲装置产生喷泉的操作是什么?结合图乙装置,请说明引发喷泉的两种方法。
二、氨水的性质
1.氨水的组成
(1)生成及电离:NH3+H2O⇌NH3·H2O⇌NH4++OH-
(大部分反应) (极少量电离)
(2)组成
①三分子:________、________、________
②三离子:________、________、________
(3)密度特点
①氨水的密度比水________
②浓度越大,密度越_____
2.化学性质
(1)不稳定性:_______________________________________
(2)弱碱性
①H2SO4:_______________________________________
②少量CO2:_______________________________________
③过量CO2:_______________________________________
④FeCl3:_______________________________________
三、铵盐的性质
1.物性:都是_____色,_____溶于水的晶体
2.热不稳定性
(1)(NH4)2CO3__________________________________
(2)NH4HCO3__________________________________
(3)NH4Cl_________________
3.与碱反应:如NH4Cl和NaOH
(1)固体加热:______________________________
(2)稀溶液不加热:______________________________(离子)
(3)浓溶液加热:______________________________(离子)
4.铵盐的检验
1.物质的升华过程中发生的变化一定是物理变化吗?请比较下列物质的升华现象
2.草木灰是一种重要的钾肥(含碳酸钾),它能否和铵态氮肥混合使用?为什么?
四、氨气的实验室制法
1.常规方法
(1)实验装置
(2)药品____________和____________
(3)反应:____________________________________
(4)干燥:盛有________或________的干燥管(或U形管)
(5)收集
①排空气法:向_____排空气法
②排液体法:排__________法
(6)验满方法
①将_______________试纸放在试管口处,若试纸变______,则说明氨气已收集满。
②用玻璃棒蘸取_________靠近试管口处,若产生________,则说明氨气已收集满。
(7)尾气吸收:棉花用__________浸湿,目的是________________
(8)棉化作用:________________________________
2.以浓氨水为原料制备氨气
(1)制备原理:NH3·H2ONH3↑+H2O
(2)发生装置
或或
(3)药品
①浓氨水和NaOH固体
②生石灰和浓氨水
(4)原理
①NaOH固体溶于水放出大量的热,加速氨水的分解
②生石灰和水反应放出大量的热,加速氨水的分解
1.判断下列离子方程式书写是否正确?
(1)碳酸铵溶液与氢氧化钠溶液反应:NH4++OH-NH3·H2O
(2)碳酸氢铵溶液与足量烧碱溶液反应:NH4++OH-NH3·H2O
(3)碳酸铵与苛性钾溶液共热:NH4++OH-NH3↑+H2O
(4)实验室用氯化铵与石灰乳共热制氨气:NH4++OH-NH3↑+H2O
(5)在溶液中碳酸氢铵与等物质的量氢氧化钠混合:NH4++HCO3-+2OH-CO32-+NH3↑+2H2O
(6)过量的NH4HSO4溶液与Ba(OH)2溶液反应:2H++SO42-+Ba2++2OH-BaSO4↓+2H2O
【考点剖析】
考点一:氨气和氨水的性质
例1.(2020·陕西渭南高一上期末检测)如图,利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一表面皿扣在上面。下表中对实验现象所做的解释正确的是( )。
考点二:喷泉实验的原理及应用
例2.(2020·辽宁沈阳高一上期末)如图是课外活动小组的同学设计的4个喷泉实验方案。下列有关操作不可能引发喷泉现象的是( )。
A.挤压装置①的胶头滴管使CCl4全部进入烧瓶,片刻后打开止水夹
B.挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹
C.用鼓气装置从装置③的a处不断鼓入空气并打开止水夹
D.向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹
考点三:氨的催化氧化实验
例3.某兴趣小组用如图装置探究氨的催化氧化。
(1)氨催化氧化的化学方程式为__________________。
(2)加热玻璃管2一段时间后,挤压1中打气球鼓入空气,观察到2中物质呈红热状态;停止加热后仍能保持红热,该反应是________反应(填“吸热”或“放热”)。
(3)为保证在装置4中观察到红棕色气体,装置3应装入____;若取消3,在4中仅观察到大量白烟,原因是_________________。
(4)为实现氨的催化氧化,也可用装置5替换装置________(填装置代号);化合物X为________(只写一种),Na2O2的作用是____________________________。
考点四:铵盐的性质及检验
例4.(2020·江苏常州高一上期末)为确定两种化肥的混合物的组成,进行下如实验:
(1)取少量样品与消石灰共热,放出可使湿润的红色石蕊试纸变蓝的气体,证明化肥中含有______离子。
(2)将上述反应后所得固体加入盐酸中,生成无色无味气体,将所得逞气体通入澄清石灰水后出现浑浊现象,证明化肥中含有______离子或______离子。
(3)另取少量样品溶于水,得无色透明溶液,加入MgCl2溶液后无明显变化,可知化肥中一定含有______离子,而排除了______离子。
(4)向样品的水溶液中,加入用盐酸酸化的BaCl2溶液,立即产生白色沉淀,可知化肥中含有______离子。
以上事实说明两种化肥分别是____________和____________。
考点五:氨气的实验室制法
例5.(2020·福建龙岩高一上期末)利用如图装置(夹持装置略)制取和收集纯净、干燥的氨气,并探究氨气的性质。
(1)关闭装置Ⅰ中的止水夹,向分液漏斗中加入适量水,打开活塞,说明装置Ⅰ气密性良好的现象是__________________。
(2)利用装置Ⅰ制取氨气,应选用的试剂为浓氨水和________(填标号)。
A.氢氧化钠 B.浓硫酸 C.硝酸钾 D.生石灰
(3)根据实验要求,仪器连接的顺序(用字母编号表示):a接____,____接____,____接____。
(4)将氨气通入盛有氧化铜粉末的玻璃管中,加热有红色固体和无色气体单质生成,证明氨气具有________性,反应的化学方程式是________________________。
(5)收集氨气,按如图玻璃装置进行实验。先打开旋塞①,B瓶中产生白色的烟,原因是_____________________________(用化学方程式表示);稳定后,关闭旋塞①,再打开旋塞②,B瓶中的现象是________________________。
【真题演练】
1.(2020年7月·湖南合格考真题)下列气体溶于水,所得溶液呈碱性的是( )。
A.HCl B.CO2 C.NH3 D.SO2
2.(2020·北京合格考真题)下列物质中,既含有氨分子,又含有铵根离子的是( )。
A.氨气 B.氨水 C.硝酸 D.硝酸钾
3.(2020·全国卷Ⅲ)喷泉实验装置如图所示。应用下列各组气体-溶液,能出现喷泉现象的是( )。
4.(2020•上海学业考试真题)已知:8NH3+3Cl2=N2+6NH4Cl,该反应可以检查管道少量的氯气泄漏,下列叙述正确的是( )。
A.可以检验氯气泄漏的现象是产生无色气体
B.NH4Cl既是氧化产物又是还原产物
C.被氧化的NH3占全部NH3的25%
D.转移0.3ml电子,生成气体6.72L氮气(标准状况下)
【过关检测】
1.实验室可以按如图所示的装置干燥、收集气体M,多余的气体可用水吸收,则M是( )。
A.NH3 B.NO C.Cl2 D.NO2
2.在1 L 1ml/L的氨水中( )。
A.含1ml NH3分子
B.含NH3和NH4+之和为1ml
C.含NH3、NH4+、NH3·H2O之和为1ml
D.含NH3·H2O为1ml
3.(2020·辽宁抚顺高一上期末)将下列固体加入到NH4Cl溶液中,不能生成NH3的是( )。
A.Na B.Na2O C.NaOH D.NaHCO3
4.氨水显弱碱性的主要原因是( )。
A.通常状况下,氨的溶解度不大
B.氨水中的NH3·H2O电离出少量的OH-
C.溶于水的氨分子只有少量电离
D.氨本身的碱性弱
5.(2020·上海金山区高一上期末)关于氯化铵的说法,不正确的是( )。
A.是一种铵态氮肥 B.属于共价化合物
C.存在离子键和共价键 D.受热分解产生氨气
6.现欲分离NaCl和NH4Cl,下列方法正确的是( )
A.加入AgNO3溶液 B.加入NaOH溶液
C.加入水 D.加热并冷却
7.下列有关氨水的说法正确的是( )。
A.氨水是弱电解质
B.浓氨水敞口久置,浓度变小
C.分别蘸有浓氨水和浓硫酸的玻璃棒靠近有白烟产生
D.浓氨水用磨口玻璃塞的细口瓶盛装
8.能鉴别Na2SO4、NH4NO3、KCl、(NH4)2SO4四种溶液(可以加热)的一种试剂是( )。
A.BaCl2 B.Ba(NO3)2 C.Ba(OH)2 D.AgNO3
9.(2021·河南周口高一上期末检测)下列反应中说明NH3既有还原性,又有碱性的是( )。
A.4NH3+5O24NO+6H2O
B.NH3+HNO3=NH4NO3
C.8NH3+3Cl2=N2+6NH4Cl
D.2NH3+3CuO3Cu+N2+3H2O
10.(2020·北京丰台区高一上期末)如图是喷泉实验装置图,下列说法不正确的是( )。
A.烧瓶中的溶液呈红色
B.该实验说明氨气可电离产生OH-
C.该实验说明氨气易溶于水
D.形成喷泉的原因是烧瓶内压强小于外界大气压
11.(2020·江西景德镇高一上期末)在右图的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是( )。
A.Cu与稀盐酸 B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸 D.NH4HCO3与稀盐酸
12.(2020·辽宁大连高一上期末)如图所示,在一个密闭的玻璃管两端各放一团棉花,再用注射器同时在两端注入适量的浓氨水和浓盐酸,下列说法不正确的是( )。
A.玻璃管中发生的反应可表示为:NH3+HCl=NH4Cl
B.用手触摸玻璃管外壁,会感觉到有热量放出
C.实验时会在玻璃管的B处附近看到白雾
D.将浓盐酸换成浓硝酸也会有相似现象
13.(2020·安徽铜陵高一上期末)下列离子方程式书写正确的是( )。
A.实验室用氯化铵和熟石灰制氨:NH4++OH-NH3↑+H2O
B.NaOH溶液与NH4Cl溶液混合加热:NH4++OH-NH3·H2O
C.氨水中加盐酸:NH3·H2O+H+=NH4++H2O
D.氨水中加入氯化铁溶液:Fe2++2NH3·H2O=2NH4++Fe(OH)2↓
【解析】选C。实验室制NH3用固体NH4Cl和熟石灰共热,不能写成离子方程式;B项应为NH4++OH-NH3↑+H2O;D项应为Fe3++3NH3·H2O=3NH4++Fe(OH)3↓。
14.(2020·吉林延边高一上期末)已知X、Y、Z、W(含同一元素)有如下所示转化关系,且X能与W发生反应生成一种易溶于水的盐,则X可能是( )。
A.N2 B.NO2 C.NH3 D.NO
15.下列装置用于实验室中制取干燥氨气的实验,能达到实验目的的是( )。
A.用装置甲制备氨气
B.用装置乙除去氨气中少量水
C.用装置丙收集氨气
D.用装置丁吸收多余的氨气
16.(2020·浙江绍兴高一上期末)下列装置用于实验室中制取干燥氨气的实验,能达到实验目的的是( )。
A.用装置甲制备氨气
B.用装置乙除去氨气中少量水
C.用装置丙收集氨气
D.用装置丁吸收多余的氨气
17.(2020·江苏徐州高一上期末)NH3是一种重要的化工原料,可以制备一系列物质(如下图所示)。下列有关表述正确的是( )。
A.NH4Cl和NaHCO3都是常用的化肥
B.NH4Cl、HNO3和Na2CO3受热时都易分解
C.NH3和NO2在一定条件下可能发生氧化还原反应
D.图中所涉及的反应都是氧化还原反应
18.(2020·四川蓉城名校联盟高一上期末联考)实验室模拟氨催化氧化法制硝酸的装置如图所示。下列说法错误的是( )。
A.装置①、②、⑤依次盛装碱石灰、P2O5、NaOH溶液
B.装置③中产生红棕色气体
C.装置④中溶液可使紫色石蕊溶液变红,说明有HNO3生成
D.通空气的主要作用是鼓出氨气,空气可用N2代替
19.(2020·浙江丽水高一上期末)某混合气体中可能含有H2、CO、CO2、HCl、NH3和H2O(g)中的两种或多种,当混合气体依次通过澄清的石灰水(无浑浊现象)、氢氧化钡溶液(有浑浊现象)、浓硫酸(无明显现象)、灼热的氧化铜(变红)、无水硫酸铜(变蓝)。对该混合气体成分的正确判断是( )。
A.一定没有CO2,肯定有H2
B.一定有CO2、CO和H2O(g)
C.可能有CO2、NH3和H2O(g)
D.一定有H2、CO2和HCl
20.(2020·河北承德高一上期末)把0.5L含硫酸铵和硝酸铵的混合液分成两等份,一份用3ml氢氧化钠刚好把氨全部赶出,另一份与1ml氯化钡恰好完全反应,由此可知原溶液中NO3-的物质的量浓度为( )。
A.1ml·L-1 B.2ml·L-1
C.4ml·L-1 D.0.5ml·L-1
21.利用如图所示的装置,可以验证NH3和HCl的有关性质。实验前a、b、c活塞均关闭。
(1)若要在烧瓶Ⅱ中产生“喷泉”现象,烧瓶I中不产生“喷泉”现象,其操作方法_____________________________。
(2)若先打开a、c活塞,再挤压胶头滴管(假设NH3不被完全吸收),在烧瓶中可观察到的现象是_____________________。
(3)通过挤压胶头滴管和控制活塞的开关,在烧瓶I中产生“喷泉”现象,烧瓶Ⅱ中不产生“喷泉”现象,其操作方法是__________________________________。
22.科学合理地保存、施用氮肥。
(1)NH4HCO3需阴凉处保存,原因是________________(写化学方程式)。
(2)铵态氮肥不能与碱性肥料混合使用,以NH4Cl为例写出发生反应的离子方程式________________________________。
(3)尿素CO(NH2)2是一种常用化肥,缓慢与H2O发生非氧化还原反应释放出NH3则尿素中C元素化合价为__________。
23.(2020·福建泉州高一上期末)碳铵是一种较常使用的化肥,它在常温下易分解。某化学兴趣小组对碳铵的成分存在疑问,进行了如下探究。
【定性实验】检验溶液中的阴、阳离子。取少量固体放入试管中,加入盐酸,把生成的气体通入澄清石灰水中,有白色沉淀生成。再另取少量碳铵放入试管中,加入浓NaOH溶液,加热,用湿润的红色石蕊试纸检验生成的气体,石蕊试纸变蓝色。
(1)根据实验现象,推测碳铵中所含有阴离子可能是________和________。
(2)根据实验现象,碳铵与NaOH溶液反应的离子方程式可能是________________。
【定量实验】测定碳铵中C元素和N元素质量比。该兴趣小组准确称取a g碳铵,加热使之分解,并把产物通入碱石灰中,如下图所示。
(3)碳铵固体应放在________中进行加热。
A.试管 B.蒸发皿 C.烧瓶 D.坩埚
(4)从安全的角度考虑,尾气处理的装置可以选用________。
(5)若灼烧后没有固体残余,称量U形管在实验前后的质量差为b g。由此测得N元素的质量是________g。
分类
______氮肥
______氮肥
________氮肥
举例
NH4HCO3
KNO3
CO(NH2)2
物质
变化及反应
应用
NH4Cl
___个_____变化,最终得到______
分离NH4Cl和NaCl混合物
干冰
_____变化
人工降雨
选项
实验现象
解释
A
浓盐酸附近产生白烟
NH3与浓盐酸反应产生了NH4Cl固体
B
浓硫酸附近无明显现象
NH3与浓硫酸不发生反应
C
氯化物溶液变浑浊
该溶液一定是AlCl3溶液
D
干燥红石蕊试纸不变色,湿润红石蕊试纸变蓝
NH3是一种可溶性碱
选项
气体
溶液
A
H2S
稀盐酸
B
HCl
稀氨水
C
NO
稀H2SO4
D
CO2
饱和NaHCO3溶液
相关试卷
这是一份第16讲 硝酸-新高一化学暑假精品课程(鲁科版2019)(原卷版),共8页。
这是一份第14讲 氮气和氮的氧化物-新高一化学暑假精品课程(鲁科版2019)(原卷版),共7页。
这是一份第13讲 硫的转化-新高一化学暑假精品课程(鲁科版2019)(原卷版),共10页。









