
江苏省扬州大学附属中学2024-2025学年高二上学期10月月考 化学试卷
展开1.“3060”双碳目标的重点是推动以二氧化碳为主的温室气体减排,下列说法错误的是
A. 研发新型催化剂将CO₂分解成C和O₂,同时放出热量
B. 燃煤中适当添加石灰石,减少污染气体排放
C. 一定条件下, 将CO₂转化为CH₃OH, 实现CO₂的资源化利用
D. 逐步用太阳能、潮汐能、风能、氢能等清洁能源替代火力发电
2. 下列反应是放热反应的是
A. Ba(OH)₂•8H₂O 与NH₄Cl混合 B. Al和Fe₂O₃高温条件下反应
C. 碳与水蒸气制取“水煤气” D. 高温煅烧石灰石
3. 甲醇是一种高效清洁的新能源,1ml甲醇完全燃烧生成液态水时放出900kJ热量,则下列关于甲醇标准燃烧热的热化学反应方程式正确的是
A.2CHₛOH1+3O₂g=2CO₂g+4H₂O1 ΔH=-1800kJ⋅ml-1
B.CH3OH1+32O2g=CO2g+2H2Og ΔH=-900kJ⋅ml-1
C.CH3OH1+32O2g=CO2g+2H2O1 ΔH=-900kJ⋅ml-1
D.2CH₃OH(l) +3O₂(g)=2CO₂(g) +4H₂O (l) ΔH=+1800kJ· ml-¹
4. 已知: 2H₂g+O₂g=2H₂Og△H=-483.6kJ⋅ml⁻¹,下列说法正确的是
A. 标准状况下, lmlH₂(g)与0.5mlO₂(g)反应生成lmlH₂O放出的热量为241.8kJ
B. 在相同条件下, lmlH₂(g)与0.5mlO₂(g)的能量总和大于 lmlH₂O(g)的能量
C. 8g水蒸气完全分解成氢气和氧气吸收483.6kJ热量
D. 常温下, 2mlH₂与 lmlO₂完全反应生成液态水放出的热量小于 483.6kJ
5. 下列关于轮船嵌有锌块实施保护的判断不合理的是
A. 腐蚀的正极反应: 2H₂O+O₂+4e=4OH-
B. 可用镁合金块代替锌块进行保护
C. 嵌入锌块后的负极反应: Fe-2e=Fe²⁺
D. 该方法采用的是牺牲阳极的阴极保护法
6. 下列措施对增大反应速率明显有效的是
A. Na与水反应时,增大水的用量
B. Fe与稀硫酸反应制取氢气时,将稀硫酸改用浓硫酸
C. 在K₂SO₄与BaCl₂两溶液反应时, 增大压强
D. N₂与H₂合成氨气时,适当增大体系的压强
7. 一定条件下,将等体积的NO₂和SO₂置于密闭容器中发生反应NO2(g)+SO2(g)
SO3(g)+NO(g),下列不能说明反应达平衡状态的是
A.V正SO2=V逆SO3 B. 混合气体颜色保持不变
C. SO₃和NO体积分数比保持不变 D. NO₂的浓度保持不变
8. 可逆反应 3Fes+4H₂Og=Fe₃O₄s+4H₂g在容积可变的密闭容器中进行,下列条件的改变对其反应速率几乎无影响的是
A. 保持容器体积不变,加入水蒸气
B. 将容器的容积缩小一半
C. 保持容器容积不变,充入稀有气体使体系压强增大
D. 保持压强不变,充入N₂使体系容积增大
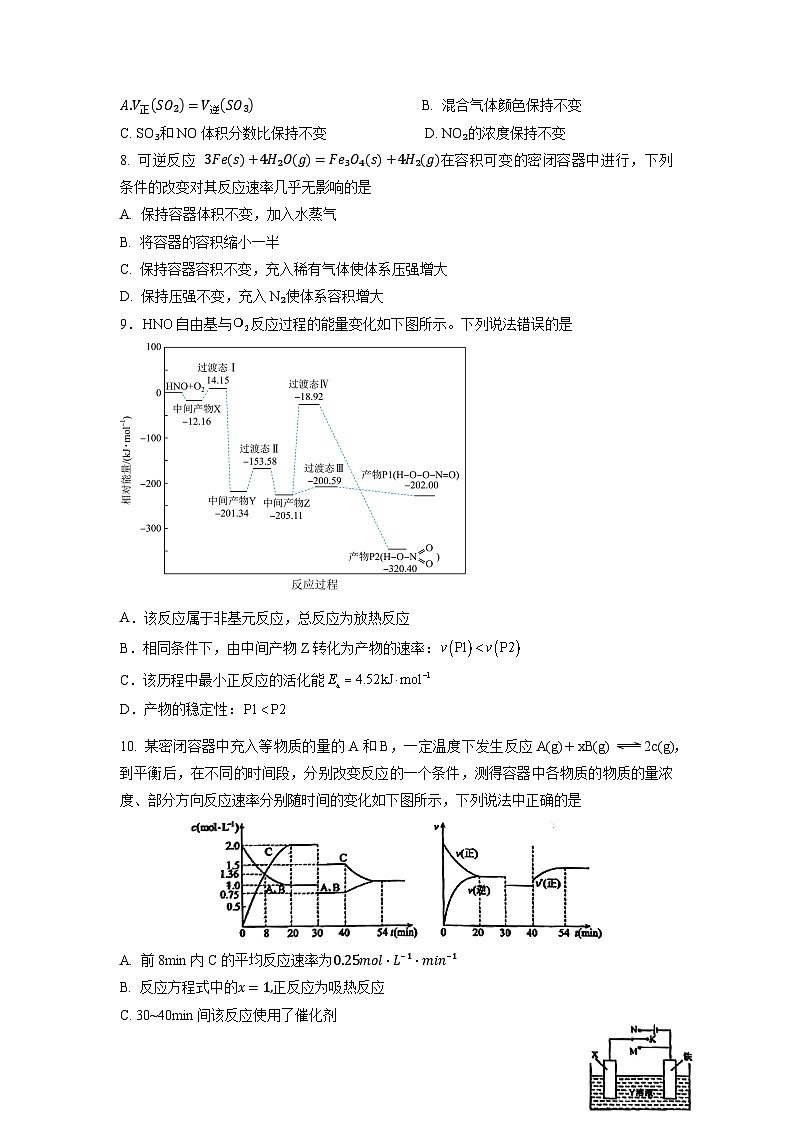
9.自由基与反应过程的能量变化如下图所示。下列说法错误的是
A.该反应属于非基元反应,总反应为放热反应
B.相同条件下,由中间产物Z转化为产物的速率:
C.该历程中最小正反应的活化能
D.产物的稳定性:
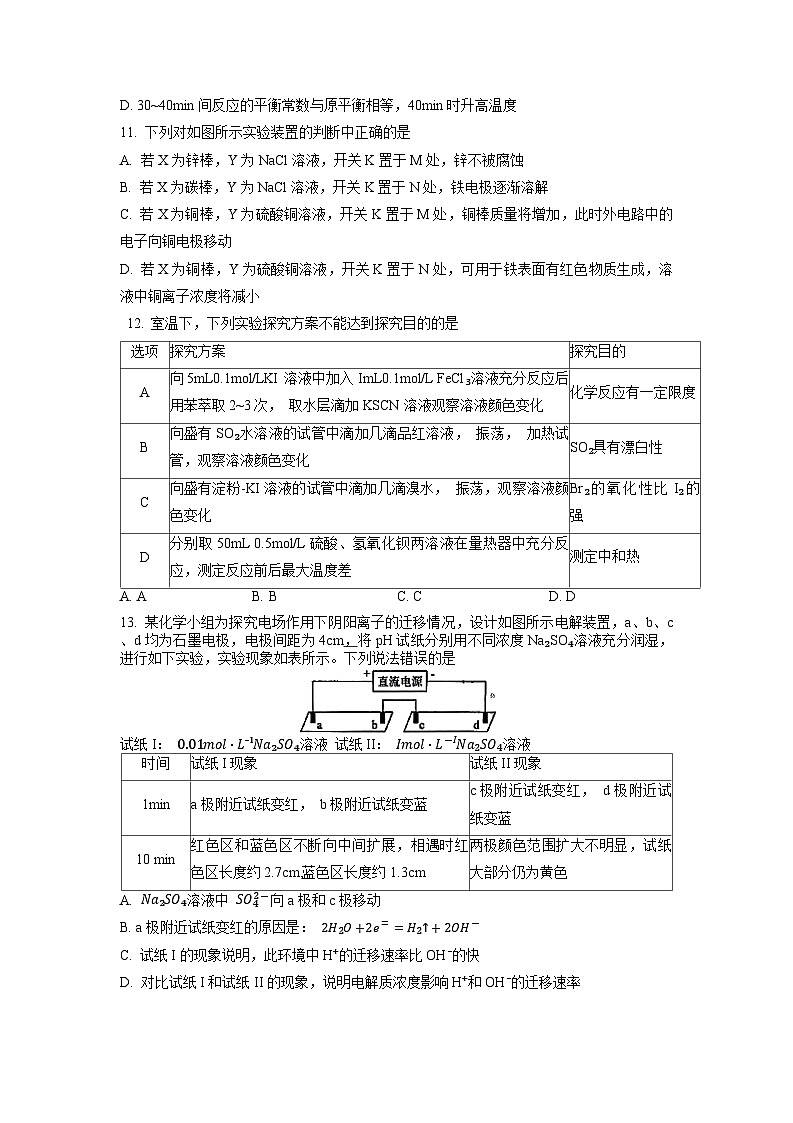
10. 某密闭容器中充入等物质的量的A和B,一定温度下发生反应A(g)+xB(g)
2c(g),到平衡后,在不同的时间段,分别改变反应的一个条件,测得容器中各物质的物质的量浓度、部分方向反应速率分别随时间的变化如下图所示,下列说法中正确的是
A. 前8min内C的平均反应速率为0.25ml⋅L⁻¹⋅min⁻¹
B. 反应方程式中的x=1,正反应为吸热反应
C. 30~40min间该反应使用了催化剂
D. 30~40min间反应的平衡常数与原平衡相等,40min时升高温度
11. 下列对如图所示实验装置的判断中正确的是
A. 若X为锌棒,Y为NaCl溶液,开关K置于M处,锌不被腐蚀
B. 若X为碳棒,Y为NaCl溶液,开关K置于N处,铁电极逐渐溶解
C. 若X为铜棒,Y为硫酸铜溶液,开关K置于M处,铜棒质量将增加,此时外电路中的电子向铜电极移动
D. 若X为铜棒,Y为硫酸铜溶液,开关K置于N处,可用于铁表面有红色物质生成,溶液中铜离子浓度将减小
12. 室温下,下列实验探究方案不能达到探究目的的是
A. A B. B C. C D. D
13. 某化学小组为探究电场作用下阴阳离子的迁移情况,设计如图所示电解装置,a、b、c、d均为石墨电极,电极间距为4cm,将pH试纸分别用不同浓度Na₂SO₄溶液充分润湿,进行如下实验,实验现象如表所示。下列说法错误的是
试纸I: 0.01ml⋅L⁻ˡNa₂SO₄溶液 试纸II: Iml⋅L-INa2SO4溶液
Na₂SO₄溶液中 SO42-向a极和c极移动
B. a极附近试纸变红的原因是: 2H2O+2e==H2↑+2OH-
C. 试纸I的现象说明,此环境中H⁺的迁移速率比OH⁻的快
D. 对比试纸I和试纸II的现象,说明电解质浓度影响H⁺和OH⁻的迁移速率
二、解答题
14.(本题14分)氢元素单质及其化合物是人类赖以生活的重要能源。回答下列问题:
(1)肼(N2H4)是一种液态火箭推进剂。N2H4分解的能量变化如图所示:
①正反应的活化能为 kJ·ml-1,气态肼分解的热化学方程式为 。
②该反应断开反应物中化学键吸收的总能量 (填“>”“<”或“=”)形成生成物中化学键放出的总能量。
(2)盖斯定律认为:不管化学过程是一步完成或分多步完成,整个过程的总热效应相同。试运用盖斯定律回答下列问题:
①反应A+B→C(△H<0)分两步进行:
(i)A+B→X(△H>0)
(ii)X→C(△H<0)
下列示意图中,能正确表示总反应过程中能量变化的是 (填字母)。
②已知:H2O(g)=H2O(l) △H1=-Q1kJ·ml-1
C2H5OH(g)=C2H5OH(1) △H2=-Q2kJ·ml-1
C2H5OH(g)+3O2(g)=2CO2(g)+3H2O(g) △H3=-Q3kJ·ml-1
则C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(l)的△H= kJ·ml-1,若将23g液态无水酒精完全燃烧,并恢复到室温,则整个过程中放出的热量为 kJ。
15.(本题16分)实际生产生活中,钢铁等金属因电化学腐蚀损失巨大,而电化学在金属制备和加工中也发挥着重要的作用。
(1)生活中钢铁腐蚀以吸氧腐蚀为主,该腐蚀过程中正极的电极反应式为 。金属的两种常见电化学防护方法如下图所示,图甲中铁闸门连接电源的 (填“正极”或“负极”),图乙所示金属的防护方法称为 。
(2)某科研单位利用—空气质子交换膜燃料电池制备高纯铬和硫酸的简单装置如下图所示:
①(Ⅱ)电极为 (填“正极”“负极”“阴极”或“阳极”),(Ⅰ)电极上发生的电极反应式为 。
②X膜为 交换膜(填“阴离子”或“阳离子”)。
③理论上,Pt(Ⅱ)电极上参加反应的O2标况下为1.68L,则Cr棒增重 g。( Cr-52)
16. (本题14分)烟气(主要污染物SO2、NOx)经O3预处理后用碱液吸收,可减少烟气中SO2、NOx的含量。常温下,O3是一种有特殊臭味、稳定性较差的淡蓝色气体。O3氧化烟气中NOx时主要反应的热化学方程式为:
2NO(g) +O2(g)=2NO2(g) △H1= a kJ·ml-1
NO(g) +O3(g)=NO2(g) +O2(g) △H2= b kJ·ml-1
4NO2(g) +O2(g) =2N2O5(g) △H3= c kJ·ml-1
(1)反应6NO2 (g) +O3(g)=3N2O5(g) △H= kJ·ml-1。
(2)O3氧化NO的氧化率随温度变化情况如图-1。随着温度升高NO的氧化率下降的原因可能是 。NO也可被O3氧化为 NO2、NO3,用NaOH溶液吸收若只生成一种盐,写出氢氧化钠吸收二氧化氮和三氧化氮的离子方程式 。
(3)一定条件下,向NOx/O3混合物中加入一定浓度的SO2气体,进行同时脱硫脱硝实验。实验结果如图-2。同时脱硫脱硝时NO的氧化率略低的原因是 ;由图可知SO2对 NO的氧化率影响很小,下列选项中能解释该结果的是 (填序号)。
a.O3氧化SO2反应的活化能较大
b.O3与NO反应速率比O3与SO2反应速率快
c.等物质的量的O3与NO反应放出的热量比与SO2反应的多
(4)尿素[CO(NH2)2]在高温条件下与NO反应转化成三种无毒气体,该反应的化学方程式为 。也可将该反应设计成碱性燃料电池除去烟气中的氮氧化物,该燃料电池负极的电极反应式是 。
17. (本题17分) 研究与的反应对减缓燃料危机和减弱温室效应具有重大意义。
与发生反应Ⅰ:
在反应过程中还发生反应Ⅱ:
(1)①反应Ⅰ的 0(填“>”或“<”)。
②已知部分化学键的键能数据如下:
则 。
(2)在刚性密闭容器中充入一定量的与,下列能判断反应Ⅰ达到平衡状态的是___(填标号)。
A.在绝热容器中,温度保持不变
B.恒温时,混合气体的密度保持不变
C.恒温时,混合气体中与的物质的量浓度相等
D.恒温时,和的物质的量之和保持不变
(3)将与按物质的量之比1∶1投料时,和的平衡转化率随温度变化关系如图所示。
①923K时,的平衡转化率大于的原因是 。
②923K时,反应Ⅱ的化学平衡常数 (计算结果保留小数点后两位)。
(4)以表面覆盖的二氧化钛为催化剂,可以将和直接转化成乙酸。
①为了提高该反应中的平衡转化率,可以采取的措施是 (任写一种)。
②催化剂在该反应中的作用是 (填标号)。
A.降低反应的活化能 B.降低反应的焓变
C.改变反应的历程 D.增大反应的平衡常数K
③923K时, 投入CH4与CO2的物质的量均为1ml,求此时体系内吸收的总热量 kJ。选项
探究方案
探究目的
A
向5mL0.1ml/LKI溶液中加入ImL0.1ml/L FeCl₃溶液充分反应后用苯萃取2~3次, 取水层滴加KSCN溶液观察溶液颜色变化
化学反应有一定限度
B
向盛有SO₂水溶液的试管中滴加几滴品红溶液, 振荡, 加热试管,观察溶液颜色变化
SO₂具有漂白性
C
向盛有淀粉-KI溶液的试管中滴加几滴溴水, 振荡,观察溶液颜色变化
Br₂的氧化性比I₂的强
D
分别取50mL 0.5ml/L硫酸、氢氧化钡两溶液在量热器中充分反应,测定反应前后最大温度差
测定中和热
时间
试纸I现象
试纸II现象
1min
a极附近试纸变红, b极附近试纸变蓝
c极附近试纸变红, d极附近试纸变蓝
10 min
红色区和蓝色区不断向中间扩展,相遇时红色区长度约2.7cm,蓝色区长度约1.3cm
两极颜色范围扩大不明显,试纸大部分仍为黄色
化学键
H-O
H-H
C=O
键能()
413
436
803
1076
参考答案
选择题
填空题
14、(1)①a+50.7;N2H4(g)=N2(g)+2H2(g) ∆H=+50.7kJ·ml-1 ;② >
(2) D Q2-Q3-3Q1
15、(1) O2+4e-+2H2O=4OH- ; 负极 ; 牺牲阳极的阴极保护法
(2) 正极 ; NO+2H2O-3e-=NO+4H+ ; 阴离子交换膜 ; 5.2
16、(1)32c+b-a2O3
(2)O3在较高温度下易分解 ;2NaOH+NO2+NO3=2NaNO3+H2O
(3)SO2的氧化消耗了少量O3,减小了O3的浓度 ;a b
(4)2CO(NH2)2+ 6NO5N2+2CO2+4H2O ;CO(NH2)2 - 6e- + 8OH- = CO32- + N2↑+ 6H2O
17、(1) > ; +140
(2)AD
(3)反应Ⅰ中和的转化率相同,又发生反应Ⅱ,转化率增大 ; 0.39
(4)增大浓度、增大压强等 ; A C ;154.4 1
2
3
4
5
6
7
8
9
10
A
B
C
B
D
D
C
C
B
D
11
12
13
C
A
B
江苏省扬州大学附属中学2024-2025学年高一上学期10月阶段检测化学试题(无答案): 这是一份江苏省扬州大学附属中学2024-2025学年高一上学期10月阶段检测化学试题(无答案),共6页。试卷主要包含了实验中的下列操作正确的是,下列有关分散系的说法正确的是,下列反应中属于氧化还原反应的是等内容,欢迎下载使用。
北京理工大学附属中学2024-2025学年高二上学期10月月考化学试题: 这是一份北京理工大学附属中学2024-2025学年高二上学期10月月考化学试题,文件包含北京市海淀区北京理工大学附属中学高二化学10月月考pdf、北京市海淀区北京理工大学附属中学高二化学10月月考答案pdf等2份试卷配套教学资源,其中试卷共8页, 欢迎下载使用。
江苏省扬州大学附属中学东部分校2024-2025学年高一上学期9月月考 化学试卷: 这是一份江苏省扬州大学附属中学东部分校2024-2025学年高一上学期9月月考 化学试卷,文件包含扬大附中东部分校2024-2025学年第一学期第一次模块学习效果调查高一年级化学学科试题pdf、月考答案pdf等2份试卷配套教学资源,其中试卷共5页, 欢迎下载使用。












